Способ селективной очистки детонационного наноалмаза
Иллюстрации
Показать всеИзобретение относится к области неорганической химии углерода, а именно: к нанодисперсным углеродным материалам и способу их очистки, и может быть использовано в различных высокотехнологичных областях промышленности и науки, где применяются порошки детонационных наноалмазов. В исходный алмазосодержащий порошок добавляют порошковый алюминий в количестве не менее 5 мас.%, смесь перемешивают, прессуют и отжигают образец при температуре 900-950° в вакууме при остаточном давлении не хуже 10-3 мм рт.ст. в течение 30 мин. В результате термодесобции осуществляется глубокая очистка поверхности детонационного наноалмаза от примесей, что позволяет получать в динамическом режиме новые композиционные алмазосодержащие материалы. 8 ил., 5 табл., 6 пр.
Реферат
Изобретение относится к области неорганической химии углерода, а именно к нанодисперсным углеродным материалам и способу их очистки, и может быть использовано в различных высокотехнологичных областях промышленности и науки для создания новых композиционных материалов.
Известен способ очистки детонационного наноалмаза от графита (Шебалин А.И., Молокеев В.А., Сакович Г.В. и др. Способ очистки алмаза от графита. // А.С. СССР №1770271 от 13.06.1984 //. Согласно этому способу, очистку исходной алмазосодержащей шихты осуществляют смесью азотной (HNO3) и серной (H2SО4) кислот или смесью HNO3, H2SО4 и SO3. Недостатком этого способа очистки детонационного наноалмаза является использование экологически опасных реагентов, к которым относится вышеуказанная смесь сильных кислот. Кроме того, происходит неконтролируемый процесс загрязнения исходного порошка молекулярными структурами исходных смесей, формирующими мощный адсорбционный примесный слой, экранирующий наноалмазное ядро, что затрудняет использование алмазосодержащий порошок для получения объемных или композиционных материалов.
Известен способ выделения синтетических алмазосодержащих веществ (Пузырь А.А., Воробьев В.Б., Бондарь B.C., Политченко Л.К. Синтетические алмазосодержашие вещества и способ их выделения. // Патент РФ №2306258, МПК С01В 31/06, опубликован 20.09.2007. // Алмазосодержащий порошок получают подрывом взрывчатого углеродсодержащего вещества, подвергают очистке путем отмывки в органических растворителях: хлороформе, бензоле, ацетоне, диметилформамиде, спирте путем кипячения в течение 10-15 минут в песчаной бане, выдерживая последовательность растворителей от гидрофобных до гидрофильных. После окончания процесса очистки растворитель удаляется декантацией, а порошок высушивается при температуре 80-100°С до влажности 1,5-2,0%.
Как следует из приведенных данных в состав алмазосодержащего порошка входит широкий спектр элементов, образующих поверхностный адсорбированный слой атомов примесей, в основном сильносвязанных с алмазным ядром. Об этом свидетельствуют приведенные данные, согласно которым получаемый порошок позволяет при многократном высушивании и простом добавлении воды получать устойчивые гидрозоли, что говорит о придании наночастицам свободнодисперсных свойств. Это свойство является недостатком способа очистки, не позволяющим использовать алмазосодержащий порошок для получения композиционных материалов, в которых наноалмазная компонента образует поликристаллические агрегаты при взаимодействии наночастиц друг с другом, а также с другими компонентами композита. Кроме того, процесс очистки приводит к замещению одних элементов примесной подсистемы на другие. В лучшем случае проводят контролируемый процесс замещения одних элементов на другие для придания тех или иных свойств алмазосодержащему порошку.
Известен также способ термодесорбции (Кощеев А.П. Термодесорбционная масс-спектроскопия в свете решения проблемы паспортизации и унификации поверхностных свойств детонационных наноалмазов. // Российский Хим. Журнал, 2008, т.LII, №5, с.88-96.) - прототип. При нагреве исследуемого образца с постоянной скоростью в вакууме или инертной атмосфере, в ходе которого с поверхности частицы образца происходит десорбция молекул и продуктов разложения поверхностных функциональных соединений. Установлено, что на поверхности нанокристаллов алмаза присутствуют кислород и водородсодержащие группы, разлагающиеся при нагреве с образованием Н2, СО и (или) СO2. Процесс десорбции осуществляется в широком интервале температур, и представляет собой последовательное выделение таких продуктов как вода (Н2О) в интервале температур 100-600°С, СO2 в температурном интервале 200-600°С, СО - в интервале 500-900°С, Н2 - в интервале свыше 800°С. В зависимости от изменения технологии очистки детонационных наноалмазов химические свойства поверхности частиц различны, не постоянны, что существенно снижает их практическое применение.
В то же время прогрев детонационного алмаза на воздухе при температуре 370°С в течение 1 часа приводит к удовлетворительному уровню содержания кислорода. Кроме того, отжиг при более высоких температурах нецелесообразен в связи с существенной потерей массы образцов, увеличении концентрации нелетучих соединений на поверхности наночастиц за счет выгорания алмазной фазы и сохранении нелетучих примесей соединений металлов, сохраняющих кислород даже при нагреве до 1000°С.
Таким образом, недостатками прототипа, являются:
1) невозможность нагрева до высоких температур в связи с выгоранием алмазной фазы;
2) сохранение нелетучих примесей соединений металлов, которые сохраняют кислород при нагреве даже до 1000°С.
Сущность изобретения
Предлагаемый способ селективной очистки детонационного наноалмаза проводят путем термодесорбции в вакууме, добавляют в исходный порошок детонационного наноалмаза порошковый алюминий в количестве не менее 5 мас.%, смесь перемешивают, прессуют и отжигают образец при температуре 900-950° в вакууме при остаточном давлении не хуже 10-3 мм рт.ст. в течение 30 мин, в ходе которого осуществляют более глубокую очистку наночастиц, вплоть до обнажения алмазного ядра.
Таким образом, способ селективной очистки детонационного наноалмаза избирательно меняет химический состав примесной подсистемы, при нагреве в вакууме до 200°С наночастицы освобождаются от воды, при нагреве до 320°С - от углеводородов, при нагреве до 480°С - от сероводорода, при нагреве до 580°С идет десорбция диоксида серы, до 680°С - идет десорбция углекислого газа, при нагреве до 760 и 860°С идет десорбция азота и водорода соответственно.
Примесная подсистема представляет собой совокупность атомов и молекулярных кластеров, находящихся в различном структурном состоянии и образующих обширную оболочку вокруг алмазного ядра, элементы которой могут быть как сильно связанными ковалентными связями, так и слабо связанными, например, с помощью Ван-дер-ваальсовских связей с алмазным ядром через подстилающий слой сильно связанных примесных атомов.
Задачей изобретения является получение детонационного наноалмаза с контролируемым заданным составом для создания новых композиционных алмазосодержащих материалов. Для достижения такой задачи:
1) осуществляют способ селективной очистки детонационного наноалмаза путем термодесорбции в вакууме,
2) добавляют в исходный порошок детонационного наноалмаза порошковый алюминий в количестве не менее 5 мас.%,
3.) смесь перемешивают, прессуют и отжигают образец при температуре 900-950° в вакууме при остаточном давлении не хуже 10-3 мм рт.ст. в течение 30 мин. выдержки исходного образца;
4) в процессе глубокой очистки детонационный наноалмаз рекристаллизуется в динамическом режиме с образованием прочных поликристаллических агрегатов.
Осуществление изобретения
Исходный порошок детонационного наноалмаза компактируют в таблетки диаметром 10 мм и толщиной 3-5 мм. Таблетки помещают в вакуумную печь при остаточном давлении не хуже 10-3 мм рт.ст. и нагревают в зависимости от практического использования до одной из температур, указанных выше. Для более глубокой очистки в исходный порошок детонационного наноалмаза добавляют не менее 5 мас.% алюминиевого порошка (алюминиевая пудра ПАП-1), готовят смесь путем перемешивания в смесителе, прессуют таблетки и затем проводят отжиг путем нагрева до температуры 950°С в вакууме при остаточном давлении не хуже 10-3 мм рт.ст.
Пример 1
Образцы готовят путем прессования таблеток диаметром 10 мм и толщиной около 3 мм на прессе усилием 1500 кг. Отжиг образцов детонационного наноалмаза осуществляют в вакуумной печи при давлении 10-5 торр путем нагрева до 950°С и выдерживают при этой температуре около 30 минут. Элементный состав определяют на установке с электронным и сфокусированным ионным пучками Quanta-200-3D в Материаловедческом центре коллективного пользования при Томском государственном университете.
Элементный состав исходного и отожженного наноалмаза приведен в таблице 1. Из приведенных в табл.1 данных следует, что в исходном наноалмазе основными примесями являются кислород, сера и железо. После проведения отжига содержание углеродной компоненты уменьшается, содержание серы также уменьшается, в то время как содержание кислорода возрастает. Из приведенных данных можно заключить, что повышение концентрации кислорода осуществляется за счет его вторичной адсорбции из атмосферы, так как концентрация других элементов, например серы, уменьшается.
Пример 2
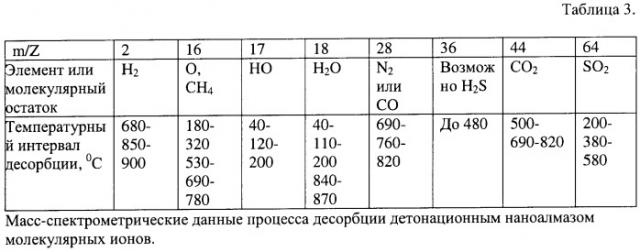
Для анализа кинетики десорбции был проведен отжиг детонационного наноалмаза, в ходе которого осуществляют регистрацию изменения давления в вакуумной камере системы. На фиг.1 приведена зависимость параметра давления от температуры при нагреве образца с умеренной скоростью.
Как следует из приведенных на фиг.1 данных десорбция адсорбированных молекул газа начинается сразу от момента нагрева образца и продолжается в температурном интервале до 800°С. Зависимость имеет три максимума газовыделения. В интервале температур до 400°С наблюдается десорбционный процесс с максимумом газовыделения около 200°С. При температуре около 430°С расположен второй максимум, выше 600°С наблюдается третий. Характерный вид зависимости (фиг.1) свидетельствует, что существуют как слабосвязанные, так и сильносвязанные с алмазным ядром примеси. Представленные данные, приведенные на фиг.1 в виде зависимости давления в вакуумной системе от температуры отжига, позволяют определить некоторые активационные параметры процесса десорбции атомов примеси. Активационные параметры определяют с помощью разработанного метода и программы вычисления эффективной энергии активации и предэкспоненциального множителя [Плотников В.А., Грязнов А.С., Макаров С.В. Свидетельство о государственной регистрации программы для ЭВМ №2008614242, 05.09.2008]. В табл.2 представлены результаты расчета активационных параметров.
Значение энергии активации процесса десорбции в температурном интервале 25-225°С составляет около 30,8 кДж/моль (0,31 эВ), а в температурном интервале 200-430°С - около 44,7 кДж/моль (0,45 эВ). Таким образом, с учетом погрешности определения энергии активации десорбции, предполагают Ван-дерваальсовский характер взаимодействия адсорбированных молекулярных комплексов с ядром наночастицы.
Значения предэкспоненциального множителя велики, согласно современным представлениям величина этого параметра характеризует масштаб элементарного термоактивируемого события. Приведенные в табл.2 значения свидетельствуют о крупномасштабных элементарных событиях десорбции. Такой характер десорбции свидетельствует о взаимодействии элементов примесной подсистемы не только с наноалмазным ядром, но и друг с другом. Таким образом, десорбция представляет собой последовательный температурно-зависимый процесс выделения молекулярных кластеров.
Проведенный анализ процессов десорбции примесей, адсорбированных наноалмазным ядром, свидетельствуют о сложном элементном составе поверхностного слоя наночастицы. Характерно, что часть молекулярных структур слабо связаны с ядром. Ван-дер-ваалсовский характер взаимодействия свидетельствует, что на поверхности наночастицы алмаза располагается подстилающий слой сильно связанных с ядром примесей, экранирующих незамкнутые ковалентные связи на поверхности наночастицы. В практических приложениях учет этих особенностей десорбции примесей обязателен.
Пример 3
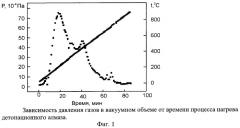
В связи с выделением большого объема летучих примесей, как показано в примере 2, проводят дифференциальный термический анализ и масс-спектрометрический анализ наноалмазных образцов и металлоалмазной шихты с помощью синхронного прибора термического анализа Luxx 409, совмещенного с масс-спектрометром Aelos 403. Термическое воздействие осуществляют путем нагрева образца в атмосфере аргона со скоростью около 10 К/минуту. На фиг.2 представлены зависимости изменения массы образца и теплосодержания от температуры нагрева наноалмазного образца исходной массы 7,1 мг. Как следует из приведенных на фиг.2 данных, при нагреве образца наблюдается значительное (величиной до 20%) монотонное уменьшение массы. Монотонное уменьшение массы с момента начала нагрева сопровождается заметным эндотермическим эффектом в интервале температур 40-200°С с максимальным значением около 0,3 мВт/мг при температуре 87°С, а в интервале температур 530-700°С наблюдается экзотермический эффект с максимумом при 675°С и величиной около 0,52 мВт/мг. При нагреве выше 700°С и вплоть до 900°С наблюдаются локальные экзоэффекты, свидетельствующие о дальнейшей эволюции примесной подсистемы.
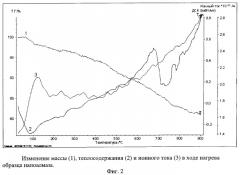
Такой эволюции примесной подсистемы наноалмаза соответствует широкий спектр масс десорбированных летучих веществ, отображенный на фиг.2, как зависимость ионного тока (3) от температуры. На фиг.2 приведен фрагмент ионного тока для отношения m/Z=17 (m - масса молекулярного иона, Z - электрический заряд) с максимумом около 100°С, другим отношениям m/Z соответствуют другие зависимости ионного тока от температуры. В табл.3 приведены обобщенные результаты анализа всех масс-спектрометрических данных десорбированных молекулярных комплексов.
Как следует из данных табл.3, (в табл.3 кроме масс-спетрометрических данных m/z, приведены температурные интервалы, в которых локализованы процессы десорбции, и положение максимума десорбции соответствующего молекулярного комплекса), процесс десорбции летучих соединений захватывает широкий температурный интервал 30-950°С. Выделяют несколько температурных интервалов, в которых наиболее активно идет процесс десорбции: низкотемпературный интервал 40-200°С; среднетемпературные интервалы 180-320 и 530-780°С, высокотемпературные интервалы 680-900 и 690-820°С, соответственно. Характерно, то что этим температурным интервалам соответствуют эндо- и экзотермические эффекты, сопровождающие нагрев образцов.
Отношение m/z=2 с максимумом в температурном интервале 680-900°С относится к водороду. Отношение m/z=16 в температурном интервале 180-320°С частично относится к воде, а в температурном интервале 530-780°С - скорее относится к углеводородам, например, CH4, но может быть и осколком углеводородной цепи. Отношения m/z=17 и 18 в температурном интервале 40-200°С относятся к десорбции воды, они всегда дублируют друг друга. Отношение m/z=28 в интервале 690-820°С с максимумом при 760°С соответствуют десорбции молекулярного азота N2, но это могут быть и молекулы СО, что совпадает с выводами работы Отношение m/z=44 в температурном интервале 500-820°С и максимумом при 680°С вероятнее всего относится к десорбции углекислого газа СO2. Тем более этот интервал совпадает с температурным интервалом экзотермического эффекта на фиг.2, что может соответствовать взаимодействию адсорбированного кислорода с углеродом неалмазной фракции с образование прочной молекулы CO2 Отношение m/z=64 в температурном интервале 200-580°С соответствует молекулам диоксида серы SO2 в нашем случае это наиболее вероятное соединение, так как в процессе очистки детонационного алмаза используется серная кислота, а кислород является одной из основных примесей детонационного наноалмаза.
Таким образом, нагревают наноалмаз до 200°С и освобождают его от воды, нагревают до 320°С, то наряду с водой происходит десорбция углеводородных молекулярных комплексов с m/z=16, а нагрев до 580°С приводит к десорбции диоксида серы с m/z=64, нагрев и выдержка в интервале температур 500-820°С с максимумом при 680°С, приводит к десорбции углекислого газа с m/z=44 и кислорода, который улетучивается, соединяясь с углеродом, нагрев и выдержка при 760°С, кроме того, приводит к десорбции молекулярного азота с m/z=28. Для десорбции молекулярного водорода с m/z=2 требуется нагрев до 860°С.
Пример 4
Для выяснения адсорбционной способности предварительно отожженного детонационного наноалмаза проводят дифференциальный термический анализ и синхронно масс-спектрометрию адсорбированных веществ. Для этого подготовленные образцы отжигают при температуре 950°С в вакууме. Затем образцы охлаждают и помещают в нормальные условия (давление атмосферы примерно 760 мм рт.ст., а температура 25°С). Как и в примере 3, для проведения термического и масс-спектрометрического анализа используют комплексную установку, включающую прибор термического анализа Luxx 409, совмещенного с масс-спектрометром Aelos 403.
На фиг.3 приведены данные по изменению массы, теплосодержания и фрагмента ионного тока для отношения m/z=17. Как следует, из представленных данных, (как и в примере 3) в ходе нагрева до 900°С наблюдается монотонное уменьшение массы образца величиной 8,3%, сопровождаемое двумя эндотермическими эффектами. Низкотемпературный интервал 40-200°С имеет максимум при 107,6°С, в высокотемпературном интервале 710-900°С можно выделить две области теплопоглощения - одна расположена при температуре 726,3°С, другая - при температуре 802,3°С. Все это свидетельствует о том, что после первого отжига детонационный наноалмаз активно адсорбирует, очевидно, газообразные составляющие атмосферы.
Рассмотрим масс-спектрометрические данные процесса десорбции вторично адсорбированных веществ (табл.4). Из данных, приведенных в табл.4, следует, что детонационный наноалмаз вновь адсорбирует тот же самый набор молекулярных комплексов, как в примере 3 (за исключением диоксида серы SO2). Из приведенных в примере 4 данных следует, что при использовании детонационного наноалмаза для практических целей необходимо учитывать вторичную десорбцию примесей и производить манипуляции по изменению примесной подсистемы необходимо одновременно с процессом десорбции примесей.
Пример 5
С учетом предыдущих выводов проводят анализ десорбции примесей из шихты, состоящей из детонационного наноалмаза и 30 мас.% алюминия. Шихту готовят путем тщательного перемешивания исходного порошка наноалмаза и порошка алюминия ПАП-1. После 10 часового перемешивания прессуют образцы как в примерах 3 и 4. Термический анализ и масс-спектрометрия показывает (фиг.4, табл.5), что при нагреве шихты до 900°С убыль массы немонотонна. В температурном интервале 40-200°С убыль массы составляет не более 2,0 мас.%. На зависимости теплосодержания от температуры этой убыли массы соответствует заметный эндотермический эффект, а на зависимости ионного тока от температуры наблюдается высокий максимум ионного тока с отношением m/Z=18, соответствующей десорбции воды. Однако в температурном интервале 170-250°С наблюдается почти полное восстановление массы, величина возврата массы составляет 1,83 мас.%. Смена десорбции на адсорбцию, очевидно, связана с обратным поглощением либо воды, либо атомарного водорода, для которого ионный ток лежит в температурном интервале 40-620°С с максимумом при 140°С.
В температурном интервале 250-430°С наблюдается заметная убыль массы величиной примерно 8,0 мас.%, которая затем в интервале 430-510°С сменяется приростом массы величиной 4,82 мас.%. Далее до 800°С наблюдается монотонная убыль массы величиной 1,3 мас.%, которая в узком интервале 800-820°С сменяется ее скачкообразным падением величиной около 4,0 мас.%.
Острый эндотермический эффект (фиг.4) теплосодержания при 665°С обусловлен плавлением алюминия, последующий экзотермический эффект в температурном интервале 670-770°С и максимум при 735°С, очевидно, связан с взаимодействием расплавленного алюминия с элементами примесной подсистемы наноалмаза в первую очередь с кислородом с образованием нелетучих соединений (например, Аl2О3), так как убыль массы составляет всего десятые доли процента. Экзотермический максимум при температуре 850°С сопоставим с небольшим (около 2 мас.%) приростом массы, что связано со взаимодействием поверхностных примесей с молекулярными комплексами летучих соединений, десорбированных при низких температурах.
Таким образом, введение в состав шихты алюминия существенно сказывается на процессах десорбции, появлению скачков убыли и прироста массы в ходе нагрева до 900°С, появлению экзотермических максимумов, обусловленных взаимодействием алюминия с примесной подсистемой. Очевидно, часть алюминия вступает во взаимодействие и с другими, более сильно связанными с алмазным ядром примесями, освобождая тем самым алмазное ядро от примесных атомов.
Пример 6
Для проверки выводов, полученных в примере 3, 4 и 5, готовят смесь, состоящую из порошка детонационного алмаза и алюминия, взятого в соотношении 5, 10, 20, 30, 40, 50, 70 мас.% алюминия и соответственно 95, 90, 80, 70, 60, 50, 30 мас.% детонационный наноалмаз. Смесь перемешивают, формируют и прессуют образцы, а затем проводят отжиг в течение 30 минут в вакууме при температуре 900°С. Структура полученных композитов приведена на фиг.5.
Структура композита представляет собой многофазную металлоалмазную смесь, состоящую из конгломератов детонационного наноалмаза, металлической составляющей и оксида алюминия. Причем при увеличении концентрации алюминия в ходе спекания наблюдают диспергирование исходных конгломератов наноалмаза и более равномерное распределение его в структуре композита.
Рентгенограмма исходного наноалмаза приведена на фиг.6. Хорошо идентифицируются рефлексы наноалмаза (111), (220) и (311). Кроме того, как видно из рентгенограммы, наблюдается значительный фон практически во всем диапазоне углов Θ съемки. По характеру изменения интенсивности фона считают, что данное диффузное рассеяние относится к малоугловому рассеянию, возникающему при наличии конгломерата частиц малого размера. Малоугловое рассеяние убывает по экспоненциальному закону в зависимости от угла дифракции. Это свидетельствует о том, что одной из компонент детонационного наноалмаза являются адсорбированные на поверхности кристалликов алмаза молекулярные кластеры различного состава. Их размеры и структура имеют самый разнообразный характер, что дает непрерывное малоугловое рассеяние.
После отжига при 900°С металлоалмазного композита состава наноалмаз-10 мас.% алюминия рентгеноструктурный анализ (фиг.7) свидетельствует, что наноалмаз композита претерпевает существенные изменения. На рентгенограмме практически отсутствует диффузный фон. Исчезновение диффузного рассеяния на углах более 20° свидетельствует, что в результате реакции с алюминием атомные кластеры и молекулярные комплексы примесей были разрушены и их атомы оказались включены в решетку алюминия или десорбированы.
Кроме того, наряду с рефлексами алмаза наблюдают рефлексы других фаз. Наличие других фаз свидетельствует, что алюминий композита активно взаимодействует с адсорбированными на поверхности наночастиц атомами примеси. В табл.5 приведены результаты расшифровки рентгенограмм металлоалмазного композита после высокотемпературного отжига.
Данные, приведенные в табл.5, свидетельствуют о том, что металлоалмазный композит после высокотемпературного отжига в вакууме не содержит чистый алюминий, а содержит оксиды алюминия, общая концентрация которых составляет 8,23 мас.%. Структурное состояние продуктов взаимодействия алюминия с кислородом представляет собой наноразмерный конгломерат частиц. То есть алюминий активно взаимодействует с кислородом, адсорбированным частицами детонационного наноалмаза. Оставшаяся доля алюминия, входит в состав соединений с другими (кроме кислорода) атомами примеси. Структурные составляющие композита детонационный алмаз и частицы оксида алюминия и других соединений имеют наноразмерный масштаб, а параметр Δd/d свидетельствует о сильном искажении межплоскостных расстояний кристаллических решеток. Искажение межплоскостных расстояний есть следствие малых размеров кристаллитов структурных составляющих композита.
Анализ микротвердости (фиг.8) показывает, что прочность металлоалмазного композита зависит от концентрации алюминия как функция с максимумом, приходящимся на концентрацию алюминия 10-30 мас.%. Такая зависимость свидетельствует о рекристаллизации наночастиц детонационного наноалмаза в условиях взаимодействия алюминия с примесной подсистемой, взаимодействием наночастиц алмаза по фрагментам границ раздела, свободных от примесей, с образованием ковалентных связей, формированием поликристаллического наноразмерного агрегата.
Таким образом, процессы десорбции примесей, глубокой очистки поверхности наноалмазных частиц и формирование металлоалмазного композита происходят одновременно в динамическом режиме путем нагрева образца до температуры 900-950°С, в течение 30 минут.
Выводы: Алмазосодержащий материал, полученный способом селективной очистки детонационного наноалмаза, обладает свойством вторичной адсорбции, что позволяет избирательно поглощать и модифицировать поверхности частиц наноалмаза различными веществами, например, органическими полимерами. Процесс глубокой очистки поверхности детонационного наноалмаза позволяет получить в динамическом режиме новые композиционные алмазосодержащие материалы.
| Таблица 1 | ||||
| Элементный состав детонационного наноалмаза. | ||||
| Элемент | Исходный наноалмаз | Отожженный наноалмаз | ||
| Содержание, Wt % | Содержание, At % | Содержание, Wt % | Содержание, At % | |
| С | 82,28 | 91,46 | 76,80 | 87,01 |
| O | 4,93 | 4,12 | 9,66 | 8,23 |
| Аl | 1,27 | 0,62 | 1,86 | 0,94 |
| Si | 0,40 | 0,19 | 1,18 | 0,58 |
| S | 4,33 | 1,79 | 2,52 | 1,10 |
| Са | 1,92 | 0,64 | 2,58 | 0,88 |
| Fe | 4,52 | 1,08 | 4,64 | 1,13 |
| Сu | 0,61 | 0,13 | 0,70 | 0,15 |
| Сr | 0,56 | 0,15 | - | - |
| Таблица 2 | |||
| Температурный интервал, °С | Энергия активации, кДж/моль | Предэкспоненциальный множитель | Коэффициент корреляции |
| 25-225 | 30,8±4,0 | 6,5±4,4 | 0,973 |
| 250-430 | 44,7±14,6 | 2,5±2,3 | 0,941 |
| Энергия активации процесса десорбции. |
| Таблица 5 | |||
| Металлоалмазный композит | Содержание компонент, мас.% | Δd/d 103 | Размер кристаллитов, нм |
| Алмазная компонента | 91,77 | 5,1 | 7,4 |
| Оксид алюминия (theta) | 6,64 | 2,8 | 18 |
| Оксид алюминия (corund) | 1,59 | 1,7 | 14,5 |
| Параметры металлоалмазного композита после высокотемпературного отжига. |
Способ селективной очистки детонационного наноалмаза, включающий в себя термодесорбцию наноалмаза в вакууме, отличающийся тем, что в исходный алмазосодержащий порошок добавляют порошковый алюминий в количестве не менее 5 мас.%, смесь перемешивают, прессуют и отжигают образец при температуре 900-950° в вакууме при остаточном давлении не хуже 10-3 мм рт.ст. в течение 30 мин.