Способ полярографического определения никеля
Иллюстрации
Показать всеРеферат
СООЗ СОВЕТСКИХ
NOMIC
РЕСПУБЛИК
09 (И) Зав "1 И 27/48
ГОсудАРОТВВжый КОмитет сссР
re делАм иэоВРетений и отнрыт1й
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
{21} 3326527/18-26
{22) 30.07.81 (46) 07 08.83. Б л. И 29 (72) Е,A.Иамбетказиев, С.И.Жданов, В.Н.Стацюк и С.В.Неталиева (71) Казахский ордена Трудового
Красного Знамени государственный университет им. С.M.Êèðîâà (53) 543 253(088.8) (56) 1. Крюкова Т.А., Синякова С,И., . АреФьева T.Â. Полярографический анализ, й., 1959, с. 363.
2, J.E1ectroanalyt. Chem, 1977
V. 79, И 2, р. 365-374. (54)(57) СПОСОБ ПОЛЯРОГРАФИЧЕСКОГО
ОПРЕДЕЛЕНИЯ НИКЕЛЯ в присутствии
Фонового электролита и комплексообразователя 2,2 -дипиридила,. о тл и ч а ю шийся тем, что, с целью повышения чувствительности и селективности анализа, в качестве Фо нового электролита используют раствор фторида натрия, 1033942
15 !
1
Изобретение относится к области аналитической химии, а именно к способам полярографического определения йикеля.
Известен способ полярографическо" го определения никеля в -присутствии фонового электролита - смеси хлорида пиридиния и хлорида аммония с предварительным кислотным разложением пробы 1).
Однако известный способ характеризуется невысокой чувствительностью и сепективностью определения, Кроме того, используется ядовитый пиридин„
Наиболее близким к предлагаемому является способ полярографического определения никеля в растворах в присутствии фонового электролита;раствора нитрида.калия - и комплексообраэователя 2,2 -дяпиридила j2 3.
Однако известный способ характери эуется низкой чувствительностью (10 моль/л)из-эа наличия, на фоне нитрида калия адсорбционных явлений, Кроме того, мешает определению желе" зо.
Цель изобретения - повышение чувствительности и селективности анализа.
Поставленная цель достигается согласно способу полярографического определения никеля в присутствии фонового электролита - раствора фторида натрия » и комплексообраэоватепя 2,2 -дипиридила, при котором в качестве фонового электролита использу» ют раствор фторида натрия.
При использовании в качестве фо" нового электролита фторида натрия не наблюдается адсорбции комплексов никеля (в отличие от ниФратных, перхлоратных и др. фоновых растворов J, Кроме того, основную массу железа, присутствующего в никельсодержа" щих продуктах, отделяют с помощью NaF в виде осадка состава 5NaF 2ГеГ некоторое количество железа остается в растворе в виде комплекса
FeF и не мешает определению никеля.
Э фторидные, комплексы железа,(9) более устойчивы по сравнению с дипиридильными комплексами железа (Й ), поэтому в объеме раствора будут превалировать фторидные комплексы же.леза, которые не восстанавливаются на ртутном электроде в рассматриваемом интервале потенциалов. В случае, когда никель находится в силикатной форме, разрушение силикатного ядра при разложении пробы ведут смесью фторида аммония с концентрированной соляной кислотой, Волна восстановления никеля на фторидном фоне (0,1 моль/л водный раствор фторида натрия) отсутствует изза необратимости разряда экваионов
Ni(Н О) . В присутствии 2,2 -дипи" ридила йа переменнотоковых полярограммах появляется четко выраженный, хорошо воспроизводимый пик при потенциале - 0,85 В (относительно насыщ. к.э.), обусловленный восстановлением на ртутном электроде монодипиридильного комплекса никеля. Высота этого пика находится в линейной зависимости от концентрации никеля, что дает возможность определять никель полярографическим методом.
Предлагаемый способ позволяет определять никель не только на чис" тых растворов, а также непосредственно из никельсодержащих проб с
25 предварительным их разложением, В никельсодержащих продуктах, как правило, никелю сопутствует ко" балы, причем содержание никеля более чем в 100 раэ превышает содержа" ние кобальта, Потенциал пика алек" тровосстановления кобальта из фто" ридно-дипиридильных растворов равен1,28 В (насыщ, к.э.) ° Присутствие стократного избытка кобальта не мешает определению никеля.
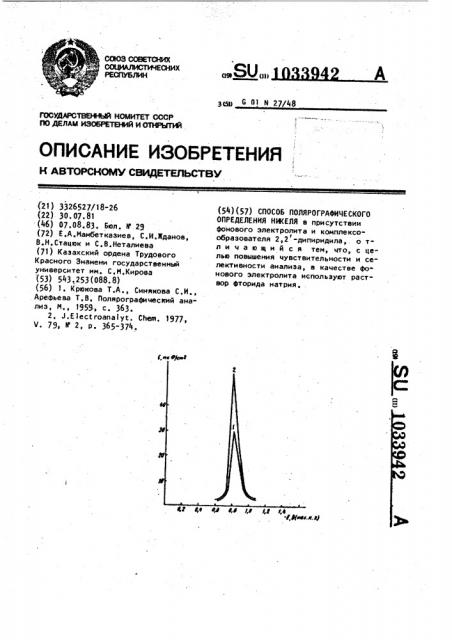
На чертеже представлены переменнотоковые полярограммы растворов, содержащих только никель (т.е.. в отстутствие мешающих элементов) на фоне нитрата калия (кривая 1) и фторида натрия (кривая 2).
Применение в качестве фонового электролита раствора фторида натрия позволяет увеличить чувствительность определения на два порядка.
Пример, Для разложения никельсодержащих продуктов навеску пробы 0,5 г.смешивают с 0,2 г фтори да аммония . Приливает 20 мл концентрированной соляной кислоты, нагревают раствор и выпаривают до влаж. ных солей. К оставшемуся раствору добавляют 10 мл концентрированной азотной кислоты и выпаривают до влажных солей. Приливают 5 мл концентрированной соляной кислоты и выпаривают досуха, Затем повторяют выпаривание с соляной кислотой два раза:,(по 5 мл), тобы удалить окиСоставитель Т.Жукова
Редактор Е.Папп .Техред Ж.Кастелевич
Корректор-Г.Решетник
«
Заказ 5615/47 Тираж 873 Подписное
ВНИИПИ -Государственного комитета СССР по делам изобретений и открытий
113035, .Москва, Ж-35, .Раушская наб., д, 4/5 филиал ППП "Патент", г. Ужгород, ул. Проектная, 4
3 10339 слы азота. К сухому остатку приливают 15 мл разбавленной соляной кислоты (1:3) и нагревают до растворения хлоридов. В охлажденный рествор добавляют по каплям 20 -ный раствор гидроокиси натрия до рН 1,5
{по индикаторной бумаге "РИФАН"}.
Небольшими порциями при перемеши:вании вводят 0,5 r Фторида натрия
{для отделения осноВной-массы желе- 16 аа ;. Раствор с осадком переносят в мерную колбу емкостью 100 мл, доводят дистиллированной водой до метки, перемешивают и через 15 мин отфильтровывают через фильтр "си" няя лента" аликвотный объем филь" тра (10 мл) в мерную колбу емкостью 50 мл и доводят до метки фоновым раствором, содержащим 2,2 -дипиридил (1 .10 " ь/л НаГ+1.1О ль/л
2,2 -дипиридила).. Анализируемый, раствор переносят в полярографическую ячейку, регистрируют переменно; токовые полярограммы (полярограф
ШПТ-1 без продувки инертным газом 2
42
4 в интервале потенциалов от -0,5 до
-1,0 В (насыщ,к.э.) при скорости изменения 2 M8/c. Измеряют максимальный ток электровосстановления монодипиридильного комплекса никеля при Е 0-0,85 В (насыщ.к.э.) . Концентрацию ионов никеля (A ) находят по калибровочному графику, .полученному с помощью стандартных раство" ров, содержащих фон; в интервале концентраций никеля 1 10 ° 104оль/л. .Содержание никеля (Х) вычисляют. по формуле, Ф:
ex 3 МОО
Н
«ф ° айь. где С„- количество никеля по калибровочному графику, моль/л;
Э - эквивалент никеля;
Н - нввеска.
Таким образом, предлагаемый способ позволяет повысить чувствитель" ность определения никеля на два порядка и увеличить селективность определения в присутствии железа.