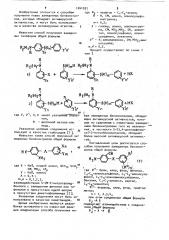
Способ получения замещенных бензонитрилов
Иллюстрации
Показать всеРеферат
СОЮЗ СОВЕТСНИХ йОИй
РЕСПУБЛИК
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
1
Ф .., 1
1
К ПАТЕНТ,Ф
_#_ — ® 4
/ В а) « = < l (6) ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 3245544/23-04 . (22) 16.02.81 (46) О7.09.83. Бюл..lt 33 (72) Лоуэлл Дин Маркли (СШИ) (7.1) .Дзе Дау Кемикал Компани (СИА) (53) 547.239.07(088.8) (56) l. Патент СНА И 4164412, кл. 71-103, опублик. 1979.
2. Патейт СНА М 3766238, кл. 260-465, опублик. 1973. (54)(57). СПОСОБ ПОПУЧЕНИЯ ЗИМЕЩЕННИХ
БЕНЗОНИТРИЛОВ общей формулы T где R — бром, хлор, фтор, фенокси, С„-С -алкилсульфинил; С„-С -:
-алкилсульфонил, С„-С -алкиламиносульфонил, бейзоил, "
С„-С -алкокси, ацетил, С -С ",. алкилтио;
„SU „„1041031 А
31Я1 С 07 С. 120/00; С 07 С 121/75;
А 61 К 31/2751 С.07 Ci 149/415.
R< - водород, хлор, фтор, трифторметил; и — 1-4, отличающийся тем, что . соединение общей формулы I1, В2 — А, подвергают взаимодействию с соединением общей формулы И1 в =х=v, 1
t де. А — галоген;
Х - кислород или сера;
У вЂ” водород, натрий или калий;
 — одна из групп при этом если В - группа (а), то
В - группа (б) и наоборот, R ", К и и имеют указанные значения, s среде инертного органического растворителя при 60-100 С в присутствии щелочного агента.
, фиа
© 4Ф
Май
1041031 1 где Р - перфтор - С<-c>- алкил;
R — Н, CN, алкил, алкилсульфонилгруппа;
rn 0,Z;
У - галоид, алкил, алкоксигруппа, CN, Й02,МН2» ОН, алкилтио, алкилсульфонил, алкилсульфинил, алканоил;
У1 - Р; алкилалкокси, СМ, М 02,ами1О . ногруппа;
n,h = 0,2.
Процесс осуществляют по схеме 1 или 2
Изобретение относится к способам получения новых замещенных бензонитрилов, которые обладают антивирусной активностью, и могут быть использованы в,качестве антивирусных агентов.
Известен способ получения замещенных тиоэфиров общей Формулы ф +OX
Т 11
К
I в о;я л) 1
Му30, >
8(о}„И+
11
Уп
8(o) „— i +их
31 в уи где У, У", Х, h имеют указанные значе- ния, И - щелочной металл или медь.
Указанные целевые соединения используют в качестве гербицидов (1 ).
Известен также способ получения за" мещенных бензонитрилов общей формулы где Х - На, низший алкил, ОСН, SCH>, 45
У .- Hag, алкил;
А=0,5; нп = 0,1,2,3, взаимодействием 4-CN-2-нитрогалоидбензола с замещенным фенолом или тифенолом.в присутствии едкой щелочи в присутствии диметилформамида (2 3.
Указанные соединения могут быть ис. пользованы в качестве нематоцидов.
Целью изобретения является разработка основанного на известной. реакции конденсации способа получения нов so,ò-Я-((o)© к Уп
l вых замещенных бензонитрилов, обладающих антивирусной активностью., которые по сравнению с известными замещенными бензонитрилами того же назначения, в частности 5-(3,4-дихлорфенокси )-2-нитробензонитрилом,. обладают более высокой антивирусной активностью.
Поставленная цель достигается способом получения замещенных бензонит" рилов общей Формулы и в ом Xx
2; (.Е ) ® )п.где Р - бром, хлор, фтор, Фенокси, С -С -.алкилсульфинил, С„-С -алкилсульфонил, С -С -алкиламиносульфонил, бензоил, С.(-С -алкокси, ацетил, C -C>-алкилтио;
R - водород, хлор, фтор, трифторметил; n = 1, 2,3,4, при этом соединение общей Формулы
В -АЙ подвергают взаимодействию с соедине-. нием общей формулы
8 =X-У ф.
1041031 где А Х
Ув
О яК
3 галоген; кислород или сера; водород или натрий или калий; одна из групп. при этом если В - группа (а ), то
В - группа б и наоборот, й", й2и ;
1 и имеют указанные значения, в среде инертного органического растворителя при 60-100ОС в присутствии щелочного агента.
Выход замеценных бензонитрилов со->5 ставляет 35-993 при продолжительнос" ти реакции до 10 ч.
Полученные соединения являются криоталлическими веществами, которые до", статочно хорошо растворимы в органи», 20 ческих растворителях, таких как мети-, ленхлорид, метанол, этанол, но ограничено растворимы в воде..
В качестве инертного растворителя при получении замещенных бензонитри- 25 лов можно испольэовать такие соединения, как диметилсульфоксид, ацетонит.рил, а в качестве щелочного агента -. гидроокись натрия или карбонат калия.
Исходные реагенты, которые пред" почтительно используют в эквимолярных количествах, можно вводить в ре" акцию в любой последовательности.
Пример 1. 2-(3,4-Дихлорфен". окси)-5-нитробензонитрил, .К раствору, 91,3 г (0,56 моль) 3 4дихлорфенола в 500 мл диметилсульфок-. сида (ДМСО) добавляют 22,4 г (0,56 моль) гидроокиси натрия(t4aOH )".
Полученную. взвесь нагревают при 60©С в течение 15 мин, после чего добавля", 40 ют 100 г (0,55 моль) 2-хлор-5-нитро " бензонитрила. Смесь нагревают при
75 С в течение 3 ч. Реакционную смесь о охлаждают и выливают во взвесь 200 мл
2 н. ЙаОН и 1800 мл льда и воды, в ре.
--: 45 зультате чего продукт выпадает в оса-. док. Полученный продукт отфильтровыв " ют, промывают водой и высушивают, в результате чего получают 163,3. r npd. дукта (выход 96,4/), т.пл. 154-155 СПосле перекристаллизации иэ 3-метокси-2-пропанола, получают 2"(3,4.-ди" хлорфенокси)-5-нитробензонитрил с т.пл. 155-156 С. В ИК-спектре 2-, " (3,4-дихлорфенокси)-5-нитробенэонит- М рила следующие полосы: ИК в нуйоЫ1
2250, 1620, 1580, 1520,. 146 .>, 1360, 1270, 1130, 1040 и 895 см ", 4
Пример 2. 2- (2,4-Дихлорфенок" си )-5"нитробензонитрил.
К раствору 5,0 г (0,0307 womb)
2,4-дихлорфенола в 150 мл ДМСО добав" ляют 1,23 г (0,0307 моль) (4аОН. Полученную взвесь нагревают при 60 С в течение 15 мин; после чего добавляют
5,04 г (0,0276 моль) 2-хлор-5-нитробензонитрила. Смесь нагревают при о
75 С в течение 3,25 ч. Реакционную смесь охлаждают и выливают в воду.
Полученный продукт отфильтровывают, хорошо промывают водой и высушивают, в результате чего получают 8,1 r продукта (выход 95,33). После верекрис.таллиэации из этанола получают 2-(2,4-дихлорфенокси)-5-нитробензо.нитрил с т.пл. 153,5-154 5 С
Пример 3 ° 2-(4-Бромфенокси)-5-нитробензонитрил.
К раствору 5,31 r (0,0307 моль)
4-бромфенола, растворенного в 150 мл в ДМСО, добавляют 1,23 г (0-,0307 моль)
Na0H, Полученную взвесь нагревают при а
60 С в течение 15 мин и добавляют
5,04 г (0,0276 моль) 2-хлор-5-нитробензонитрила. Полученную смесь нагревают при 75 С,в течение 4 ч. Реакционную смесь охлаждают и выливают в во" ду. Выпавший продукт отфильтровывают, промывают водой и высушивают, в ре-. зультате чего получают 8,1 г неочищен" ного продукта. Данный продукт растворяют в СН2С72 и промывают 104-ным вод" ным раствором йаОН, водой, после чего высушивают Йа29), . После удаления растворителя в вакууме получают 7,5 г (выход 853 ) продукта. После перекристаллизации из этанола получают
2-(4-бромфенокси)-5-нитробенэонитрил с т.пл. 171-172ОС.
Пример 4. 2-(4-Хлорфенокси )-5-нитробензонитрил.
К раствору 3,95 г (0,0307 моль).
4-хлорфенола в 150 мл ДМСО добавляют
1,23 г (0,0307 моль) МаОН. Полученную взвесь нагревают при 60 С в течение
15 мин, после чего добавляют 5,04 г
70,0276 моль ) 2-хлор-5-нитробензонит" рила и полученную смесь нагревают при
75 С в течение 3 ч. Затем реакционную смесь охлаждают и выливают в во" ,ду. Выпавший целевой продукт собира,ют, отфильтровывают, хорошо промывают водой и высушивают,. в результате чего получают 7,0-r продукта (выход
923). В результате перекристаллизации из этанола получают очищенный 2-(43 10410
-хлорфенокси )-5-нитробензонитрил, т.пл. 163-1640С.
Пример 5. 2-(4-феноксифен. .окси)"5"нитробензонитрил.
К раствору 5,71 r (0,0307 моль) 5
4-феноксифенола в 150 мл: ДМСО добавляют 1,23 r (0,03070 моль)йаОН. Полученную взвесь нагревают при, 75 C в течение 15 мин, после чего добав" ляют 5,04 г (0,0276 моль ) 2-хлор-5-нитробензонитрила и полученную смеСь нагревают при 75ОС в течение 4 ч. 3атем реакционную смесь охлаждают и вы:ливают в воду. Целевой продукт отФильтровывают, хорошо .промывают во- IS дой и высушивают. Данный продукт раст" воряют в СН СФ2 и промывают 103-ным . водным раствором NaOH и высушивают йа2SO+. После удаления растворителя в вакууме получают 8,0 r .(выход 873) 20 целевого продукта. После перекристаллизации из этанола получают 2-(4-феноксифенокси )-5"нитробензонитрил с т.пп. 150-151 С.
П р,и м е р 6. 2-(4-(Метилтио) 25 фенокси)-5-íèòðîáåíçîíèòðèë.
К раствору 11,55 г (0,0824 моль)
4-(метилтио)-Фенола в 150 мл ДМСО добавляют 3,3 r (0,0824 моль) NaOH. Cloлученную взвесь нагревают до 60 С, З0 после чего добавляют 13,7 г (0,0730 моль) 2-хлор-5-нитробензонит- . рила и полученную смесь нагревают при
75 С в течение 2,5 ч. Полученную смесь охлаждают и выливают е ðàñòâoð 200 мл
5.н., водного раствора NaOH и 500 мл во ды. Целевой продукт. отфильтровывают, хорошо промывают водой и высушивают, в результате чего получают 20,3 r продукта (выход 94,6i). После пере- 4 кристаллизации из метанола получают очищенный 2-1 4-(метилтио)фенокси ).о
-5-нитробензонитрил с т.пл. 124-126 .C °
Пример 7. М,N-Диметил-4-(2-циано"4-нитрофенокси)-бензолсульфон45. амид.
К раствору 6,37 г (0,0317 моль )
М,й-диметил-4-оксибензолсульфонамида в 150 мл ДМСО добавляют 1,27 г (0,0317 моль) йаОН. Полученную смесь .нагревают go 60oC, после чего добавля50 ют 5,26 r (0,0288 моль ) 2-хлор-5-нитробенэонитрила и полученную смесь нагревают при 75 С в течение 2,5 ч.
Затем реакционную смесь охлаждают и выливают в раствор 400 мл водной NaOH 55 и 300 мл воды. Полученнйй целевой продукт отфильтровывают, хорошо промыва- ют водой и высушивают, в резульгате
31 б чего получают 8,8 г продукта (выход
88 ). В результате перекристаллизации из смеси этанола и диметилформамида получают очищенный Й,N-.диметил-4-(2-циано-4 -, нитрофенокси)" бензолсульфонамид с т.пл. 221,5-223ОС.
Пример 8. N,N-Диэтил-4, (2"циано-4-нитрофенокси)-бензолсульфонамид.
К раствору 6,73 r (0,0294 моль)
NPl-диэтил-4-оксибензолсульфонамида в 150 мл ДМСО добавляют 1,18 г (0,0294 моль ) ИаОН. Полученную смесь нагревают до 60 С, а затем добавляют
4,88 r (0,0267 моль ) 2-хлор-5-нитробензонитрила и полученную смесь нагревают при 75 С в течение 3 ч. Затем в реакционную смесь охлаждают и выливают в раствор 400. мл 2 н.водного раствора NaOH и 300 мл воды. Полученный продукт собирают, отфильтровывают, хорошо промывают водой и высуши-. вают, в результате чего получают.
8,8 г целевого продукта (выход 88 ).
В результате перекристаллизации из этанола получают очищенный Н,N- äèэтил"4.-(2-циано-4-нитрофенокси)-бензолсульфонамид с т.пл. 163-164 С.
Пример 9. 2.-(4-Бенэоилфенокси )-5-нитробензонитрил, К раствору 11,4 г (0,0575 моль)
4-оксибензофенола в 150 мл ДМСО добавляют 2,3 r (0,0575 моль) NaOH.
Полученную смесь нагревают до 60 С и к смеси добавляют 10,0 r (0,0548 моль) 2-хлор-5-нитробензонитрила, после чего ее нагревают при
75ОС в течение 3 ч. Затем реакционную смесь охлаждают и выпивают в раствор 100 мл 2 н. водной NaOH u
700 мл воды. Выпавший целевой продукт отфильтровывают, хорошо промывают водой и высушивают, в результате чего получают 17,75 r целевого продукта (выход 89,á3). В результате перекристаллизации из смеси этанола и диметилформамида и второй перекристаллиэации иэ хлороФорма получают очищенный 2-(4-бенэоилфенокси )-5-нитробензонитрил с т.па. 179,5-180,5 С.
Пример 10. 2- ((4-Хлорфенил )-, тио|" 5-нит робен зонитрил .
К раствору 15,2 г (0,105 моль)
4-хлортиофенола в 150 мл ДМСО добавляют 4,2 г (0,105 моль) NaOH. Полученную смесь нагревают до 60 С, добавляют 18,3 г (0,100 моль) 2-хлор-5-нитробейзонитрила и полученную смесь нагревают при 60 С в течение 2,5 ч.
7 1041
Затем смесь охлаждают и выливают в: раствор 100 мл 1 н. водного МаОН и
600 мл воды. Целевой продукт отфильтровывают, хорошо промывают водой ивысушивают, в результате чего полу- чают 28,8 r продукта (выход 994).
В результате перекристаллизации иэ . этанола получают очищенный 2-((4-хлорфенил )тио -5-нитробензонитрил с т.пл. 162-164,5ОС.
Пример 11. 2-(3-Метоксифен" окси)-5-нитробензонитрил.
В 250 миллилитровую одногорлую колбу, снабженную магнитной мешал-. кой и обратным .холодильником и азот-. . 15 ным барботером, помещают 9,13 r (0,050 моль ) 2-хлор-5-нитробензонит:рила, 6,39 r (0,0515 моль) 3-метоксифенола 7,10 (0,0515 моль) безводного карбоната калия (К (;03 ) и 75 мл аце2 тонитрила. Полученную смесь нагрева-, ют до температуры кипения с обратным холодильником и выдерживают при этой температуре 3 ч, Затем реакционную смесь охлаждают до комнатной темпера-.25 туры и разбавляют 150 мл воды. Целевой продукт выпадает в осадок. Твердую часть отфильтровывают, тщательно промывают водой и высушивают воздухом.
Высушенный твердый продукт перекрис30 таллизовывают с использованием 200 мл абсолютного этанола, в результате чего получают 7,15 г (выход 53 )очищен- ного 2-(3-метоксифенокси )-5-нитробензонитрила с т.пл. 102-103,5 С.
Пример 12. 2- ((4-Трифторметил )фенокси)-5-нитроЬензонитрил.
В 250-,,миллилитровую одногорлую колбу, снабженную магнитной мешалкой и обратным холодильником с азотным 40 барботером, помещают 9,13 г . (0,050 моль.) 2-хлор-5-нитробензонитрила, 8,35 г (0,0515 моль ) 4-(трифторметил)фенола, 7,10 г (0,0515 моль) безводного К СО > и 75 мл ацетонитри; ла. Полученную смесь нагревают до температуры кипения с обратным холодильником и выдерживают при ней в течение
3 ч. Затем реакционную смесь охлаждают до комнатной температуры и раэбав- 50 ляют 150 мл воды. Целевой продукт выделяют в виде твердого вещества.
Его отфильтровывают, тщательно промы" вают водой и высушивают воздухом. Высушенное твердое вещество перекристал.55 лизовывают из 350 мл абсолютного эта- нола, в результате чего получают
12,35 г (выход 80< ) очищенного 2"
031 8.
-t(4-трифторметил )-фенокси)-5-нитробензонитрила с т.пл. 154-155,5ОС.
П р и и е р 13. 2-(4-Ацетилфенокси )-5-нитроЬензонитрил.
B 250-миллилитровую одногорлую кол" . бу, снаЬженную магнитной мешалкой и обратным холодильником с азотным бар" ботером, помещают 9, 13 r (0,05 моль )
2-хлор-5-нитробензонитрила, 7,01 г (0,0515 моль ) 4-оксиацетофенона, 7,10 г (0,0515 моль ) Ьезводного К СО> и 75 мл ацетонитрила. Полученную смесь нагревают до температуры кипения с обратным холодильником и выдерживают в течение 3 ч. Затем реакционную смесь охлаждают до комнатной температуры и разЬавляют I50 мл воды.
Продукт выделяют в виде твердого вещества. Твердую часть- отфильтровыва- . ют, тщательно промывают водой и высушивают воздухом. Высушенное твердое вещество дважды перекристаллизовывают из 300 мл абсолютного этанола, в результате чего получают 4,95 г (выход 35 ) очищенного 2-(4-ацетилфенокси -5-нитроЬензонитрила с т.пл.
135-136,5 С.
Пример 14. 2-(4-Хлор-2-метилфенокси )-5-нитробензонитрил.
В 250-миллилитровую одногорлую колбу, снаЬженную магнитной мешалкой и обра ным холодильником с азот" ным барботером, помещают 9,73 г (0,0533 моль ) ?-хлор-5-нитробензо-. нитрила, 7,83 г (0,0549 моль ) 4-хлор"
-Z-метилфенола, 7,56 г (0,0549 моль) безводного К2СО з и 75 мл ацетонитрила. Иолучейную смесь нагревают до температуры кипения с обратным холодильником и выдерживают при ней в течение 3 ч. Затем реакционную смесь охлаждают до комнатной температуры и разЬавляют 150 мл воды. Продукт выделяют в виде твердого вещества.
Твердую часть отфильтровывают, тща"
- тельно промывают водой и .высушивают воздухом. Высушенную воздухом твердую часть перекристаллизовывают из
400 мл аЬсолютного этанола и небольшого количества ацетона, в результате чего получают 9,60 г (выход 624) очищенного 2-(4"хлор-2-метилфенокси )-5-нитробензонитрила с т.пл. 144,5145,5 С.
П р и и е р 15. 2-(3,4,5-Трихлорфенокси )-5-нитробеязонитрил.
В 250-миллилитровую одногорлую коколбу, снабженную магнитной мешалкой и обратным холодильником с азот1041
9 ным барботером, помещают 8,68 г (0,0475 моль ) ?"хлор-5"нитробензонитрила, 9,67 г (0,0489 моль ) 3,4,5-три" хлорфенола, 6,/5 г (0,0489 моль) без- водного К С0> и 75 мл ацетонитрила.
Полученную смесь нагревают до .температуры кипения с обратным холодильником и выдерживают при ней в тече ние 3 ч. Затем .реакционную смесь охлаждают до комнатной температуры и 10 разбавляют 150 мл воды. Продукт вы деляют в виде твердого вещества..Твердую часть отфильтровывают, тщательно промывают водой и высушивают воздухом..
Высушенную воздухом твердую часть пе" 15 рекристаллизовывают из смеси 200 мл абсолютного этанола и 100 мл ацетона, в результате чего получают 11,62 г (выход 711 ) очищенного 2-(3,4,5-трихлорфенокси )-5-нитробензонитрила в . виде маленьких белых кристаллов с т.пл. 162-164 С.
Пример 16. 2-(2,3р5 6-Тетра"
Фторфенокси )-5-нитробензонитрил.
В 250"миллилитровую одногорлую кол бу, снабженную магнитной мешалкой и обратным холодильником с азотным барботером, помещают 9,13 r (0,050 моль ) 2-хлор-5-нитробензонит-I рила, 8,55 г (0,0515 моль) 2,3,5,6-(30 тетрафторфенола, 7,10 г (0,0515 моль/ безводного К2С03 и 75 мл ацетонитрила. Полученную смесь нагревают до температуры кипения с обратным холодильником и выдерживают, при ней в течение 3 ч. Затем реакционную смесь охлаждают до комнатной температуры и разбавляют 150 мл деиониэированной воды. Продукт выделяют в виде осадка.
Осадок отфильтровывают., тщательно промывают водой и высушивают возду»хом. Высушенную воздухом твердую часть перекриствллизовывают иэ 300 мл абсолютного этанола, в результате чего получают 11,36 г .(выход 73 ь ) очищенного 2-(2,3,5,6-тетрафторфенок- 45 си )-5-нитробензонитрила с т.пл. 152,5154,5.С °
ll р и м е р 17. 2-(2,3,4,5,6-Пен, тафторфенокси )-5-нитробензонитрил.
В 250"миллилитровую одногорлую, SG колбу, снабженную магнитной мешалкой и обратным холодильником с азотным, . барботером, помещают 9,59 г (0,0525 моль) 2-хлор"5"нитробензонит-. рила, 9,96 r (0,0541 моль) 2,3,4,5,6- Ы пентафторфенола, 7,56 г (0,0541-моль): безводного К СО и 75 мл ацетонитрила. Полученную смесь нагревают до.тем031 1О пературы кипения с обратным холодильником и выдерживают при ней в течение 3 ч. Затем реакционную смесь ох" лаждают до комнатной температуры и разбавляют 150 мл деиониэированной( воды. Продукт выделяют в виде кристаллического твердого вещества.; Твердую часть отфильтровывают, тщательно промывают водой и высушивают воздухом.
Высушенную воздухом твердую часть пе" рекристаллизовывают из 200 мл абсо лютного этанола,. в результате чего получают 9,91 .г (выход 573 )очищенного .2-(2,3,4,5,6-пентафторфенокси )-5-нитробенэонитрила с т.пл . 127,5 129 С.
Аналогично получены и другие 2" (замещенный - фенокси)-5-нитробензонитрилы по предлагаемому способу.
Пример 18. 2- ((3,4-ДихлорФенил)тио1-5-нитробенэонитрил, т.пл. 13/"139 С.
A р и м е р 19. 2-.(4-фтоошенокси)-5-нитробензонитрил, т.fill ° 132,5,133 5 С. .П р и м.е р 20. 2-(2,3-.Дихлорфенокси )-5-нитробензонитрил, т.пл. 146-147оС.
Пример 21. 2-(2,5-Дихлор
I фенокси )-5-нитробензонитрил, т.пл 167-168,5оС;
Пример,22. 2-(2,6-Дихлор" фенокси)-5-нитробензонитрил, т.пл.157159 C
Пример 23. 2-(3 5-ДихлорФенокси)-5-нитробензонитрил, т пл.-196-198 С.
Пример 24. 2"Д2-Трифторметил)фенокси)-5-нитробензонитрил, т.пл. 113-115îÑ
Пример 25.. 2-Ц 3-Трифторметил)фенокси .)-5-нитробензонитрил, т.пл. 85,5-86,5ОС.
П р и м .е р 26. 2- (3,5"бис -{Трфторметил.)фенокси)-5"нитробензонитрил, т.пл. 138-140 С;
Пример 27. 2-(2,3,4-Трияорфенокси )-5-нитробензонитрил, т.плЛ03204,5 C.
Пример 28. 2-(2,3,5-Трихлорфенокси )"5-нитробенэонитрил, т.пл. 160-162 С.
Пример 29. 2"(2,3,6"Трихлорфенокси )-5" нитробензонит1 ил, т.пя. 141-143 С»
Пример 30. 2-f4-(ИетилсульФинил )фенокси.)-5-нитробенэонитрил, с т.пл. 159-160 С, выход 92,8Ф.!
1041031
Пример 31. 2-(4-(Метилсуль" фонил фенокси )-5-нитробензонитрил,. о т.пл. 206-207 С, выход 98,23.: з
12физические свойства соединений бщей формулы (1) полученных в укаанных примерах, приведены в табл. 1, Таблица 1
° 4ваю Й
Т.пл., С
1 155-156
3"С t
1. 0 4ct
2 0 4СЮ
2 "СФ
1 153;5-154,5 Н
1 171-172.
6 0
4-SCH>
Н
4-Я), И(СН )2 Н
4-SOLON(C H ) Н
7 0
8 0
1 179,5-180,5
10 Ь 4 СК
11 0 3-ОСНОВ
0 4-CF3 о
И
0 4-СCH
14 0 . 4-Cf
15 0 4-ce
2-Сн
1 144,5-145,5
395-сй
3,5,63,4,5,616 0 2 F
17 0 2-F
18 S 4СФ
1904F
20 0 2-СФ
21 0 2 Се
22 0 г се
3"СМ
5-С 2
167-168,5
6-С Ю
157-159
1 196-19
0 3-СЮ
5-Се
Соеди-. нение, полученное по .примеру
4 -0 4-CJ " .н
5 0 4 О .. Н
9 0 4ct н
1 163-.164
1 150-151 5
1 124-126
1 221;5-223
1 163-164
1 162-164,5
102-103,5
1 . 154"155 5, 1 135-136,5
2; l 62-164, 3 152,5-154,5
127 I 5-129
1 137-139
132,5- :133,5 . 1 146-147
1041031
Продолжение табл, 1
Т.пл., С
Соединение полученное по прииеру
5-CF3
3,4-Ct
3,6-СЕ
4-5сН
4- Ы) СНЗ
30 0
31 0
Продолжение табл. 1
Найдено, 3
9,06
1,99
9,17
9,20
50,3
50,7
9,06
50,51 1,96 !
1,97. 3 48,93 2,21
56,85 2,57
5 68,67 3,64
48,9
8,78
9 05
2,21
10,29
2,52
8,44
3,60
8,43
68,7
6 58,73 3 52
3,61
58,5
9,77
9,79
7 51,87 3,77
8 54,39 4,56
69,76 . 3,51
10 53,70 2 "3
11 62,22 3,73
3,82
12,12
4,55
11,23
69,7
8,06 °
9,56
8,14
3,55
2,52
10, 32
3 72
Соединение, полученное по примеру
24 0 2С, 3 С 3
26 0 3-CF>
27 0 2-СФ
28 0 2-CP
29 0 2 СЗ
Выцислено, Ф
50,51 1,96
10,20 56,6
12,10 51,6
11,19 54,6
9,64 53,5
10 37 61,94
1 113 115
85,5-86,5
1 138-140
1 203-204,5
1 160-162
1 141-143
1 159-160
1 206-207
1041031
Продолжение табл. 1
Найдено, Соеди.нение, полученное по примеру
Вычислено, 3
Н
12 54,55 2,29
63,83 3,57
9,12.
9,09 54,5
2,38
9,93 . 63,8
3,69 9,89
3,35 9,6ф
14 58,24 3,14
58„2
9 70
8,15 45,4
45,45 1,47
16 50,01 1,29
17 47,29 0,92
1,64
8,26
50,3
9,09
8,97
1 53. 8,49
47,58,49
8,70
1,20
2,06
8,62 4ф,1
48,01 1,86
60,47 2,73
50,51 1,96
2,87 10,92
10,85 60,3
9,06 50,34
2;15
9,09
9,14
9,06
2,17
50,51 1,96
50,5
50,4
2,06
9,06
9 03
9,06
2,04
9,06
50,3
9 09 54,6
: 9,09 54,3 ..,7,45 47,9
9,12.
2,52
2,56
9,23
7,55
1,72
8,10
45 3
8,15
Ъ
8;15 27
8,23
1,69
8,15 45,4
8,30
1,75
3,38
9,27
9,47
55,5
30.
8,80 52,9
8,83
3,23
50,51 1,96
50,51 1,96
54,55 2,29
54,55 - 2,29
47,88 1,61
45,45 1,47
45,45 1,47
45,45 1,47
55,62 3,33
52,82 3,17
У
Замещенные бензонитрилы обладают антивирусной активностью, особенно они эффективны против пикарновирусов. И
Пикарновирусы включают такие вирусы как Коксакивирусы, Риновирусы и ряд вирусов болезней растений.
Указанные бензонитрилы обладают достаточно широким спектром действия, йе оказывают вовсе или проявляют незначительные побочные эффекты. Антивирусную активность замещенных бензонитрилоц определяют для культур
Таблица 2
Тестирование тканевой культуры
Соединение, полученное
Цитотоксичность, мкг/мл
RY-8
RV-64
RY""2
RY-1A
RY-5 сох А21
:по примеру
0,25 0,25
0,625 1 25
О;25 0,156
0 5
ЫОО
0 5
>100
0,625
2 5
2,5
1,25
>100
1,25.<6
< 0,625 < 0,625 0,625 ..< 0,3
И 00
17 1041 тканей по следующей тестовой методи" ке.
Монаслой клеток HeLa в чашках для культивироаания тканей {d = 16 мм) обрабатывают 1 мл.культурной среды (сре-> да Игла с добавлением сыворотки плода теленка ), содержащей целевые соединения в соответстаующей концентрации или без него.
После такой обработки монослой 1р клеток заражают 0,05 мл риновируса типа 1A(RV-А), риновируса типа 2 (ЯЧ-2) или Coasackie А „.вируса (Сох
А,1)в культурайьмой среде. Некоторые из бензонитрилов испытывают также против риновируса типа 5 (RV-5), ри" носируса типа 8 (RV-8) или риновируса типа 64 (RV-64). Контрольные клетки не заражают вирусами. Далее на культурах определяют цитотоксичность бензонитрилов и цитопатичный эффект спустя 48 и 72 ч после обработки.
Кроме того, некоторые соединения испытывают на животных по методике называемой как тест "одноразовой оральной дозы", согласно которой самцы швейцарских мышей весом 10-12,г заражают внутрибрюшинно (1P ) 0,2 мл,. т.е. дозой вируса, достаточной для того, чтобы вызвать смертельный исход у 10"1003 зараженных животных в течение 1О дн. после заражения ,СОх2 в фосфатном буферированном,физиологическом растворе, содержащем 1 термоинактивированной сыворотки плода теленка..Спустя 3 ч мышам орально З5 вводят 0,2 мл соединения данного изобретения суспендированного в 0,54 оксипропилметилцеллюлозы {метоцел ® ) или 0,2 мл 0,53 метоцел Щ не содержа. щей соединения изобретения, Концентра 40 ция соединения в суспензии составляет
031 18 .
30 мг/мл или 600 мг/кг ). Мышей проверяют ежедневно в течение 7-10 дн после заражения и смертные случаи ре" гистрируют. С помощью модифицированного объединенного метода наименьших квадратов Handsel-HachZel определяют . эффективность соединений в сравнении с контрольными группами, где абработ" ка вирусом отсутствует.. Среднеквадратичные значения, превышающие 3,84, соответствуют активности соединения в этом тесте 953.
Кроме того,:некоторые .из соединений также испытаны на животных с применением методики, называемой как тест
"Продолжительного орального приема".
Для этого вирус Сохзас ie А выращенный на клетках Не1„а, вводят в концентрации, которая приводит к смерти в 80-1004 случаев у мышей весом 1011 r в течение 10 дн., если мышам делают инъекцию 0,2 мл/мышь вирусного препарата.
Тестовые соединения вводят в пищу животного в концентрации .0,06 вес.3 в день, Смертные случаи как в контрольной,. так и экспериментальных группах регистрируют в течение 10 дн. и полученные результаты обрабатывают по методу наименьших квадратов. Значение наименьших квадратов, превышающие
3,84 указывают на то, что активность соединения составляет 95l.
Полученные результаты представлены в табл. 2 и 3 (символ ЙА указывает на то, что соединение предлагаемого > изобретения неактивно против км "петного вируса в стандартных тестовых условиях, пропуски в таблице указывают на то, что этот конкретный тест не проводили ).
19
1041031
Продолжение т абл. 2 тТекстирование тканевой культуры
Цитотоксичность, мкг/мл
RY-64
Сох AZ„
RY-5
PY-2
RY-8
RY-1А по примеру йА . 50
6,25
>100. 100
6,25
>100
6,25
+50 ЙА
)100
+100
12,5
>100
+ 3,125 1,б
6,25 3,125
l,6
25 .
6,25
3,125
0,3125 0,625
2 5
3,125
>50
3,125 C 3,125 6,25
6,25
750
12 5
6,25
3,125 ,1,25
12 5
>50
1,25
2 5
1,25 0,3125
1,25 0 3125
3,125
1,25
3,125
43, 125
125
12,5 ф,25
6,25
1,25
3,125
1О
2 5
+2 5
0,625 0,625
0,625 0,625
0,625
1,25
< 3,125
>50
21 с6,25
46,25 3,125
6,25
12 5
>50
3,125
3 125
3,-125
3 125
: 3 125 <3,125 3,125
>50
3,125
6,25
6,25
3,125 25
>50
i,25
320
0,625 1,25 0,625
0,625 1,25
1"., 5
2,5
2>5
1,25
10
NA 20
«+5
+1О
>20
2,5
2,5
125 5
2,5
3,125 3,125 3,125
>?0
6,25 ñ6,25
Соедйнение, полученное
NA 46,25 6,25 (3,125: 3, l25 с3,125
3,125 12,5
0,3125 0,625
3,125 6,25
3,125 ИА
1041031
22
Продолжение табл. 2
Цитотоксичность, мкг/мл.
Тестирование тканевой культуры
RY-8
RY-64
RY" 1А
RY-2
Сох А21 ВУ-5
3 l >100
32 50
t2,5 <6,25
ЙА
3,125 <3,125 3,125 ЙА
NA. ЙА
Цифры в графе "Цитотоксичностьн соответствуют концентрации соединения, которая оказалась токсичной для клетки в мкг/мл.
Наименьшая концентрация соединения (мкг/мл ), необходимая для того, чтобы вызвать 504 снижения цитопатического эффекта.
% 3(+
Известное соединение 5-(3,4-дихлорфенокси)-2-нитробензонитрил.
Т а б л и ц а 3
Тестирование животного
Продолжительный оральный прием
„2%Ф.
Клиническая оральная доза, мкг/г
Доза, вес.б Х
23,62
5,36 0,06
600
600
1,38
3 659 0,06
5,81
2,139 0,06
600
10,61
600
0,26
600
6,91
600
0,06
9 03
0,06
2,84
0,64
4;805 0,06
600
0,215
10,513
600
0,06
18,94 0,06
0,095 0,06
18,82
600
10,45
600
0,06
0,0253
2 „
П р и м е ч:а н и е . Х " среднеквадратичные значения.
Соеди" ение, полученное по примеру
Соединение, полученное по примеру
0,252 0,06
0,719 0,06
0,609,0,06
23 1041031 24
Данные табл. 2. и 3 свидетельству- . турами тканей они проявляют более высо- . ют о том, что больюая часть замещенных. кую активность,более высокую ингитирубензонитрилов обладает более широким ацую вирусную активность они проявляют спектром действия и в тестах с куль- и в случае тестированияживотного.
Составитель M: Måðíóëîâà
Редактор Н. Рогулич Тех е С.Ийг нова Корректор Bå .ГиЯняк.
Заказ 961/ О . Тираж ;, - Подписное
ВНИИИИ Государственного комитета СССР по делам изобретений,и открытий
1ЦОЯ Москва . М-- Ра ская наб. 4
Филиал ППП Патент, г. Ужгород, ул. Проектная,