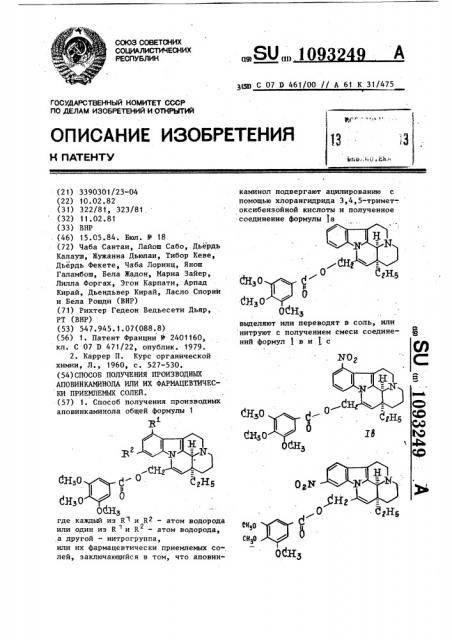
Способ получения производных аповинкаминола или их фармацевтически приемлемых солей
Иллюстрации
Показать всеРеферат
1. Способ получения производных aпoвинкa шнoлa общей формулы 1 -«1 каминол подвергают ацилированию с помощью хлорангидрида 3,4,5-триметоксибензойной кислоты и полученное соединение формулы 1а
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИН
-SU„„10
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К ПАТЕНТУ
hr,о НЗ О
Обнз й?зО био бНЗО б
dz o
Обнз (- РН5
Og>
2+5 "30
НЗ
ОаНз (21) 3390301/23-04 (22) 10.02.82 (31) 322/819 323/81 (32) 11.02.81 (33) ВНР (46) 15.05 ° 84. Бюл. N 18 (72) Чаба Сантаи, Лайош Сабо, Дьердь
Калауш, Жужанна Дьюлаи, Тибор Кеве, Дьердь Фекете, Чаба Лоринц, Янош
Галамбош, Бела Жадон, Мариа Зайер, Лилла Форгах, Эгон Карпати, Арпад
Кирай, Дьендьвер Кирай, Ласло Спорни и Бела Рошди (BHP) (71) Рихтер Гедеон Ведьесети Дьяр, РТ (ВНР) (53) 547.945.1.07(088.8) (56) 1. Патент Франции У 2401160, кл. С 07 D 471/22, опублик ° 1979.
2. Каррер П. Курс органической . химии, Л., 1960, с. 527-530. (54)СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
АПОВИНКАИИНОЛА ИЛИ ИХ ФАРИАЦЕВТИЧЕСКИ ПРИЕИЛЕИЫХ СОЛЕЙ. (57) 1. Способ получения производных аповинкаминола общей формулы 1 i где каждый из R1 и R2 — атом водорода или один из R " и R — атом водорода, а другой — нитрогруппа, или их фармацевтически приемлемых солей, заключающийся в том, что аповин31а11 С 07 9 461/00 // А 61 К 31/475 каминол подвергают ацилированию с помощью хлорангидрида 3,4,5-тримет оксибензойной кислоты и полученное соединение формулы 1а выделяют или переводят в соль, или нитруют с получением смеси соедине- ф ний формул 1 в и 1 с
1093249 г
1 бн,о нз о обн ги Опи- (1я O
1н о
Обвэ
3.— С вЂ” 0 2 & где R алкил С -CS или фенил, возможно замещенный трифторметилом или С -С, - 35 алкоксигруппой, обладают свойствами селективно расширять кровеносные сосуды мозга. Эти соединения получают путем ацилирования (+) - винкаминола преимущест" венно в среде хлорированного углево- НЗО, дорода с помощью галоидангидрида соот- Н50 ветствующей карбоновой кислоты при комнатной температуре 1 .
I8,которую затем разделяют на отдельные продукты формулы Тв или 7 с или при желании переводят в соли.
2. Способ по п. f, о т л и ч а юшийся тем, что ацилирование про1
Изобретение относится к способу получения новых производных аповинкаминола общей формулы где каждый иэ R"и R — атом водорода, или один из R и R - атом водорода, а. другой — нитрогруппа, или их фармацевтически приемлемых солей, обладающих ценными фармакологическими свойствами.
Известные структурные анало сываемых соединений — производ эфиров винкаминола общей форму водят в среде хлорированного углеводорода.
3. Способ по п. 1, о т л и ч а юшийся тем, что нитрование проводят при температуре около 0 С в присуто ствии ледяной уксусной кислоты.
Цель изобретения — получение новых производных винкаминовых алкалоидов, обладающих иными. фармакологическими свойствами по сравнению с известными
5 структурными аналогами, Цель достигается тем, что согласно способу, основанному на известном методе ff 1, а также на методе нитрования ароматических азотсодержащих
1О соединений с помощью концентрированной азотной кислоты при 0 С в присутствии ледяной уксусной кислотыГ23, аповинкаминол подвергают ацилированию с помощью хлорангидрида 3,4,5-три15 метоксибензойной кислоты и полученное соединение формулы
ЗО выделяют или переводят в соль, или нитруют с получением смеси соединений формул
1093249
Оги
СН,О
СН 0
10 которую затем разделяют на отдельные продукты формулы 1в и 1с и при желании переводят в соли.
Процесс ацилирования предпочти- 15 тельно ведут в среде хлорированного углеводорода, а нитрование предпочтительно проводят при температуре о около О С в присутствии ледяной ук. сусной кислоты. 20
Пример 1. Получение (-)-аповинкаминол-3, 4, 5 -триметокси/ t бензоата.
3,10 г (10, 1 ммоль) (-)-аповинкаминола растворяют в 60 мл безводного 25 дихлорметана, после чего к раствору добавляют 3,10 r безводного карбоната натрия и 2,50 r (10,9 ммоль) хлоран-, гидрида 3,4,5-триметоксибензойной кислоты. Реакционную смесь перемеши- З0 вают в течение 24 ч при комнатной
Ф, температуре, затем разбавляют 100мл воды. После отделения органической фазы из водного слоя дважцы порциями но 20 мл проводят экстракцию ди3S хлорметаном. Объединенные дихлорметановые растворы высушивают над безводным сульфатом магния, фильтруют и фильтрат упаривают при пониженном давлении. В результате получают 4,50 r 40 целевого соединения. Выход 89,1Х.
С о Нэ4020
Мол. bee. 502, 61.
ИК-спектр (пленка) щ „ 1725 см (-C=0), 1620 см "(=С=С)
Масс-спектрометрия (м/е): 502/53, 432/100, 290/17, 261/41, 220/19, 216/23, 212/18, 195/35. (с = -22,0 (c=0,7 дихлорметан)
Пример 2. Получение (-)аповинкаминол-3, 4, 5 -триметокси1 I бензоатгидротартрата.
Полученный по примеру 1 продукт растворяют в диэтиловом эфире и к раствору добавляют насыщенный эфирный раствор D-винной кислоты до тех пор, пока из него не прекращается выделение осадка гидротартрата. Выпадающий осаO док соли отфильтровывают и высушивают. T.ïë. 120-121 С, мол. вес. 652,7.
ИК-спектр (KBг):4„щ„ 1730 см "(-С=О), 1640-1655 см "(=С-С=). (И.ф= -8,5О(с=1, пиридин).
Пример 3. Получение (-)-9-нитро-аповинкаминол-3,4,5 - триметоксибензоата и (-)-11-нитро-аповинкаминол-3,4,5-триметоксибензоата. (1
I t
5 г (-)-аповинкаминол-3,4,5-триметоксибензоата растворяют. в 50 мл ледяной уксусной кислоты,-после чего к раствору при О С и перемешивании б добавляют смесь 20 мл ледяной уксусной кислоты и 10 мл концентрированной азотной кислоты (d=1,52). Затем реакционную смесь выпивают в 350 мл ледяной воды и с помощью 25Х-ного водного раствора аммиака устанавливают рН 9.
Из щелочного раствора проводят экстракцию дихлорметаном: сначала 250 мп, а затем дважды порциями по 200 мл.
Объединенные органические растворы высушивают над безводным сульфатом натрия, фильтруют и фильтрат упаривают досуха при пониженном давлении.
Полученную смесь разделяют на отдельные компоненты с помощью хроматографии (адсорбент-силикагель 60, элюентсмесь бензола и ацетона в соотношении
10:2). В этих условиях Rg 9-нитропроизводного больше, чем 11-нитропроизводного.
Выход: 1,7 r 9-нитро- и 1,8 г 11-нитропроизводного. (-)-9-Нитро-аповинкаминол-3, 4, 51 г триметоксибензоат имеет следующие физические константы.
Т.пл. 77-78 С.(Û)D-78,5 (с=1. хлороформ) .
"Н-SIMP (CDC Pg): с 3,8(S, 6Н, 2хСНЗ О-); 3, 91 (S, ЗН, 1хСН30-);
7,3(d, 1Í, Н1 ); 7,96 (d, .1H, Н „);, (-)-11-Нитро-аповинкаминол-3,4,5Ф ( триметоксибензоат имеет следующие физические константы.
Т.пл. 72-73 С,Щр =-143,3 (С=1, хлороформ) .
"Н ЯМР(СОС9 ): al" 3,8(S, 6н, 2хСН О-), 3 9(S, 6Н, 2хСН О-); 7 56 (d, 1H, Й ), 8,1(d, 1Н, Н. ); 8,9(d, 1Н, Н ц).
0 р и м е р 4.Получение 9-нитроаповинкаминол-3,4,5-триметоксибензоатгидрохлоридаи 1 1-нитро-аповинкаминол-3,4,5-триметоксибензоатгидрохлорида.
Полученные в соответствии с приме-. ром 19-нитро- или 11-нитро-аповинками1093249
S нол-3,4,5-триметоксибензоат растворяS ют в метаноле, после чего с помощью солянокислого раствора метанола устанавливают рН 3-4. При добавлении диэтилового эфира образующийся гидрохло-5 рид выпадает в осадок, который отфильтровывают, промывают и сушат.
Т.пл. гидрохлорида 9-нитро-производного 144-150 С, гидрохлсрида
11-ни гропроизводного 141-144 С.
Было установлено, что описываемые в соответствии с настоящим изобретением соединения могут оказывать влияние на активность энзима фосфодиэстеразы и могут использоваться для лечения и профилактики кожных заболеваний, связанных с патологической пролиферацией клеток.
Так как некоторые иэ кожных заболеваний, связанных с патологической пролиферацией клеток (например, псориаз), встречаются только у людей, то действие соединений по отношению к псориазису можно обнаружить только косвенным путем.
Установлено, что патологическая пролиферация клеток сопровождается снижением уровня аденозин-монофосфата (с-АМФ). Известно, что с-АМФ об- ЗО разуется в результате воздействия аденилциклазы и разлагается под действием энзима фосфодиэстеразы.
40.Таблица 1
Влияние на активность энзима,Ж по отношению к контрольному препарату, при концентрации соедиСоединение нения мол/л
1 х 10
5х10
5х 106
64,5
49,2
47,2
Таким. образом, если соединение оказывает заметное тормозящее действие на функцию фосфодиэстеразы, то его, можно использовать для лечения псориаза или других связанных с патологической пролиферацией клеток заболеваний.
Модельные опыты проводят с помощью фосфодиэстеразы, вьщеленной из тканей животных (мозга крыс и крупАповинкаминол 3, 4, 5-триметоксиl бенэоат гидрохлорид ного рогатого скота, сердца крупного .рогатого скота. ф I
Энзим выделяют по методу I.Sehroder, Н.V. Richenberg.
Очистку вьщеленного энзима фосфо диэстеразы осуществляют .по методу Т,С, Hardman, Е. M. SutherIand.
Активность очищенного энзима определяют с помощью радиоизотопного метода по С.Poch в присутствии избытка третичного с-АМФ (10, 1 ммоль с-АМФсубстрата, из которого 3Н-с-АМФ
2,59 К Sg) в инкубационной системе вначале без тормозящего средства, а затем в присутствии.9-нитро- или
11-нитро-аповинкаминол-3, 4, 5-три1 метоксибензоата в качестве тормозящего средства после инкубации в течение 20 мин.
Из испытуемого соединения готовят
1-миллимолярный водный солянокислый основной раствор. С помощью этого основного раствора к инкубированному энзимному препарату добавляют различные количества испытуемого соединения с таким расчетом, чтобы концентрация его в инкубированном образце составляла 5x10, !х10, 5х10 1х10, 5x10, и 101мол/л. Аналогичным образом к энзимному препара-, ту добавляют водный раствор папаверина (контрольное соединение).
Активность контрольного препарата (раствора энзима без добавки тормозящего средства) принимают за 1007.
Активность растворов, содержащих в качестве тормозящего средства апо
1 винкаминол-3, 4, 5-триметоксибензоат, его 9-нитро- или 11-нитропроизводное или папаверин, выражают в процентах по отношению к контрольному препарату.
Результаты, полученные при использовании энэима, вьщеленного из мозга крыс, приведены в табл, 1.
1093249
Продолжение табл. 1
Соединение
1 х 10Г 5 х 10
5 х 10 (-)-11-Нитра-аповинкаминол3,4,5 -триметокси -бензоат гидрохлорид 53,6
44,4
37,3
37,7
61,6
62,9
Папаверин гидрохлорид
60,5
89,7
91,2
Таблица 2
50, моль, на фосфодиэстеразе выделенной из
Соединение сердца крупного рогатого скота мозга крыс
1,5
15
Папаверин гидрохлорид
70
Из приведенных таблиц видно, что соединения полученные по предлагаемому способу в большей степени тормозят действие энэима, выделенного из сердца крупного рогатого скота ,и мозга крыс (в 35-50 и 4,5-9 раз соответственно), чем использовавшийся для сравнения папаверин. (-)-9-Нитро-аповинкаминол3, 4, 5 -триме ток сибеизоат гидрохлорид
Аналогичным образом определяют активность по отношению к энзиму, выделенному из сердца крупного рогатого скота.
На основании полученных результатов строят кривую зависимости активности энзима от логарифма концентраАповинкаминол-3,4,5-триметокси( бензоатгидрохлорид.
1 (-)-1i-Нитро-аповинкаминол-3 4 5 -триметоксибензоат .гидрохлорид (-)-9-Нитро-аповинкаминол-3,4,5 -триметоксибензоат гидрохлорид
Влияние на активность энзима,Ж по отношению к контрольному препарату, при концентрации соединения, мол/л ции ингибитора энзима, выраженной в микромолях, и на этой кривой находят концентрацию ингибитора, при которой активность энзима снижается на 503 (18о)
Полученные результаты представлены в табл. 2.
Первые клинические опыты проводили с помощью использующихся для наружного применения препаратов (мазей, кремов, растворов, настоек, паст, аэрозолей), содержащих активное вещество. В опытах использовали кремы (! с содержанием аповинкаминол-3,4,5-триметоксибензоата или его (-)-949
1О
Таблица 3
Активное вещество, Соединение 1,8 0,6 0,5 1,8 1,3 0,75 1,2 0,4 формулы 1а
0,7 2,5 2,5 1,3
1в 2,2 1
1,5 0,5 0
1с 24 18 13 22 13 13
1 6 1,2 081
Составитель И. Федосеева
Техред K.Kàñòåëåâè÷ Корректор В, Синицкая ю
Редактор Л. Веселовская
Заказ 3289/47
Тираж 410 Подписное
ВНИИНИ Государственного комитета СССР по делам изобретений и открытий
113035, Иосква, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент", r. Ужгород, ул. Проектная, 4
9 10932
-нитро- или (-)-11-нитропроизводных, Х: 2, 1, 0 5, О 25 и О 1.
Испытания препаратов проводили на больных, страдающих псориазом.
При этом отбирали пациентов, которые одновременно не получали никакого другого систематического лечения (например, иммуносупрессивного, цитостатического или лечения с помощью глюкокортикоидов). 10
Отобранные больные подвергались исследованию по методу Плакэ: одну половину пораженного участка кожи обрабатывали кремом, содержащим активное вещество, а другую — лож- 15 ным лекарством. Для сравнения дру) гие пораженные участки кожи обрабатывали другими лекарствами, например кремом, содержащим в качестве активного вещества флуметазонпивалат 20 и салициловую кислоту. Начинали испытания с кремов с максимальным содерТаким образом, предлагаемый способ позволяет получать новые производные жанием активного вещества, после чего обрабатывали других пациентов кремами с минимальным содержанием активного вещества. Курс лечения продолжался в течение двух недель.
Крем накладывали ежедневно.
Эффективность соединений оценивали по трем симптомам: воспалению, инфильтрации и десквамации (шелушению).
Каждый из симптомов оценивали в баллах. При этом О означает отсутствие симптома, 1 — умеренный симптом, 2 — сильный симптом, 3 — очень силь" ный симптом.
Симптомы оценивали до начала лечения (4), после лечения в течение одной (8) и двух (С) недель.
В табл. 3 приведены результаты испытаний средние баллы — общее число баллов, деленное на количество больных). винкаминовых алкалоидов, обладакнцие ценными фармакологическими свойствами.