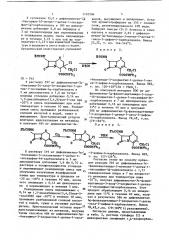
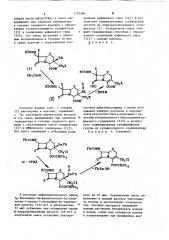
Способ получения 1-оксадетиацефалоспоринов
Иллюстрации
Показать всеРеферат
СПОСОБ ПОЛУЧЕНИЯ 1-ОКСАдаТИАЦЕФАЛОСПОРИНОВ общей формулы о RCONH -I -1J СНгХ CQOW где R - свободный фенил, фенил, замещенный нитроили цианогруппой, метилом или атомом хлора, бензил или феноксиметил;. Е - водород или метоксигруппа; СООВ - карбоксигруппа, бензилоксикарбонил или дифенйлметоксикарбонил; X - водород или галоген или 1-метилтетразол-5-илтиогруппа , отличающийся тем, что соединение общей формулы о д ксокнЧ-r N z СНгХ о соов где R , Е, СООВ и X имеют приведенные значения; Z - галоген, окси-, трифторацетокСИ- , фенилтио-, Ci-Cit-алкилтиоили i фенилселенил-группа, подвергают обработке метилатом щелоч СО ного металла, пиперидином, 1,5С -диазабицикло С4,3,01нон-5-еном или 1,5-диазабицикло С5,4,0 ундец-5-еном, когда Z - атом галогена, или тионилхлоридом или хлорокисью фосфора в присутствии пиридина или метилпиридина , или пивалоилизоцианатом, когда Z - оксиили трифторацетоксигруппа , или М-хлорпербензойной 00 О) кислотой или перукс.усной кислотой, когда Z - фенилтио-, ,-алкилтиоили фенилселенил-группа, в раствориа: теле при температуре от -50° С до температуры кипения ацетона с обратным холодильником в течение времени от 10 мин до 5 сут.
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (19) (11) 1б1) С 07 D 498/04
«/ описании изоьрктяни .
И IlATEHTV Ад.
СН2Х
Е. СОЯЯ
) ОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 2706007/23-04 (62) 2579850/23-04 (22) 03. 01 . 79 (23) 14. 02. 78 (3i ) 15813/77 (32) .15.02.77 (33) Япония (46) 23.08.84. Бюл. ¹ 31 (72) Мицуру Есиока, Соитиро Уео, Есио Хамасима, Икуо Киккава, Терудзи
Цудзи и Ватару Нагата (Япония) (71) Сионоги энд Ко ЛТД (Япония) (53) 547.867.2.07(088.8) (56) 1. Патент СССР № 1056903» кл. С 07 D 498/04, 1976. (54) (57) СПОСОБ ПОЛУЧЕНИЯ 1-ОКСАЦЕТИАЦЕФАЛОСПОРИНОВ общей формулы
СООБ где R — свободный фенил, фенил, за" мещенный нитро- или цианогруппой, метилом или атомом хлора, бензил или феноксиметил;
Š— водород или метоксигруппа
»
СОО — карбоксигруппа, бензилоксикарбонил или дифенилметоксикарбонил;
Х вЂ” водород или галоген или 1-метилтетразол-5-илтиогруппа, о т— л и ч а ю шийся тем, что соеди-нение общей формулы
СООВ .где R Е, СООВ и Х имеют приведенные значения;
Z — галоген, окси-, трифторацетокси-, фенилтио-, С»-С»-алкилтио- или фенилселенил-группа, подвергают обработке метилатом щелоч « ного металла, пиперидином, 1,5-диазабициклоС4»3,01нон-5-еном или
1,5-диазабицикло Г5,4,01ундец-5-еном, когда Z — атом галогена, или тионилхлоридом или хлорокисью фосфора в присутствии пиридина или метилпиридина, или пивалоилизоцианатом, когда Z — окси- или трифторацетоксигруппа, или М-хлорпербензойной кислотой или перуксусной кислотой, когда Z — фенилтио-, С -С -алкилтиоили фенилселенил-группа, в растворителе при температуре от -50 С до тем. пературы кипения ацетона с обратным холодильником в течение времени от
10 мин до 5 сут.
1110386
К1СОЮН
z (Щ
Сн Х
CO0S1
00+3
М вЂ” M
1! сн;й 00ВЗ ) 1 ЕЗ
f 5
R СОИН
О +3
СООСНРЬz
t,0
QKg сооснв .
Изобретение относится к способу получения новьх производных 1-оксадетиацефалоспоринов, которые могут быть использованы в качестве продук. тов в синтезе биологически активных соединений.
Известен способ получения 1-оксадетиацефалоспоринов общей формулы где Ar — 2-или З-тиенил, фенил, й-оксифенил или и-ацетоксифенил;
СООВ и СОО — независимо одна от 20 другой свободная или защищенная карбоксигруппа, ацилированием 7-амино-7-метокси-1-оксадетиацефалоспорина соответствующей арилмалоновой кислотой или ее реакционноспособным производным.
Эти соединения обладают биологически активными свойствами (13, Цель изобретения — получение новых производных 1-оксадетиацефало- 30 споринов, расширяющих ассорт1 мент полупродуктов для синтеза биологически активных веществ.
Поставленная цель достигается способом получения 1-оксадетиацефало. 35 споринов общей формулы
СООВ1 где К» - свободный фенил, фенил,, замещенный нитро- или цианогруппой, 45 метилом или атомом хлора, бенэил или феноксиметип;
Š— водород или метоксигруппа;
СОО — карбоксигруппа, бензилокси-! карбонил или дифенилметоксикарбонил;
Х вЂ” .водород или галоген, или
1-метилтетразол-5-илтиогруппа, Ph. ВОЯК который заключается в том, что соеди кение общей формулы
Е где R, Е, СООВ и Х имеют приведенные значения;
Z. — галоген, окси-, трифторацетокси-, фенцлтио-, С,-С -алкилтио- или фенилселенил-группа, подвергают обработке метилатом щелочного металла, пиперидином, 1,5-диазабицикло(4,3,01нон-5-еном или.
1,5-диазабицикло (5,4,01ундец-5-еном, когда Z — - атом гологена,, или тчонил" хлоридом или хлорокисью фосфора в присутствии пиридина или метилпиридина, или пнвалоилизоцианатом, когда
Z — - дикси- или трифторацетокси-группа, или Я:-хлорпербензойной кислотой или перуксусной кислотой, когда Z — - фенилтио-, С -Сч-алкилтио- или фенилселенил-группа, в растворителе при температуре от -50 С до температуры кипения ацетона с обратным холодильником в течение времени от
i0 мин до 5 сут.
Соединения могут быть выделены из реакционной. смеси посредством удаления использованного растворите.ля, непрореагировавших веществ, по- .
1. бочных продуктов и подобных загрязняющих примесей с помощью концентрирования, экстрагирования, промывки, высушивания или аналогичных методов и очищены при помощи повторного осаждения, хроматографии, кристаллизации, абсорбции или аналогичных методов очистки.
Пример 1. Раствор 1-детиа-1-оксацефамового соединения в растворителе смешивают. с отщепляющим агентом в условиях, приведенных в табл.1, и получают 1-детиа-1-оксацефамовое
;соединение (Е).
Показатели для реакции 12 представлены с целью иллюстрации методики эксперимента отщепления (см. табл.1).
3 1110386 4
K cÓ ll H3HH 15,0 r дифенилметил-7 водой, высушивают и выпаривают, рста-бенэамин-ЗЮ-метил-1-детиа-1-оксаце- ток хроматографируют на 350 г силнка-
Фам 4/=карбоксилата в 100 мл дихлор- геля, дезактивированного 101, воды. метана добавляют 6,8 мл пирйдина и Элюируют смесью (9:1) бензола и этил3 мл тионилхлорида при перемешивании 5 ацетата и полУчают 2,65 г дифенили охлаждении льдом; смесь перемешива- метил-7а -бензамидо-3™етил-1-детиа-1ют в течение 7,25 ч пои той же тем- -окса-3-цефем-4-каРбоксилата. Выход пературе и 2, 25 ч при комнатной темпера" 25, 27, т. пл. 144-146 С. туре и выливают в смесь воды со льдом.
Органический слой отделяют, промывают Пример 2.
KCONH
RCONH
N
0, Свгс1
СООСНГЬ, -бензамидо-Ç-хлорметил-!-детиа-1-ок-. са-3-цефем-4-карбоксилата. Выход 867, т. пл. 120-128 C(R = PhCH ).
По описанной методике 800 мг дифенилметил-7Ы-фенил-ацетамидо-3-хлор-ЗЯ.-хлорметил-1-детиа-1-оксацефам-4 -карбоксилата в 7 мл дихлорметана об« рабатывают О, 16 мл пиперидина при
15 С в течение 40 мин и получают
586 мг дифенилметил-7 ;фенилацетамидоL 3-хлорметил-1-детиа-1-окса-3-цефем-4-карбоксилата. Выход 78,4Х, т.пл.
1,79-182 С.
Пример 3.: е ЩС1 сооснгь (К -- РЬ)
К раствору 597 мг дифенилметил-7oL-б енз амид-3 L-хлор-3 й-хлорм е тил-1-де» тиа-1-оксацефам-4 -карбоксилата в
5 мл дихлорметана и 1,6 мл тетрахлорида углерода добавляют 0,14 мл
1,5-диазабицикло(3.,4,0)нон-5-ена при о
-20 С и смесь перемешивают при этой температуре в течение 10 мин. Реакционную смесь промывают разбавленной соляной кислотой и водой, сушат и выпаривают. Кристаллический остаток
30 повторно кристаллизуют из метайбла и получают 484 мг дифенилметил-7аРЬСОЯК
РЬСОЯН эвм
О
О; СН O -. СН С1 СН С1
СООСНРЬ QOOMPh 2 . СООCBPh, К раствору 519 мг дифенилметил-7 - -3-цефем-4-карбоксил В
40 ар оксилата. Выход 863, -бензамидо-3-экзометилен-1-детиа-1- т. пл. 127- 128 С.
-оксацефем-4k-карбоксилата в 5 мл Согласно этому же способу проводихлорметана добавляют 1,6 мл 0,76 н,,цят Реакцию 705 мг дифенилметил-7араствора в четыреххлористом углероде -Фенилацетамидо-3-метилен-1-детиа-1и перемешивают реакционную смесь при -оксацефем-4oL-карбоксилата с 1,77 обл учении излучением вольфрамовой
45 эквивалентами хлора в 7 мл хлористолампы при температуре в пределах от го метилена при температуре ниже о-00
-20 до -30 С в течение 40 мин, после -25 С, получая дифенилметил-7 -фенилчего смешивают с 0,14 мл циклопенте- ацетамидо-3-хлор-3-хлорметил-1-детиана и перемешивают в течение 5 мин. -1-оксацефем-4М-карбоксилата. Этот
Реа еакционную смесь перемешивают с продукт обрабатывают 0,16 мл пипери50
0,14 мл 1,5-диазабицикло(3,4,0)нон-5- дина при 15 С в течение 40 мин, полу"
-ена(РВИ) при -20 С в .течение 10 мин, чая в результате 586 мг дифенилметил промывают разбавленной соляной кисло- 7о ;фенилацетамидо-3-хлорметил-1-детиа той и водой, сушат и отгоняют раство- -окса-3-цефем-4-карбоксилата. Выход
Ритель. Кристаллический остаток пере-55 78,4Ж,т.пл. 179-182 С (c.разложением) с разложением . ,кристаллизовывают из метанола, получая Согласно данным, представленньФк таким способом 484 мг дифенилметйл-7d; в табл. 2,. раствор сульфида (I) в
-бензамино-3-хло метил-1р тил 1-детиа-1-окса- дихлорметане смешивают ср,-хлорпербев1110386 динення цефемового типа (III) в результате элиминирования сульфеновой кислоты из непрореагировавшего сульфоксида (I). Реакционную смесь очи5 шают традиционным способом с образованием соединения цефемового типа (III) с данным выходом.
Пример 4.
МЮЯН
СН2Х
СООВ
Е
ЕСОР
СН СОО
ЕСОВН
СЯ2Х
СООВ
Согласно данным табл. 3 сульфид (I) растворяют в ацетоне, смешивают с 5н. раствором перуксусной кислоты и эту смесь выдерживают при заданной 30 температуре в течение заданного времени с образованием смеси сульфоксида (II) и цЬфемового соединения (III).
Эту .смесь смешивают с небольшим колиРй.СОБАК
Sech
СЕ2 С1
СООСНРЬ, g
СЫ ei снгк
m — СРВ
КСОЯН
ePh! CHZCi
СООСНРЬ3
К раствору дифенилметилового эфира, 7о-бензамидо-Зо -фенилселенил-Зц-хлорметил-1-детиа-1-оксацефем-4а-карбоиовой кислоты (132 мг) в дихлорметане (3 мл) добавляют при охлаждении льдом
9l-хлорпербензойную кислоту (49 мг) и полученную смесь оставляют реагнрозойной KHcJIQTOH(m-СРВА) и смесь вы-: держивают при заданной температуре в течение заданного времени с образованием соответствующего сульфоксица. (II) н соединения цефемового типа (IrI). Эту смесь нагревают с обратным холодильником в течение 30 мин в среде ацетона с образованием соеО СН2Х (ш) сооз
sK - -Иозк чеством диметилсульфида с целью разложения избытка реагента и полученную в результате смесь нагревают с обратным холодильником с образованием це— фемового соединения (III) в результате элиминирования сульфенильной группы из сульфоксидного соединения(ц)
Пример 5. (селенил). вать на 10 мин. Реакционную смесь переливают в водный раствор тиосульфата натрия и экстрагируют этилацетатом. Раствор экстракта промывают водным раствором бикарбоната натрия и водой, сушат над сульфатом натрия и концентрируют при пониженном дав1110386
Е
Е СОЕК
RC0NH Е
Н2Х (I) сн,х
I ()f
R СОЯН
СНгХ
C003 ленни. Остаток очищают хроматографией на силикагеле с образованием дифенилметилового эфира 7о-бензамидо-3-хлорметил-1-детиа-1-окса-3-цефемг
ОО
Согласно данным табл,,4 и 5 сульфид (Х) реагирует с раствором м-хлорпербензойной кислоты в дихлорметане при заданной температуре в течение заданного времени с образованием суль-4-карбоновой кислоты (63 мг) .
ИК: 1МД",ф 3340, 1793, 1732, 1675 см .
Пример 6. фона (ZZ) и затем такой сульфон обрабатывают сильным основанием в среде дихлорметана с образованием соединения цефемового типа (Ш) .
1110386
О О
С0 «Ф
I I О Ф
ОО Ф фь
ОЭ
l Ф
ОО ф О0 Оа фС
ОО
CO
Ф
Ф
ОЭ ж а
С 4 .CO
Ю
О0
CO О
СО
CO
0С х
С! м с 4 ъР С0
СС Е °
С В ож
С иЪ
О 1
01 CO мИ в м
Юм ф
СС 0!
»» ць. о х
Ю5.
Ио
CV
» о
СЭ х о н
° 4
С» и
»
О х о
СС
О
Cl х о ж о
С4
Л"
О х
Ю
Ю
С !
Ю
Ю
СО
Ю
l/l х х х Ъ! I I ж - х
° С СО. ж х С 1 а-1
1, х х
Ю Ю
- к
1 1
М х, СР О О
1 1
М н и и !
» Е»
СР 03 9)
1 I 1
° С Ф
С4 С4 фе ъ4
1 о
v!.СС
С4 ,,%" о
s С Ай
Р4 D 04 W C4
I 1 I 1 I
hl м м! О, С СР
Ю
СС
I х.
o„
Ц ь с
„s
M CV е
КЮ
Р Ра Рф
1 1
СЧ
СЧ
v.
ОС х о. м о о
Ю
Э
СС! ! и х
k и
1» х
I !.И СС
С4,И сС Р, хоо о
1 I
I l
° 0
СЧ
1 о
СЧ
«СЪ о
СЧ
1 о
СЧ х
СЧ
Ch с Ъ
«О м х
С Ъ и
С Ъ
Ca a
Ф 44 а к
1 1
« 4«
4 4
1 .Ф 1
1 1
CO
С o о
«СЪ «СЪ
«О Ct
С 4
«4Ъ
С«Ъ
СЧ
Ф Ф
an 01
С 4
«С« с \
О
1 о
an
«С«
4 4
1 ю о о о с"Ъ о
Р о
° О (4« о с х
IA (4 х (1
Ю
С 4
K . и (C
«I х о
» ° ь м an мо
«z
44« ох
О 4( (СЪ О
33 г «4 л«0 л сЪ 0«
I1a х ою оо с»\ сс z
III
v x о е о
О ао сЪ Ч!
t4 И
Ч «4«
0Ъ
c«4 «Са
Дс М
V0:
О ю
cia o
D с. х
Kl а
D
Л
«х
CI
° Ф о
44 х
v о
СЧ
° ю с о сч о о
° 4 D о
И (4« с(4 с( х
Г->
v сс о
an с4
«4
v с4 х
С 4
44
I о
Cv х
v (I
D
С4 х
v с-« о (4 х
v (0
c 4
Ю
С«
In
О«
«СЪ
СЧ
° (О
Ю
С««
Ю
С4 х
v о х
О о Х и о м
D х
Ю
М
v о х
ТЪ
IЪ х о (I
1 х о
1 х х ° с о. о о
1 1 1
«4
1 х о
14 и
СП
4
1 н и (4 и
CI
1-4
I (—
«с
4 о
4 о
1 х
1 с4 с х о
1 х х
Сч с
1 с
С« х
С с
04 с.( с (a4
C ° с (aI х
CL х о
Ф х ю
v ! с
1 с
1 с
0«
I с
04
I с
I с
04
1 с
СЧ м с ь
С 4
° I
«0! an
aC l
RI
1 х! 1
1 1
1 1
1 1
С Ъ л
Са«0а х о о щ «0
1 1 (4 С4 с
0. о (41
«Э
Ф
I ф
W
° »
СЧ
00 С
i a0
° »
О «СЪ
Ф с л м .С0 (О
«О
»
CO
С 4 л
Ф
С0
CO л
Ю о с«Ъ .Ф
С «
lllO386 (Ч
«(Ъ
СЧ ф
an «(0
С 4 Т
СЧ
Ю
Ю
С«
;Г ю х ь о о д
° Х
ov z
О1 (0 (оg а
»« и
Л 7
v o х
v v х
1> F х
СЧ (O
С Ъ
«О
С 1
» х с Ъ
M с»1
-Ф х
Ю
fC с л н
o s
«1 СЧ
z
СЧ х о
v Д о к сЧ
»
zo
С(« в
4 (4
D (с« с
» о
Ю
Ф
С Ъ
С Ъ («О
«О
» о
С 4 л
»
СО
CO
In
О«
Ч:«
an
СЧ с
» ь
0« л с
44
Р» х о
O
1 о
Р»
Ф х
«ю (1
13 щ Е л е
1 еч
1 л о
Ф.
I л ееЪ
° 11
М сО
Ф е Ъ
Ое Ф
« ее л
« х м ееъ л л
М х е"Ъ
CCl ь. О е
М сеъ
M еО м
« х
М
CO м
Ф е«Ъ о
Ое л
О л
СаС
Ф аао л
Ф
М » еч л
М ее
Ю о
М
D ееъ
1 о х
z о
° Ф х
Я «»
«» еЕеЪ
1 с
И о
an
I о
1 ееЪ ! о ааа х
v д е г
g a .«Ъ О а ао еч о о
ФО ,«ФеГ
1»
Ое
° уе Ф а ее
° °
И6 Ъ а
41
CCI ч
«
«е
«е о е» х и о
М
\Ч е о х о е»
»
1.Ъ ее
\Ч
° » о х
v е»
° ° о
«с еО е о е е о
° ф, ею м о саС
D еЧ ееЪ ь
M щ х о
1Ъ1 . °
«е
1
1е и а9
Ch н
СЭ
l» ,и
Э
1»
I е о
Ъе и са н
Ccl
I е4
Y .
Ъ и
1» саС
Й
1 о
v
1 ее и .Е
1 о
Х
6 х
I фе ,И
ССа х
1 и
0
И о т х ч а1
Ф
Ф
Ю
Х
Ф
«е
Г 6
Я ф ъФ е еъ
Сас
«е о!
1!038б
« с.Ф о м.
° Ф
an
1
D в п
g .
Ц 11
° «
К Ъе
aca u
1 ааа
an 1»
-* 1
tC
)a ее и
tf
IC ILs
1 -
1 *.
I и g
ФЧ м л л
: О м л л о л л о л
Ы
1 с
Ф
1Ч оъ л
Ф м о\ л м
Ch л с о
Ф м ь
Ю .4 о
Ф м
Ю о м
Ф о
03 о
3 34 вй аь о о а
3м m ко со
° ф л
C)
CV
I м о .- Ч
C) л
in л
1 g!
1 °
1 Н
I
М
Ю "й ам м
СО Х Х о
Ю (V о л
4 g
С4 х о о
МЪ о х
4 о х о
Ъ1 х
I ф1 х х
1 !
Ъ 6 о о о х о н и
Ф
1ч сп
Оа м ж
v ф
° »
1 э э w ао
+ e а1-ао
-I
1110386!
1 О м
1 о о
I сч
W и в 1- о л
1, 1
A .И
Фе Ою м м х ж
u v ю О
М>
Ю н
О
МЪ м л
Ф иЪ
00 л н ,О о
CO м м
Ч0 О м
Ф л
О
МЪ л л
° 4
О и
Ф
00 Ф
О и
CaI
«4
О ф
Р
00 л ь л
Ф о
Ф л
Ф н ,О
М.
CV м О О а»
° еа ол а
Ф т
Й ю
Ф о л
an
Оъ
О
an
4Ч л
%.о 00 л
Ф о
00 л
an
00 л
Ф л
CO л о 3
Ъ.Ф о
Оъ л
М
Ж"
Ф о
О
СЭ
Ф
D о
СЧ м о ь
° .ф м ь
00 л о о ° м ь о
° ° о
an м
<Л
I
I ь л
Ф«
1 ф ч
° ч о
«С
Р4 ю ln о
D л о
an о
CV сЧ
Ф ь
Ф ь .
° О
Ю о
CV
Ф ь м
Ю
Ю ь м
Ф ь.Ф
Р
CO л ь О м о о
СЧ
ФЧ
CV о
IK о
«М . М и и
4l фч
CA и
Ф
f4
LI
k)l
С1.К 1 З,0
СЗ О.
С0
Ъ цр р Ф
В З К0 с «
°, ч ф
et
34
5 е
1!10386 о ю
О R О а
00 О м
«» CV
Ф Ф3
I I
° Й 0
М Фа и и
4l O н
М, 00 О
00, О
СЧ
О а (Ь о о о
1О М М о о о U
Ф 1
5 СЧ СЧ ь о
CV 00
6 00 о о
6 6 5 В и и
0I н
О Cll
19 и
C)
1«, I
1 Ф
° л
C) Ф л л
«Ф
Ch
Ю» ь
О1 л ь
00 ф« ь
C) ii м
< 1
О1
СЧ ф.е 1! (ь
1 ь О
4ь ь м
ЪФ ь
Х ь
\tl ь
1 t»
1
1
1 I !
Я вЂ” -
1 03 I
P I
1
> I
O 1 Х
4 о
5 о е й
I М
1 1 1 0386
-И
8 о
6"
L 2 о о
О о о и
t4
6)
63
3С ь сР
6
Ф ь
Фс1
Я г
««
Я
1 1 10366
Таблица 4
Е
КСОЖН
Е
Я, СОМЫ О2П43 м-сРВ>1,, Т "мл -;я- Время> .! мг тура ". ; мин
Сульф»д (i) Сульфон ((з.) снес!2 мл
Реакция.Вьсод> ЦК: Ч,„„с о» сцсЕ»
> мг
Н ь -. 7
РВ !5-Н
30 190 3425> 1785, 1742, 1672
40 234 3400> 1790> 1745, !700
200 4 126 0
296 HMR: Ю г !» 2.33ВЭН, 2.88s3H
15, Таблица 5
ROOFS
ЕСОЯН
8 2 3 сн,осн, о
СООСЦИ2 (ис) Реакция
Сульфон ((Т) Снес!
ВВЧ (у2) Цефемовое соединение (Ш) Температура, с
Время, мин
Выход» HK: )>м»ес си мг
150 1 75 -20 40 16 3430, 1790, 1725» 1673
1 Ph !5-Н
2 Теиил qL-CH>!O 230 2, 5 В2 "30 .25 144 Э420, 1790, 1725, 1700
ЬВц - 1,5-диааобицинло(5»4,0)ундсц"-5-ен
Составитель З>Латыпова
Редактор С.Пекарь Техред А. Кикемезей Корректор С.Шекмар
Заказ 6111/46 Тираж-410 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д.4/5
Филиал ППП "Патент", г.Ужгород,ул.Проектная,4 442О Са43
СООСНРЬ2
2. Тенил »("CB O 300 2 200 0
3 Толил о>-СН10 200 l 5 140 0
СН2 ОСН !
С00СНГИ2 СН2ОСНЗ
C00eHPhZ