Способ получения сложных эфиров аповинкаминовой кислоты
Иллюстрации
Показать всеРеферат
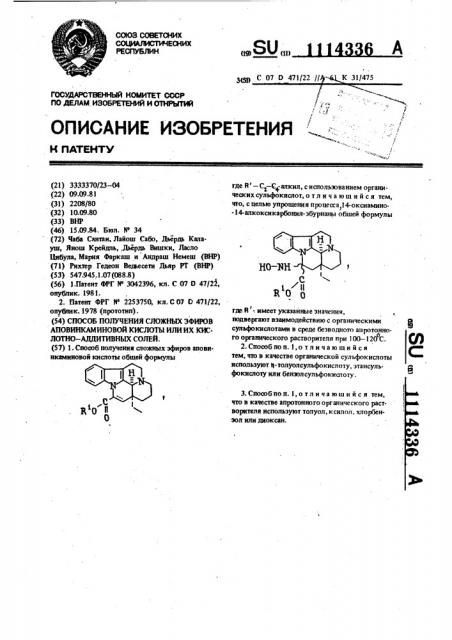
1. Способ получения сложных эфиров аповинкаминовой кислоты общей формулы где R - Cj-CvariKHn, с использованием органических сульфокислот,отличающийся тем, что, с целью упрощения процесса 14-оксиамиио-14-алкоксикарбонил-эбурнаны обшей формулы где R % имеет указанные значения,, подвергают взаимодействию с органическими сульфокислотами в среде безводною анротонноО ) го oi tiHH4ecKoro растворителя при 100-120 С. 2.Способ по п. 1,отличающийся тем, что в качестве органической сульфокислоты используют ц-толуолсульфокислоту, этансульфокислоту или бензол сульфокислоту. 3.Способ по п. 1, отличающийся тем, что в качестве апротонного органического растворителя используют толуол, ксилол, хлорбен4ib зол или диоксан. :о со сь
СОЮЗ СОВЕТСНИХ
РЕСПУЬЛИН (1cn (П) ЗСЮ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР /
flO ДЕЛАМ, ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ :..с
ОПИСАНИЕ ИЗОБРЕТЕНИЯ к пдп=нту
Н0
Я 0 0
С
3 О
0 (21) 3333370/23 — 04 (22) 09.09.81 (31) 2208/80 (32) 10.09.80 (33) ВНР (46) 15.09.84. Бюл. Н 34 (72) Чаба Сантаи, Лайош Сабо, Дьердь Капауш, Янош Крейдль,,Дьердь Вишки, Ласло
Цибула, Мария Фаркаш и Андраш Немеш (ВНР) (71) Рихтер Гедеон Ведьесети Дьяр Fl (ВНР) (53) 547 945.1.07 (088.8) (56) 1.Патент ФРГ 1! 3042396, кл. С 07 О 47/22, опублик. 198! .
2. Патент ФРГ и 2253750, кл. С07 О 471/22, опубли к. 1978 (прототип) . (54) СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ
АПОВИНКАМИНОВОЙ КИСЛОТЫ ИЛИ ИХ КИСЛОТНΠ— АДДИТИВНЫХ СОЛЕЙ. (57) 1. Способ получения сложных эфиров аповиикаминовой кислоты общей формулы где R — С вЂ” С алкил, с использованием органических сульфокислот, о т л и ч а ю щ н и с я тем, что, с целью упрощения процесса 14-оксиамнноf
-14-апкоксикарбонил-збурнаны обшей формулы
1 где Й -. имеет указанные значения, подвергают взаимодействию с органическими сульфокислотами в среде безводного ап ротонного органического растворителя при 100 — 120 С. о
2. Способ по п. 1, отличающийся тем, что в качестве органической сульфокислоты используют В-толуолсульфокнсл оту, эта нсульфокислоту или бензол сульфокислоту.
3. Способ по п. 1, о т л н ч а ю ш и и с я тем, что в качестве апротонного органического растворителя используют толуол, ксилол. хлорбенэол или диоксан.
1 1114336
Изобретение относится к усовершенствованному способу получения сложных эфиров .аповинкамнновой кислоты общей формулы
40 в о где R — алкильная группа с 2-4 атомами углерода, являющихся ценными фармакологически активными соединениями.
Известен способ получения сложных эфиров аповинкаминовой кислоты общей формулы (1) t5 путем взаимодействия соответствующего 11-галоидзамещенного 14-оксо-15-оксиимино-Зф, E7g -Е-гомоэбурнана в присутствии дегидратируюшнх кислот, преимущественно концентрированной серной кислоты, с соответствующим желательному эфиру спиртом. Выход 60—
80 o (11 °
Однако при необходимой температуре реак ции 100 — 104 С при воздействии используемой дегндратирующей кислоты присутствую- э5 щий спирт превращается в значительней сте. пени в соответствующий простой эфир, что .особенно нежелательно при крупнопромышленном осуществлении способа
Кроме того, продукт, получаемьш указан- 30 ным способом, имеет также недостаточно высокую чистоту.
Наиболее близким к предлгагаемому явля ется способ получения сложных эфиров аповинкаминовой кислоты общей формулы (E) из виникаминовой кислоты, получаемой путем гидролиза ввнкамнна, переводом ее в соответствующий сложный эфир, который далее превращается в сложный зфнр аповинкамнновой кислоты путем дегидратацки с помощью концентрированной серной или этансульфокислоты. Выход целевых продуктов до 75% (21.
Недостатками способа являются необходимость сначала получать вннкамин путем многостадийного (5 стадий) синтеза, а также
45 низкие выходы и недостаточно высокая чистота целевого продукта.
Цель изобретения — разработка более простого способа получения сложных эфиров аповинкаминовой кислоты с высоким выходом целевого продукта.
Цель достигается тем, что согласно способу получения сложных эфиров аповинкаминовой кислоты общей формулы (1), с иснользованием органических сульфокнслот, отличитель- 55 ной особенностью которого является то, что
14-оксиамнно-14-алкоксикарбоннл-эбурнаны общей формулы (ss) С
1 -ll
О
Ъ где и — имеет указанные значения, подвергают взаимодействию с органическими сульфокнслотами в среде безводного апротонного органического растворителя при 100—
120 С.
В качестве органической сульфокислоты в процессе предпочтительно . используют 11 -толуолсульфокислоту, этансульфокислоту или бензолсульфокислоту,. а в качестве апротонного органического растворителя — толуол, ксилол, хлорбензол или диоксан.
Исходные соединения общей формулы (11) могут получаться из соответствующих гексагидроиндоло- хинолиэиниевых соединений путем взаимодействия с диэфирами метиленмалоноой кислоты.
Согласно изобретению можно получать как рацемические, так, и также оптически активные соединения общей. формулы (1) в зависимости от того, используются ли рацемнческие нли оптически активные исходные соединения общей формулы (11).
Предлагаемый способ обладает важным преимуществом по сравнению с известными способами в том, что в нем исходят из легко доступных и просто обрабатываемых соединений и применяются меньше вызывающие коррозию, реактивы, желательные эфиры аповинкаминовой кислоты общей формулы (1) получают путем лишенного побочных реакций. превращения, при щадящих условиях, хорошей чистоты и с высокими выходами, нри этом сокращается число стадии с 8 до 4.
В случае особенно предпочтительного варианта осуществления предлагаемого способа, соот- ветствующее соединение общей формулы (11) нли его соль присоединения кислоты, в особенности его гидрохлорнд, в безводном толуоле кипятят 1-2 ч с также безводной г1 -то-, луолсульфокисло той.
Пример 1. 70 r (0,1 моль)! — /-1e .
- (метоксикарбонилэтнл) 1 g-этил-1,2,3,4,6,7,12, 12 в -октагидроиндоло(2,3-a)-хннолизш -0-дибензоилтартрата суспендируют в 300 .мл толуола; Суспеизию смешивают с 70 мл концентрированного водного раствора гидроокиси аммония и смесь перемешивают в течение
10 мин при комнатной температуре. Затем толуольную фазу отделяют, обезвоживают путем азеотропной перегонки и затем обьем смеси дополняют толуолом до 300 мл. Толу3 1114336 . 4 ольный раствор смешивают с 36 мл (31 г) роокисн аммония и 2 г целита. Перемешитрат -бутилнитрита и 25 г трет -бутилата вают при +10 С в течение 5 мин и отфильто натрия и смесь перемешивают в атмосфере - ровывают. Фазы филь|рата разделяют, водную азота в течение.25 мин при 30 С.,Реакцион- фазу экстрагируют 50 мл толуола и толуольную смесь потом смешивают с 300 мл эта- 5 ные фазы объединяют, промывают 50 мл воды иола и перемешивают при 60 С в течение и сушат над 20 г безводного сульфата нато часа. После этого смесь подкисляют 36 0-ной рия, После отфильтровывания фильтрат Выводнои солянон кислотой до рН-2, охлаждают паривают в вакууме досуха, остаток смешивадо О С и выпавший в осадок продукт от- ют с 40 мл этанола. Полученный раствор фильтровывают при этой же температуре и ð кипятят в теченйе 1 мин, затем охлаждают промывают дважды по 100 мл водой. Полу- до О С. и оставляют стоять в течение часа ченный таким образом продукт сушат на воз- при этой температуре. Выпавший в осадок духе и высушенный продукт затем обрабаты- продукт отфильтровывают, промывают по вают 100 мл 10%-ного водного раствора гид- 20 мл охлажденного до 0 С этанола и высуроокиси аммония, отфильтровывают, лромыва- 15 шивают ют трижды но 50 мл водой и высушивают. Таким образом получают 30 r этилового
Получают таким образом 20 г / — /-14-этокси- эфира /+/-аповинкаминовой кислоты (86% от карбонил-14-оксиамино.ЗМ, 36Ì -эбурнана (геории); т. пл. 144 — 146 C; (g, ) = 141 (52% от теории); т; пл. 172 — 173 С; (К)0 = 146 (с = 1, в хлороформе). о. 7о — 114,1 (c = 1, в хлороформе). 20 Анализ для C>21375Ng0Z(won.вес. 35044).
Пример 2. 19 г (0,05 моль) / — /-14- Найдено,%: С 75,31; Й 7,42; N 7,90
-этоксикарбонил-14-оксиамино-3 6, 16й, -збур- Вычислено%: С 75,33; Н 7,45; N 7,99. нана (нолучен согласно примеру 1) и 19,8 г Пример 4. Работают описанным в (0,125 моль) безводной A -толуолсульфокисло- примере 3 образом, с тем отличием, что ты в 350 мл безводного толуола кипятят с 25 в качестве исходного вещества используют обратным холодильником в течение 1,5 ч. 38 г (0,1 моль) / — /-14-этоксикарбонил-14Реакционную смесь затем охлаждают до 20 С, -оксиамино-Зе, 14@ эбурнана смешивают с 200 мл воды и рН (значение Получают 31,5 г (90% от теории) этиловосмеси) устанавливают равным 9 с помощью при го эфира /+/-аповинкаминовой кислоты, т. пл. примерно 20 мл концентрированного водного 144 — 146 С; (К ) = 141 — 146 (с,.= 1, в
30 раствора гидроокиси аммония. Органическую хлороформе) . фазу отделяют и водную фазу экстрагируют ° Пример 5. Работают описанным в
50 мл толуола. Объединенные толуольные фа- примере 3 образом, с тем отличием, что зы сушат над безводным сульфатом натрия, вместо толуола применяют 400 мл беизола в отфильтровывают, фильтрат осветляют 1 г качестве растворителя. активного угля и снова отфильтровывают.. 35 Время реакции 12 ч.
Фильтрат выпаривают в вакууме досуха, оста- Таким образом получают 32,4 г этилового ток растворяют в 20 мл этанола. Этот раст- эфира /+/-аповинкаминовой кислоты c670 o о
У вор кипятят 1 мин и охлаждают до О С, от теории); т. пл. 141 — 145 C; (c, ) = 141наконец, вьпсристаллизовавшийся из охлажден . 144 (с 1, в хлороформе). ного раствора продукт отделяют и высушива40
Пример 6. Работают описанным в примере 3 образом, с тем отличием, что
Таким образом получают 16,6 г этилового вместо толуола используют 400 мл ксипола в эфира /+/-аповннкаминовой кислоты (95% от качестве растворителя. Реакция осуществляется теории); т. an. 3 44 — 145 С; (К) и =144,1 о 7о при 140 С, время реакции 30 мнн. о 145,1 (с = 1, в хлороформе). Чистота про0 45
Таким образом получают 30,5 г этилового дукта: 99,8 — 100,1% титруют в ледяной уксус- эфира /+/-аповинкаминовой кислоты (87,3% ной кислотезв присутствии индикатора крис- or теории); т. пл. 144 — 146 С; (м ) о 141таялического фиолетового. 146 С (с = 1, в хлороформе)., Пример 3. 47,5 г (0,25 моль) гид- Пример 7. Работают описанным в рата и -толуапсульфокислоты растворяют 50 примере 3 обрмом, с тем отличием, что в 400 мл толуола, раствор обезвоживают вместо толуола используют 400 мл хлорбенпутем азеотропной перегонки, смешивают с . зола в качестве растворителя. Реакция прово42 r (0,1 моль) / — /-14-этоксикарбонил-14-ок- дится цри 130 С, время реакции 40 мин. сиамино-Зф, 16п, -эбурнан-гидрохлорнда и ки- Таким образом получают 30,8 r этилового пятят с обратным холодильником в течение 55 эфира /+/-ановинкаминовой кислоты (88% от
2 ч при церемешивании. Реакционную смесь теории).
0 охлаждают до +10 С, смешивают со 100 мл Пример 8. Работают описанным воды, 30 мл 25 o-ного водного раствора гид-. :в прюаере 3 образом, с тем отличием, что
Составитель И. Федосеева
Техред Л. Мнкеш
Корректор В. Гирняк
Подписное
Редактор А. Гулько факаз 6648/47
Тираж 409
ВНИИПИ Государственного комитета СССР по делам изобретений н открьггий
113035, Москва, Ж-35, Раушская наб„д. 4/5 Филиал ППП "Патент", г. Ужгород, ул. Проектная, 4
S 1! 14336 вместо 47,5 г (0,25 моль) гидрата ll -толуолсульфокислоты используют 43 r (0,25 моль)
Дезводной ll -толуолсульфокислоты и в качесн ве растворителя вместо толуола применяют
400 мл диоксана. Реакция проводится прн 5
100 С, время реакции 16 ч.
Таким образом получают 180 г этилового афнра /о/-ановннкнннновой кналоааа (5/,й% от.теории); т. пл. 141 — 143 C; (® У е"
140 1430 (c 1 в хлороформе).. !О
Й р и м е р 9. Работают описанным в примере 3 образом, с тем отличием, что имев 47,5 г (0,25 моль) гидрата q -толуолсульфокислоты применяют 27,5 г (0,25 моль) этансульфокислоты.
Получают 30,0 r (86% от теории) этилового эфира /+j-аповннкаминовой кислоты; т.нл.
144 — 146 C.> feb ) 141 — 146о (с = 1, в хлороформе) .
Пример 10. Работают описанным в примере 3 образом, с тем отлиеем, что вместо 47,5 r (0,25 моль) иядрата !1 -толуолсульфокислоты используют 39,5 г (0,25 моль) бензолсульфокислоты.
Таким образом получают 30,5 r этилового эфира /+/-аповинкаминовой кислоты (87,5% от теории); т. пл. 144--146/тС; (el )т1= 144146о (с = 1, в хлороформе).
Предлагаемый способ позволяет получать сложные эфиры аповинкаминовои кислоты простым методом и с высокими выходами.