Способ инверсионного электрохимического определения вольфрамат-ионов
Иллюстрации
Показать всеРеферат
СПОСОБ ИНВЕРСИОННОГО ЭЛЕКТРОХИМИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВОЛЬФРАМАТ-ИОНОВ путем концентрирования их на электроде в виде поверхностных соединений с материалом электрода и последующей регистрацией катодных кривых восстановления этих соединений, отличающийся тем, что, с целью одновременного определения вольфрамати молибдат-ионов, эти ионы концентрируют на ртутном электроде на фоне индифферентного электролита 0,050 ,10 М раствора нитрата или сульфата калия при рН раствора 5,0-5,5 в области потенциалов 0,28-0,35 В с последующей регистрацией катодных двухступенчатых хронопотенциограмм при плотности тока 3-3,5 мкА/мм и (Л по значениям переходных времен определяют концентрации молибдати вольфрамат-ионов. 0,05 О.Ю 0.15 Q 0,05 0.10 0,15 0,20 t,C ФигЛ
СОЮЗ СОВЕТСКИХ И Р
РЕСПИЬЛИК
3сбн G 01 N 27/48
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
И АВТОРСИОМЪ(СЮЗДЕТЕЛЬСТВУ
V,В
005
0,35
0,05 0,10 0,5 0 Ц05 ОЛО 0,5 0,20 t, с
Фиг.1
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 3621377/18-25 (22) 15.07.83 (46) 23.10.84. Бюл. У 39 (72) Т.E Иванова, В.И. Баканов и М.С. Захаров (7 1) Тюменский индустриальный институт им. Ленинского комсомола (53) 543.257(088.8) (56) 1. Эршлер А.В. Гальваностатические методы в исследованиях механизмов электрохимических реакций.
В сб. Электросинтеэ и биоэлектрохимия. Прогресс электрохимии органических соединений. M., "Наука", 1975, с. 199-25 1.
2. Брайнина Х.3. Инверсионная вольтамперометрия твердых фаз. N., "Химия", 1972, с. 45 (прототип). (54)(57) СПОСОБ ИНВЕРСИОННОГО
ЭЛЕКТРОХИМИЧЕСКОГО ОПРЕДЕЛЕНИЯ
ВОЛЬФРАМАТ-ИОНОВ путем концентрирования их на электроде в виде поверхностных соединений с материалом электрода и последующей регистрацией катодных кривых восстановления этих соединений, о т л и ч а ю— шийся тем, что, с целью одновременного определения вольфрамати молибдат-ионов, эти ионы концентрируют на ртутном электроде на фоне индифферентного электролита 0,050,10 И раствора нитрата или сульфата калия при рН раствора 5 0-5,5 в области потенциалов 0,28-0,35 В с последующей регистрацией катодных двухступенчатых хронопотенциограмм при плотности тока 3-3,5 мкА/мм и
2 пс значениям переходных времен определяют концентрации молибдат- и .вольфрамат-ионов.
1 1 I
Изобретение относится к аналитической химии, в частности к вольтамперометрическим способам определения анионов в водных растворах.
Известна совместная адсорбция двух компонентов раствора на ртутном электроде в случае различия в энергиях адсорбции этих компонентов, позволяющая при регистрации электродного процесса в гальваностатическом режиме получить хронопотенциограмму с двумя задержками потенциала, отвечающими электрохимической реакции в адсорбционном слое с участием первого и второго компонентов в растворе (1) .
Однако эта закономерность не реа" лиэована для определения вольфрамати молибдат-ионов при совместном их присутствии в растворе.
Наиболее близким гехническим решением к изобретению является способ инверсионногоэлектрохимического определения вольфрамат-ионов путем концентрирования их на электроде в виде поверхностных соединений с материалом электрода и последующей регистрацией катодных токов восстановления этих соединений.
Сущность известного способа заключается в определении вольфраматионов в отсутствие молибдат-ноно, основанном на анодном электроосаждении на ртутном электроде с последующим катодным восстановлением малорастворимой соли в режиме линейно меняющегося потенциала f2) .
Недостатками известного способа являются мешающее влияние молибдатионов при определении в их присутствии вольфрамат-ионов, мешающее влияние вольфрамат-ионов при определении в их присутствии молибдат †ион, невозможность раздельного определения содержания обоих анионов при совместном нх присутствии в растворе, Цель изобретения — одновременное определение вольфрамат- и молибдатионов.
Поставленная цель достигается тем, что согласно способу инверсионного электрохимического определения вольфрамат-ионов путем концентрирования их иа электроде в виде поверхностных соединений с материалом электрода и последующей регист20233 2 рацией катодных кривых восстановления этих соединений, эти ионы койцентрируют на ртутном электроде на фоне индифферентного электролита
0,05-0,10 М раствора нитрата или сульфата калия при рН раствора 5,05,5 в области потенциалов 0,280,35 8 с посдедующей регистрацией катодных двухступенчатых хронопотенциограмм при плотности тока
3-3,5 мкА/мм и по значениям переходных времен определяют концентрации молибдат- и вольфрамат-ионов.
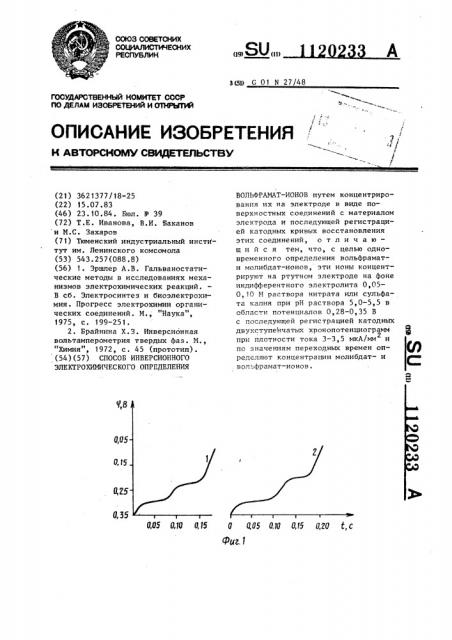
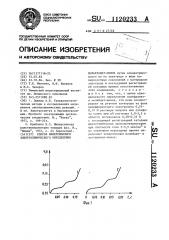
На фиг. 1 представлена катодная кривая на фиг. 2 — калибровочный график.
Для определения указанных авионов предложено проводить накопление иэ раствора на поверхности ртутного пленочного электрода при постоянном потенциале, достаточном для хемо.сорбции только вольфрамат-ионов (0,26-0,28 А на с.к.э.) с образованием соединения Ня ИО4 на поверхнос2 ти электрода. с последующей регистрацией гальваностатической кривой электрорастворения вольфрамата ртути. Потенциал накопления анионов подбирается опытным путем. При потенциале менее 0,26 В не происходит заметной адсорбции ИО, а тем бо2лее МоО -ионов. При потенциале бо 2лее 0,28 В кроме адсорбции VO -ионов начинается адсорбция Мо0,1-ионов, что нежелательно. Поэтому оптимальный диапазон потенциалов адсорбцни ИО,; -ионов 0,26-0,28 В.
Величина переходного времени гальваностатических кривых пропорциональна содержанию вольфрамат-ионов в растворе. Содержание молибдат-ионов в растворе 10 — 10 при этом не сказывается на определении вольфрамат-ионов, При постоянном потенциале, достаточном для электрохемосорбции обоих ионов 0,33-0 35 В производится совместное накопление на поверхности электрода поверхностных соединений Ня ЫО1 и Не No04 с последующей регйстрацией катодных хронопотенциограмм их электрорастворения. Потенциалы накопления ниже
0,-3 В нецелесообразны ввиду малой
7величины адсорбции МоО +ионов, при потенциалах выше 0,35 8 становится возможна элекрокристаллиза à осадков, что искажает катодные з 1 хронопотенциограммы. Поэтому для анализа рекомендуется диапазон
0,33-0,35 В. Катодные гальваностатические кривые при этом имеют два переходных времени. Первая задержка потенцйала (по ходу кривой) соответствует восстановлению молибдата ртути и регистрируется в диапазоне потенциалов 0,28-0,30 В. л
Величина переходного времени (, соответствующего восстановлению
Hg
В качестве фонового электролита могут быть использованы растворы нитрата или сульфата натрия или калия при концентрации 0,05-0,1 M u рН 5-5,5. Меньшая концентрация фонового электролита и выход за указанные пределы рН нецелесообразны, так как это приводит к увеличению сопротивления электролита. Концентрация более 0,1 М ведет к неоправданному увеличению расхода реактивов, поэтому оптимальной концентрацией фонового электролита является
0,05-0, 1 M.
Катодная гальваностатическая кривая регистрируется при постоянной плотности тока, равной 33,5 мкА/мм, Выбранные величины плотностей токов дают наиболее оптимальные переходные времена катодных хронопотенциограмм, достаточно чувствительные к изменению концентра". ции определяемого вещества.
Для определения анионов предлагаемым способом может быть использована обычная хрбнопотенциометрическая установка с осциллографической регистрацией хронопотен щограмм.
Пример . Определение вольфрамат- и молибдат-ионов проводятся в растворе нитрата калия с содержанием WO -ионов 5 10 M и МоО
Ф Ф ионов 1 10 М. Концентрация нит" рата калия 0,1 М, рН 5,2.
Навеску препарата растворяют в
100 мл дважды дистиллированной врды, переносят раствор в электрохимическуЬ ячейку и деаэрируют током инертного газа. Отполированный торец серебряной проволоки, впаянной в стеклянный или тефлоновый держа120233 l0
55 тепь, смачивают чистой ртутью для образования ртутной пленки произвольной толщины. Электрод споласкивают затем 1 н. серной кислотой и тщательно промывают большим количеством дистиллированной воды. Приготовленный таким образом электрод переносят в ячейку и определение анионов ведут следующим способом.
Электрод выдерживают при э=
= 0,28 В в течение 10 мин и затем регистрируют катодную гальваностатическую кривую электрорастворения
Hg 2WO4 при плотности тока 3 мкА/мм
Величйна переходного времени g -t кривой пропорциональна содержанию
2WO -ионов. Определив по калибровоч4 ному графику (фиг. 2) содержание вольфрамат-ионов, не разделяя пробу и не проводя каких-либо подготовительных операций, проводят далее электролиз при э = 0,35 В в течение 13,5 мин, после чего регистрируют катодную гальваностатическую кривую электрорастворения смешанного осадка Н8 Мо04 и Hg2WO4 . На катодной g -t кривой регйстрируются две задержки потенциала: первая по ходу кривой соответствует растворению Hg2No04, вторая — растворению
Нд, ИО1 (фиг. 1). Зависимость длины
2 первой задержки от С® -- при постоянной С>>2- является линейной. !
Содержание молибдат-ионов в пробе при установленной концентрации
МО4 -ионов определяют по градуиро2 вочному графику.
Варьирование времени предэлектролиза позволяет подбирать конкретные условия определения вольфрамати молибдат-ионов в качестве примесей.
Предлагаемый способ позволяет
-6 определить при С = 0,28 В 2 10
i0 М WO4 -ионов в присутствии
Ио04 -ионов 2 10 — 10 затем при = 0,35 В содержание молибдатионов в указанных пределах концентрации в присутствии 2 10 — 10 вольфрамат-ионов.
Предлагаемый способ определения вольфрамат- и молибдат-ионов не требует разделения анионов в смеси и каких-либо других .подготовитель4 ный операций по устранению их взаимного влияния.
Перимуществом предлагаемого спо-; соба является возможность определения каждого аниона в смеси, наличи .
ЩО С Ю м
5,0
Фиг,2
7,5
Составитель И. Рогаль
Техред А,Ьабинед Корректор М. Леонтюк
Редактор А. Козориз
Заказ 7731/3 I Тираж 822 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент", r Ужгород, ул. Проектная, 4 хорошей разрешающей способности . и воспроизводимости,.Он чуветвите+ лен, прост и может быть использован в анализе чистых реактивов и препа1120233 е ратов, содержащих вольфрамат- и молибдат-ионы в качестве примесей.
Относительная ошибка определения не .превышает SX.