Способ получения производных пиразолина
Иллюстрации
Показать всеРеферат
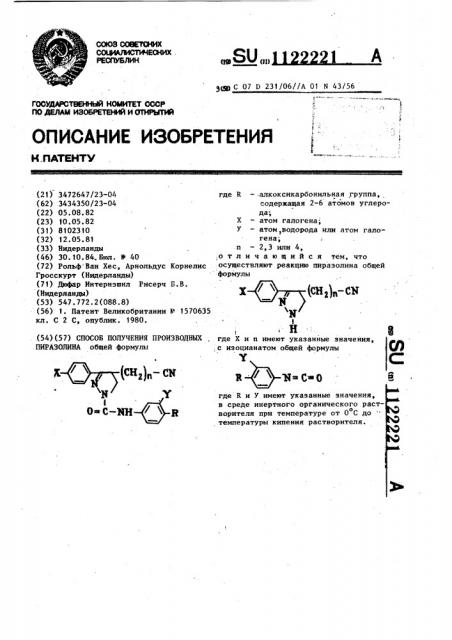
СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ . ПИРАЗОШНА общей формулы где R - алкоксикарбонильная группа, содержащая 2-6 атомов углерода , X У атом галогена; атом,водорода или атом галогена i п - 2,3 или 4, отличающийся тем, что осуществляют реакцию пираэолина общей формулы (CH2)n-CN где X и п имеют указанные значения, ;с изоцианатом общей формулы ( СК где R и У имеют указанные значения, в среде инертного органического растворителя при температуре от О С до температуры кипения растворителя.
СОЮЗ СОЕГСНИХ
СВНЦ Р
PECfMiËÈН,.S< m>
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТНРЫТЮ
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н. ПАТЕНТУ (сн21.-сн (сн,)„- ск
R МСО
0-* С-)ЯК (21) 3472647/23-04 (62) 3434350/23-04 (22) 05.08.82 (23) 10.05.82 (31) 8102310 (32) 12. 05. 81 (33) Нидерланды (46) 30. 10. 84„Бюл. Ф 40 (72) Рольф Ван Хес, Арнольдус Корнелис
Гросскурт (Нидерланды) (71) Дюфар Интернэшнл Рисерч Б.В. (Нидерланды) (53) 547.772.2(088.8) (56) t. Патент Великобритании Р 1570635 кл. С 2 С, опублик. 1980...(54) (57) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
ПИРАЗОЛИНА общей формулы
3ЦР С 07 Р 231/06//А 01 N 43/56 где R— -: алкоксикарбонильная группа, содер:кащая 2-6 атомов углерода, Х вЂ” атом галогена
У вЂ” атом, водорода или атом галогена; и - 2,3 или 4, отличающийся тем, что осуществляют реакцию пираэолина общей формулы
И где Х и п имеют указанные значения, с изоцианатом общей формулы
Y где: R и У имеют укаэанные значения, в среде инертного органического расто ворителя при температуре от 0 С до температуры кипения растворителя.
1122221
Изобретение относится к способу получения новых производных пиразо- лина общей формулы
g 10 где R — алкоксикарбонильная группа, содержащая 2-6 атомов углерода;
Х - атом галогена;
I5
У вЂ” атом водорода или атом галогена; и - 2,3 или 4, обладающих инсектицидной активностью.
Известен способ получения про- . 20 изводных 1-замещенных карбамоилпиразолина-2 взаимодействием производных пиразолина-2 с замещенным изоцианатом(1 .
Целью изобретения является синтез новых производных пиразолина, обладающих инсектицидной активностью.
Поставленная цель достигается тем, что согласно способу получения производных пиразолина формулы ?, 30 осуществляют реакцию пиразолина общей формулы (сн,),-си
II где Х и и имеют указанные значения, с изоцианатом общей формулы 40 г где R и У имеют указанные значения, в среде инертного органического растворителя при температуре от 0 С до температуры кипения растворителя.
Пример 1. Получение 1-(4-изо-50 пропоксикарбонилфеннлкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолина.
Раствор из 125,3 г 4-нзопропоксикарбониланилина в 160 мл диок- Ы сана по каплям в течение 30 мин при
0-10 С добавляют к раствору 100 мл фосгена в 300 мл диоксана при перемешивании. Затем реакционную смесь перемешивают при 20 С в течение
30 мин и далее нагревают до кипения, растворитель отгоняют и остаток перегоняют при поникенном давлении.
Требуемый 4-изопропоксикарбонилфенилизоцианат получают с выходом 136,8 г, т.кип. 87-88 C/0,2 мм.
51,5 г полученного 4-изопропоксикарбонилфенилиэоцканата добавляют к раствору 61,9 г 3-(4-хлорфенил}-4-(3-цианопропил)-2-пиразолина в
450 мл диэтилового эфира при комнатной температуре. После перемешиваиия в течение 30 мин при комнатной температуре добавляют 50 мл петролейного эфира (40-60), после чего реакционную смесь перемешивают при комнатной температуре еще в течение 1 ч. Кристаллический осадок отсасывают, промывают петролейным эфиром (40-60) и сушат на воздухе.
Получают 95,0 г 1-(4-изопропокснкарбонилфенилкарбамоил)-3-(4-хлорФенил)-4-(3-циаиопропил)-2-пиразолина.
После перемешивания 10 r полученного продукта с 100 мп диэтнлового эфира полученный продукт имел
p ..пл. 109-1IÇ С, Аналогичным способом получали следующие соединения:
1-(4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(2-цианоэтил}-2-пиразолин, т.пл. 199ОС;
1-(4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфеннл)-4-(4-цианобутил)
-2-ниразолин, т.пп. 106 С, 1-(4-этоксикарбонилфенилкарбамоил)—
-3-(4-хлорфенил)-4-(2-цианоэтил)-2-ниразолин, т.пл. 171 С;
1-.(4-втор.бутоксикарбонилфенилкарбамдил)-3-(4-хлорфенил)-4-(2-цианоэтил)-2-пиразолин, т.пл. 195ОС, 1-(4-этоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин, т.пл. 110 С;
1-(3-хлор-4-изопропоксифеннлкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропнл)-2-пиразолин, т.пл. 140 С;
1-(4-втор.бутоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин, т.пл. 102 С;
1-(4-метоксикарбонилфеннлкарбамоип)-3-(4-хлорфенил)-4-(4-цианобутил)-3-пиразолнн, т.пл. 132 С; I-(3-хлор-4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-41! 22221 з
-(4-цианобутил)-2-пиразолин, т.пл.
108 С, 1-(4-втор.бутоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(4-цианобуткп)-2-пиразолин, т.пл. 106 С;
1-(3-хлор-4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(2-цианоэтил)-2-пиразолин, т. пп. 158 С;
1-(4-н-пропоксикарбонилфенилкар- 1О бамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин, т.пл. 164 С;
1-(4-н-бутоксикарбонилфенипкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин, т.пл. 182 С; 15
1-(4-метоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(цианопропил)-2-пиразолин, т.пл. 160 С.
Пример 2. Аналогично проводят взаимодействие 3-(4-хлорфенил)- 20
-4-(со-цианпропил)-2-пиразолина и
4-изопропил-оксикарбонил-фенилизоцианата при температуре кипения реакционной смеси в течение 10 мин.
Взаимодействие указанных реагентов 25 осуществляют также при О С в течение 2 ч.
В обоих случаях получают 1-(4-изопропил-карбонил-фенил-карбамоил)-3-(4-хлорфенил)-4-(со-цианпропил)- 30
-2-пиразолин с количественным выходом.
Соединение (1) — это 1-(4-изопропил-оксикарбонил-фенилкарбамоил)-3-(4-хлорфенил)-4-(3-цианпропил)-2-пиразолин.
Пример 3. 20 личинок
Aedesaegypti (личинки малярийного комара) обрабатывают водными суспензиями активных соединений, 40 имеющими различные концентрации. Эти суспензии выдерживают 10 дней при
25 С, в течение которых (период ино кубации) в качестве пищи для личинок используют водные суспензии порошкообразного черного хлеба и дрожжей, Через 10 дней определяют процент смертности, учитывая естественную смертность. Результаты этих экспериментов представлены в табл.1, где N в скобках указаны номера следующих соединений: (2) 1-(4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(2-цианоэтил)-2-пиразолин; 55 (3) 1-(4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(4-цианобутил)-2-пиразолин;
4 (4} 1-(4-зтоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(2-цианоэтнл) — 2-пиразолин-, (5) 1-(4-втор-бутоксикарбонилфенилкарбамоил)-3-(4-хлорфенип)-4-(2-цианоэтил)-2-пиразолин;
{6) 1-(4-этоксикарбонилфеннлкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин; (7) 1-(3-хлор-4-изопропоксифенилкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин; (8) 1-(4-втор.бутоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(3-цианопропил)-2-пиразолин; (9) 1-(4-метоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(4-цианобутил)-2-пиразолин, (10) 1-(3-хлор-4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(4-цианобутил)-2-пиразолнн; (11) 1-(4-втор.бутоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(4-цианобутил)-2-пиразолин; (12) 1-(3-хлор-4-изопропоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(2-цианоэтил)-2-пиразолин, (13) 1-(4-н-пропоксикарбонилфенилкарбамоил)-3-(4-хлорфенкл) †.4-(3-цианопропил)-2-пиразолин, I (14) 1-(4-н-бутоксикарбонилфенилкарб амоил) -3- (4-хлорфенил) -4- (3-цианопропил) -2-пиразолин, (15) 1-(4-метоксикарбонилфенилкарбамоил)-3-(4-хлорфенил)-4-(3 циано. пропил)-2-пиразолин.
Пример 4. Взрослые растения карликовой фасоли обыкновенной (PhaseoIus vuIgaris L), имеющие два хорошо сформированных листка, удаляли из почвы, после чего растения опрыскивали до стекания композиция-, ми, полученными согласно примеру 2, взятыми в различных концентрациях
После высушивания растений их помещали в прозрачные пластиковые цилиндры и затем инфицировали 5 личинками EpiEaehna varivestis (личинки мексиканского жука). Затем цилиндры накрывали бумагой и ватой и помещали на полки, причем продолжительность освещения составляла 18 ч, р темноты — 6 ч; температура при освещении составляла 24 С, относительная влажность (RH) 707; температура в темноте 19 С при %1 80 — 90X.
1122221 испытаний представлены в табл.2, где номера соединений соответствуют номерам табл.1.
Таблица 1
Через 6 дней определяли процент смертности личинок. Каждый эксперимент повторяли триады. Результаты этих
Концентрация активного соединения на 1 л, мг
Активное соединение
1 0,3 0,1 0,03 0,01 (2) (4) (6) + (8) (10) (12) (15) П р и м е ч а н и е: + означает 90-100Х смертности; означает ! 50-90Х смертности; — означает <50Х смертности.
1 Таблица 2
100
50-90
0-50
100
70, (2) 0-50
-3-(4-хлорфенил) -4-(3-цианопропил)-2-пиразолин
Известное соединение(7 7
1
50"90
90-100
90-100
50-90
0-50
90-100
90-100
90-100
90-100
1 122221
90-100
90-100
90-100
50-90
100
10
0"50
90-100
90-100
90-100
50-90
100
10
0-50
90-!00
90-100
90-100
90-100
10
0-50
100
90-100
50"90
10
0-50, 100
90-100
50-90
0-50
100
90-100
90-100
0-50
100
90-100
0-50
0-50
100
90-100
50-90
0-50
Продолжение табл. 2
Il22221
Продолжение табл.2
100
90-100
90-100
10
0-50 (12) 100
90-100
90-100
90-100
10
0-50 (13) :1 00
90-100
90-100
90-100
30!
0-50 (14) 100
90-100
90-100
90-100
90-100
0-50 (15) 100
90-100
50-90
50-90
10
0-50
Составитель Л. Якунина
Техред M.Íàäü, Корректор С.Шекмар
Редактор Н.Явыдкая
Заказ 8009/45
Тирам 409 Подписное
ВНИИПИ Государственного . комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Рауаская. наб., д. 4/5
Филиал ППП "Патент", г. Уагород, ул. Проектная, 4