Способ получения меркаптидов тетраалкиламмония
Иллюстрации
Показать всеРеферат
СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТИДОВ ТЕТРААЛКИЛАММОНИЯ общей,формулы ФЭ (R,N S Rg где R - С -С -алкил; R2 - С„С л-алкил, циклогексил, фенил, низший алкилфенил, фурфурил или пиридил, взаимодействием гидроксида тетраалкиламмония общей формулы (R, ) NOH, где RJ имеет указанные значения, с меркаптаном формулы RgSH, где Ro имеет указанные значения, в органическом растворителе в инертной атмосфере при 6-10 С с последующим упариваинем реакционной смеси, отличающийся тем, что, с целью повышения качества и расширения ассортимента целевых продуктов, в качестве органического растворителя используют бензол.
СОЮЗ СОВЕТСКИХ
СОЦИАлистических
РЕСПУБЛИК ае а»
4(51) ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
®e (»и,i,ì) s к, ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР по делАм изОБРетений и ОтйРцтий (21) 3597790/23-04 (22) 30.05.83 (46) 23.01.85. Был. 9 3 (72) И.А. Рыбакова, P.È. Шехтман и Е.Н. Прилежаева (71) Ордена Трудового Красного Знамени институт органической химии им. Н.Д. Зелинского (53) 547.269.07(088.8) (56) 1. Патент США 1Ф 3219699, кл. 260-567.6, опублик. 1965 (прототип). (54) (57) СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТИ ДОВ ТЕТРААЛКИЛАИИОНИЯ общей формулы где К» — С»-С4-алкил;
R2 — С2С»2 алкил цикл фенил, низший алкилфенил, фурфурил или пиридил, взаимодействием гидроксида тетраалкнламмония общей формулы (R )„ ЮН, где R» имеет указанные значения, с меркаптаном формулы
R2SH
Ф где К2 имеет указанные значения, в органическом растворителе в инерто ной атмосфере при 6-10 С с последующим упариваинем реакционной смеси, »ш отличающийся тем, что, с целью повьппения качества и расширения ассортимента целевых продуктов, в качестве органического растворителя используют бензол. В
1135
Изобретение относится к усовершенствованному способу получения меркаптидов тетраалкиламмония общей формулы
Юе ((Е,) Х) 8 Я р (1) где R1 — С -С4-алкил;
R — С -С„,- -алкил, циклогексил, 10
2 фенил, низший алкилфенил, фурфурил или пиридил, которые могут найти применение в качестве промежуточных продуктов в синтезе восстанавливающих агентов типа алюмогидридов татраалкиламмония и биологически активных веществ.
Известен способ получения тиофенолятов тетраалкиламмония общей формулы 20
R — М-R
3 1
25 где R — R — различные алкильные
4 радикалы;
Ar — арильный радикал, заключающийся во взаимодействии
30 ,гидроксида, галогенида или нитрата
I тетраалкиламмония с тиофенолом в среде инертного растворителя, такого как вода, алифатические спирты, алифатические кетоны или кислород- 35 содержащие растворители, включая эфиры, Процесс можно проводить в инертной атмосфере как при комнатной температуре, так и при температурах выше и ниже комнатной. По окончании реакции побочно образующиеся дисульфиды и полисульфиды отделяют фильтрованием, фильтрат упаривают в вакууме, о а продукт сушат при 50-80 С и пониженном давлении на эффективном масля-45 ном или ртутном вакуумном насосе. Выходы целевых продуктов близки к количественным (11 .
К недостаткам известного способа относятся низкое качество целевых 50 продуктов, так, тетраметиламмоний тиофЕноксид (где К1-R4 — метил; Ar— фенил) получают с т.п. 143-146 С изза того, что вследствие черезвычайно высокой нестабильности меркапти- 55 дов тетраалкиламмония их очистку необходимо проводить в условиях, полностью исключающих влагу и кислород
742 2 (а по известному способу процесс проводят или в присутствии воды, или кислородсодержащих растворителей). В случае несоблюдения этих условий вещества загрязняются продуктами окисления и гидролиза. Кроме того, способ характеризуется недостаточным ассортиментом получаемых целевых продуктов, Цель изобретения — повышение качества и расширение ассортимента целевых продуктов.
Поставленная цель достигается предлагаемым способом получения меркаптидов тетраалкиламмония общей формулы I; заключающимся в том, что гидроксид тетраалкиламмония формулы (R ) N0H, (II) где R имеет указанные значения, подвергают взаимодействию с меркаптаном формулы
R SH, (III) где R2 имеет указанные значения, в бензоле в качестве органического рас". чорителя в инертной атмосфере при 6-10 С с последующим упаривани6 о ем реакционной смеси при 50-55 С и давлении 10 — 10 торр.
Выходы целевых продуктов — 92,599,8%. Т.пл. соединения формулы Е где R — метил, R — фенил — 161—
164 С.
По предлагаемому способу получа ют ряд новых соединений формулы I, где R — циклогексил, фурфурил, пиридил и С2-С 2 -алкил.
Пример 1 (для сравнения) .
30 r 10%-ногo водного раствора (0,033 моль) тетраметиламмоний гидроксида под аргоном смешивают с
3,6 r (0,033 моль) тиофенола. Реакционную массу перемешивают до тех пор, пока тиофенол не растворится.
Небольшое количество образовавшегося фенилдисульфида удаляют фильтрацией. Фильтрат упаривают на роторном испарителе при 45 С. Затем продукт о сушат 24 ч под вакуумом 10 торр при 70 С. Получают 5,7 r соли, выb ход 94,2%, т,пл. 143-146 С (в предварительно вакуумированном и запаянном капиляре). ИК-спектр, см
:33оо (он).
Наидено, %. С 59,98; Н 10,16, N 7,82; S 12,09
С„й„, Ы
1135742
Вычислено, .: С 65,58; Н 9,29;
7,65; Я 17,48.
Пример 2 (для сравнения).
0,9 г (0,01 моль) тетраметиламмоний гидроксида под аргоном смешивают с 10 мл Н -бутилового спирта и 1,1 r (0,01 моль) тиофенола, Реакционную массу перемешивают 0,5 ч, затем упаривают на роторном испарителе при 45 С. Затем продукт сушато 10 о
24 ч под вакуумом 10 торр при 70 С.
Получают 1,65 r соли, выход 91,6, т.пл. 150-153 С (в запаянном капилляре) °
Найдено, %: С 64,7; Н 9,04;
$ 15,28; N 7,5.
Вычислено,,: С 65,58; Н 9,29;
S 17,48; N 7,65.
Пример 3. Получение тетраметиламмоний тиофеноксида. 20
0,015 моль (1,36 r) тетраметиламмоний гидроксида под аргоном смешивают с 10 мл бензола. Смесь охлаждают .до 6 С. Затем при перемешио вании прикапывают 0,015 моль-(1,70 г) 25 тиофенола, поддерживая температуру о реакционной массы .10 С. Через час эту массу упаривают на роторном испарителе при вакууме 10 мм рт.ст.
Белые кристаллы сушат 12 ч под вакуумом 1(Г торр при 50 С. Получают о
2,69 r соли, выход 97,8 . При проведении реакции при 10 С выход не изменяется. Т.пл. 161-164 С (в предвао рительно вакуумированном и запаянном капилляре).
Найдено, .: С 65,27; Н 9,25;
N 7,38; S 17.44.
С10Hqt NS
Вычислено, %: С 65,58; Н 9,29;
N 7,65; S 17,48 °
ИК-спектр показал отсутствие
-SH и -ОН полос поглощения.
Спектр ПМР (CD>OD, ГИДС, d,м.д. )
7,33 (2Н, СН кольца); 6,91 т (2Н СН кольца), 6,74 т (1Н, кольца), 2,98 с (12H, N(CH1) J .
Спектр " С:Ph:р-С 121,29; (О-С)
128,58; 134, 49; S-С: 150,78; (M-С)
NMeg . 55,97.
Пример 4. Получение тетраметнламмоний додецилмеркаптида.
0,015 моль (1,36 г) тетраметиламмоний гидроксида под аргоном смешиваот с 10 мл бензола. Смесь охлаждают до 60С, затем при перемешивании прикапывают 0,015 моль (3 г} додецилмеркаптана, так, чтобы температура о реакционной массы не превышала 10 С.
Через час гелеобразную массу упаривают на роторном испарителе при вакууме 10 мм рт.ст. Белые кристаллы сушат 12 ч под вакуумом 10 торр при
55оC. Получают 4,05 г соли, выход
98 8%. При проведении реакции при
10 С выход не изменяется. Т,пл. 146148 С.
Найдено, .: С 68,48; Н 13,96;
N 4,93; $ 11,92 °
C«H»NS
Вычислено, .: С 69,82; Н 13,45;
N 5,09; S 11,64.
ИК-спектр показал отсутствие -$Н и -ОН полос поглощения.
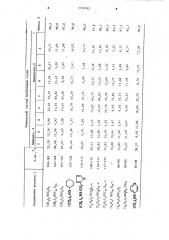
Характеристика остальных аналогично полученных меркаптидов тетраалкиламмония приведена в таблице.
Таким образом, предлагаемый способ позволяет получать как известные арилмеркаптиды тетраалкиламмония, так и впервые описанные алкил- и гетерилмеркаптиды тетраалкиламмония с выходом, близким количественному (97-99%}. Кроме того, при осуществлении предлагаемого способа упрощается процесс за счет исключения операции фильтрования, так как в отличие от известного способа побочное образование дисульфидов при использовании в качестве растворителя бензола не наблюдается и повьппается качество целевых продуктов.
1135742
Г
О
Г:4
О I л
iа I
О
l
С4 л О
О1
С4 л
Ch м л л л л
СЧ Г а\
Оi Ch Ch
С) л л
О1 сч л
СЧ Г л л л У 00
I и
1 л
1
1 л
Ми ,1 и 1
% О л л л л м л
CD (, Ь
CD л сГ) Ch
С) л
Ю л м
Ch 1
О1 00 л л м м
IO ХИ СД 01
gl ы 1 ggI Ж
1(у I 1 !
О
1 ц
I Й о ! х c0
1. .и 1
t л б" л м л л
С 4
Ch и л
СЧ
С) О л м и
Г л м
CD л
CO I
00 Ch а л л м ча
С 4
00 л
Ch О м м м
tl1
С)
ГГ л
СЧ
Щ л
С> л л
CO л
СЧ О а
ГГ
Г Л
О1 л л О м
CD л м
М г;;
CO л м
ID
С) о о б л л
Ch Ch л
С4 а
СЧ и
О л О о и
О 1
С> м а
Гг
О1 а м О
00 л
1 О О л л м м и
С 4 л
О1 о о а) И
С0
Ch л
С ч
00 4 л м
СГ
СЧ л м
ГГ1
Г
CO а (Г) 00
С) л л
00 0 л л и
Л Г
С 4
Г О о о л
0О б
Ф
1 I О
"О л О
С 4 О
ГГ) I
С>
С>
С) Г >
С>
СГ
Ch 00 О
1 1 1 1
О CD
СО 00 Ch н
О
О
Ве
У) л-4 3
Сс ж
04
С > х х х х
t(ю
1
Гл> !
О о
Я х 1
Э 1
04
Ц I
CrI ло
1 («I :
Ои
1 O
1 ! ж с4
СЛ
Р 5 Ф х о
00 00 00 СГ л л л л
00 Ch 0O
Ch Ch Ch Ch
g Ж
O D
С0 Q2
Х Я
СГ М и:иГ
Юф. о
СЛ сГ
СГ х
СГ о
Г
04 х .о
CQ
-4 о к
ССъ ж о са к з Ф
СГ- 0ы ж о о х о
l Ф
Ь
СЛ
Ф 4 х о
«Ф м
Ch л
00!
I л 1 (Г3 л
00 л