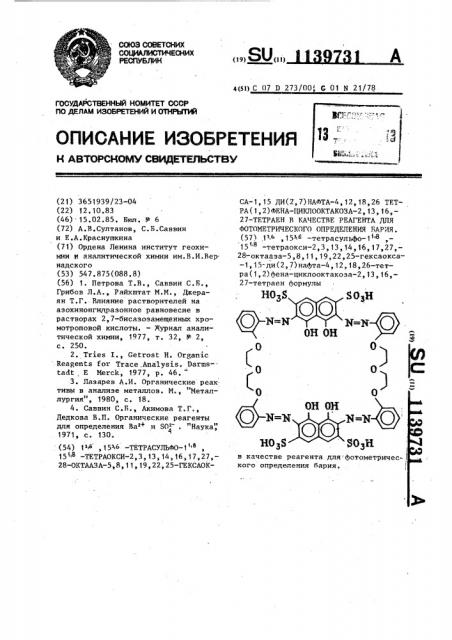
1 @ ,15 @ -тетрасульфо-1 @ ,15 @ -тетраокси-2,3,13,14,16,17, 27,28-октааза-5,8,11,19,22,25-гексаокса-1,15 ди(2,7)нафта-4, 12,18,26 тетра(1,2)фена-циклооктакоза-2,13,16,27-тетраен в качестве реагента для фотометрического определения бария
Иллюстрации
Показать всеРеферат
.Р.ь ,15з,е -тетрасульфо-1 8 , -тетраокси-2,3,13,14,16,17,27,28-октааза-5 ,8,11,19,22,25-гексаокса-1 ,15-ди
(19) (11) СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИН
ОПИСАНИЕ ИЗОБРЕТЕНИЯ и ABTGPCHGMY СВИДЕТЕЛЬСТВУ
ЗО Н
N=_#_
0Н ОН
:) p
ОН GH
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТНРЬГГИЙ (21) 3651939/23-04 (22) 12.10.83 (46) 15.02.85. Бюл. ¹ 6 (72) А.В.Султанов, С.Б.Саввин и Е.А.Краснушкина (71) Ордена Ленина институт геохимии и аналитической химии им.В.И.Вер. надского (53) 547.875(088.8) (56) 1. Петрова Т.В., Саввин С.Б., Грибов Л.А., Райхштат M.M. Джераян Т.Г. Влияние растворителей на азохинонгидразонное равновесие в растворах 2,7-бисазозамещенных хромотроповой кислоты. — Журнал аналитической химии, 1977, т. 32, ¹ 2, с. 250.
2. Tries I., Getrost Н. Organic
Reagents for Trace. Analysis. Darmstadt Е Merck, 1977, р. 46.
3 ° Лазарев А.И. Органические реак. тины в анализе металлов. M., "Металлургия", 1980, с. 18.
4. Саввин С.Б., Акимова Т.Г., Дедкова В.П. Органические реагенты для определения Ва2+ и SO, "Наука"
1971, с. 130.
: (54) 1 а, 15З -ТЕТРАСУЛЬФО-1 8
15 8 -ТЕТРАОКСИ-2,3, 13, 14, 16, 17,27,—
28-OKTAAÇA-5,8, 11, 19,22,25-ГЕКСАОК4(51) С ()7 D 273/00 6 01 N 21/78
СА-1, 1 5 ДИ (2, 7) HASTA-4, t 2, 18, 26 TF TРА(1, 2) ФЕНА-ЦИКЛООКТАКОЗА-2, 13, 16,—
27-ТЕТРАЕН В КАЧЕСТВЕ РЕАГЕНТА ДЛЯ
ФОТОМЕТРИЧЕСКИГО ОПРЕДЕЛЕНИЯ БАРИЯ. (57) 1 З,6, 15>S -тетрасулы о-1 6 тетраокси 2,3,13,14
28-октааза-5,8,11,19,22,25-гексаокса-1,15-ди(2,7)наАта-4,12,18,26-тетра(1,2)Лена-циклооктакоза-2, 13, 16,—
27-тетраен формулы в качестве реагента для фотометричес-) кого определения бария. I
1139731!
®з
ОН ОН
ОН 0Н
25 которое может быть использовано в качестве эффективного реагента для фотометрического определения малых количеств бария в технических и природных материалах.
Указанное соединение, его свойства и способ получения в литературе. не описаны.
Известен нециклический эфир 2,7-бисазозамещенной хромотроповой кислоты (11 фомулы
35
Сн О 40
OH ОН
И=И Ж=Ж,!1
8О,Н
НОз3
Однако он не дает цветной реакции с барием и не используется в аналитической химии.
Для фотометрического определения бария известен реагент аналогично го строения — производное 2,7-бисаэозамещенной хромотроповой кислоты — ортаниловый С (Ш). Этот реагент по литературным данным является лучшим для определения бария
$2(и $4) .
Изобретение относится к органической химии, в частности к синтезу нового химического соединения
1з 6, 15з ь -тетрасульфо-11, 15 .
-тетраокси-2, 3, 13, 14, 16, 17, 27, 28-октааза-5,8,11, 19,22,25-гексаокса-1,— 15 ди(2, 7)нафта-4, 12, 18, 26 тетра(1,—
2)фена-циклооктакоза-2,13,16,27-тетраен (гексаоксациклоазохром, ГОЦАХ) формулы
О Н
ОН OH
И=К
НО 3
PeaFeHT применяется только в водно-органических средах, поскольку в водной среде обладает невысокой чувствительностью, которая выража ется в низком значении молярного коэффициента погашения его комплекса с барием, равного 1, 12. 10 j4) .
Цель изобретения — синтез нового макроциклического эфира 2,7-бисазозамещенной хромотроповой кислоты с улучшенными аналитическими свойствами.
Поставленная цель достигается описываемым 1з, 15з 6 -тетрасульфо-1, 15 "8 -тетраокси-2, 3, 13, 14, 16,.
17,27,28-октааза-5,8, 11, 19,22,?5-гексаокса-1, 15 ди(?,7)нафта-4, 12,—
18,26-тетра(1,2)фена-циклооктакоза-2, 13, 16,27-тетраеном формулы 1 в качестве реагента для фотометрического определения бария.
Предлагаемое соединение получают азосочетанием диазотированного бис(2-аминофенилового) эфира диэтиленгликоля с хромотроповой кислотой в щелочной среде, создаваемой гидроокисью лития.
Указанное соединение взаимодействует в нейтральной и кислой средах с ионом бария и может применяться для его определения.
ГОЦАХ получают следующим образом.
Диаэотирование. 0,3 r бис(2-аминофенилового) эфира диэтиленгликоля размешивают в 3 мл 2,5 M НС1, охлаждают до 0-5 С и диазотируют, вводя 0,5 мл раствора NaN02. Конец диазотирования устанавливают по иодокрахмальной бумажке.
Азосочетание. Азосочетание проводят, используя технику высокого pasбавления. К 400 мл раствора LiOH в
Нз0 с рН 10-11,5 медленно по каплям. одновременно из двух капельных воронок прибавляют раствор соли диазония, разбавленный водой до 50 мп, и раствор 0,4 r динатриевой соли хромотроповой кислоты в 50 мл Н,О.
Кислотность среды поддерживается на первоначальном уровне добавлением водного раствора гидроокиси лития.
39731 4 но без металла.. Оптическую плотностЬ растворов измеряют при длине волны
704 нм относительно раствора соединения.
|Контрастность реакции (а% =
= Ъ вЂ” ), т.е. расстояние макс" макс.
МФР в нм между максимумами поглощения комплекса и реагента, 1 OItAX с барием составляет 90 нм.
10 Рассчитанное значение молярного коэффициента погашения (6) комплексного соединения бария, которое является объективной характеристикой чувствительности реакции, равно
1,2 10
Таким образом, чувствительность реакции бария с ГОЦАХ по сравнению с чувствительностью реакции с ортаниловым С в водных растворах, в
20 молярных коэффициентах погашения, выше на порядок.
Селективность реакции ГОЦАХ с барием сопоставима с селективностью ортанилового С.
25 В таблице приведены важнейшие аналитические характеристики фотометрических реагентов на барий. маас
3heg з
Реагент аФ ее11 . нм
Элемент
Среда, рН
1 2 ° 10
2,4
ГОЦАХ
704.
Ва
Ор таниловый С
70 1, 12 ° 10
Ва
2,4
638
Составитель Т.Раевская
ТехредС.Легеза Корректор О.Билак
Редактор Н.Киштулинец
Тираж 384 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Заказ 219/18
Филиал ППП "Патент", г. Ужгород, ул. Проектная, 4
После прибавления растворов реакционную смесь перемешивают еще 2 ч при комнатной температуре, затем подкисляют конц. НС1, осадок отфильтро,вывают и промывают О, 1 М НС1 до почти бесцветных промывных вод.
Продукт очищают неоднократным переосаждением кислотой из щелочного раствора. Выход 0,42 г (30 ). К
0,32 (бутанол-пропанол — NH ag, 50:30:80 íà Silufol UV-254, УФ-спектр (в Н 0) . hloKcq (E):
615 нм (б 34 10 ) и Ъ | а с (Я}-
9.
670 нм (4,80 10 ) .
Найдено, .: С 43,87, Н 3,60, N 7,89, S 9,00
С дй а О Ng Я На
Вычислено, : С 43,95; Н 3,40, N 7,88, $ 9,02.
Указанные. аналитические данные подтверждают представленную формулу соединения.
Методика построения калибровочного графика для спектрометрического определения бария заключается в
|следующем °
В мерные колбы емкостью 25 мп вводят от 3 до 30 мкг Ва, 5 мл
0 1 М НС1 для создания рН 2,4, 5 мл водного раствора ГОЦАХ с концентрацией 10 M и доводят до метки дистиллированной водой. Раствор сравнения готовят в тех же условиях, Из таблицы видно, что предлагаемое соединение ГОЦАХ превосходит
t
|по чувствительности и контрастности реакции лучший Hs известных реагентов на барий — ортаниловый С.