Способ определения содержания лизоцима
Иллюстрации
Показать всеРеферат
СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ЛИЗОЦИМА путем инкубации биологической жидкости с клеточными стенками Micrococcus lysodeikticus, отличающийся тем, что, с целью ускорения способа повышения его чувствительности и точности, инкубацию проводят 10-15 мин при комнатной температуре, добавляют раствор 5-аминосалициловой кислоты и перекиси водорода, затем прибавляют раствор пероксидазы и спектрофотометрируют .
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (19) () ) ) А
4(51) С 12 1 00
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
О ЫТИЙ (21) 3591494/28-13 (22) 08.04.83 (46) 07.03.85. Бюл. Р 9 (72) А.М.Сухоруков, Т.П.Журавлева, В.С.Цветков и Э.Г.Щербакова (71) Центральный ордена Ленина институт усовершенствования врачей (53) 577.152.087.4(088.8) (56) 1. Каграманова К.А., Ермольева З.В. Сравнительная характеристика методов определения активности лизоцима. -"Антибиотики", 1966, ))- 10, с. 917-919 (прототип).
0гппииеслюя
nrtom o em
12ХО 021 112 166 7Ю 7У
0У
08
07
ОХ
ЦУ
02
01 (54)(57) СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ЛИЗОЦИМА путем инкубации биологической жидкости с клеточными стенками Hicrococcus lysodeikticus отличающийся тем, что, с целью ускорения способа повышения
его чувствительности и точности, инкубацию проводят 10-15 мин при комнатной температуре, добавляют раствор 5-аминосалициловой кислоты и перекиси водорода, затем прибавляют раствор пероксидазы и спектрофотометрируют.
4 1143
Изобретение относится к экспериментальной медицине и может быть использовано для определения содержания лизоцима в биологических жидкостях, тканях и молоке, в клини- S ческой и экспериментальной медицине, в медицинской и молочной промышленности.
Наиболее близким к изобретению по технической сущности и достигаемому результату является способ определения содержания лизоцима, который заключается в том, что субстрат клеточных стенок Micrococcus
1ysodeikticus добавляют к агару
"ВЫсо". Сыворотку или другую биологическую жидкость вносят в лунки агара. Чашки инкубируют в термостате при 37 С в течение 20 ч. Содержание лизоцима определяют путем сравнения диаметров зон лизиса субстрата исследуемыми образцами и стандартными растворами лизоцима. Концентрацию лизоцима вычисляют по стандартной полулогарифмической кривой. 25
Однако известный способ является длительным и трудоемким (требует приготовления агаровой среды с субстратом), мало чувствителен, так как зависит от диффузии лизоцима в агар, ЗО и частичного его связывания агаровым гелем. Кроме того, способ является недостаточно точным, так как полученные результаты оцениваются визуально путем измерения зон задержки
35 роста тест микроба.
Цель изобретения — ускорение способа, повышение его чувствительности и точности.
Поставленная цель достигается тем, что согласно способу определения содержания лизоцима путем инкубации биологической жидкости с клеточными стенками Micrococcus lysodeikticus, инкубацию проводят 10-15 мин при комнатной температуре, добавляют раствор 5-аминосалициловой кислоты и перекиси водорода, затем прибавляют раствор пероксидазы и спектрофотометрируют.
Способ осуществляется следующим образом.
Определение лизоцима в исследуемой биологической жидкости начинают с построения стандартной кривой. Для 55 этого лизоцим титруют в 0,5 мл физио- логического раствора начиная с 5000 до 38 нг/мл ° Из полученных разведе778 1 ний лизоцима отбирают по 0,1 мл и переносят в два параллельных ряда большого пластикового планшета для микроагглютинации. Взвесь стенок
Micrococcus lysodeikticus с концент- рацией 1 мг/мл готовят перед исследованием и после тщательного растирания в физиологическом растворе добавляют по 0,05 мл к разведениям лизоцима. Инкубацию проводят при комнатной температуре в течение
10-15 мин, после чего к реакционной смеси добавляют по 0,5 мл субстрата
/ на пероксидазу (0,087-ный раствор
5-аминосалициловой кислоты с 0,057ным раствором перекиси водорода (5-АС H O ) в соотношении 9:1) .
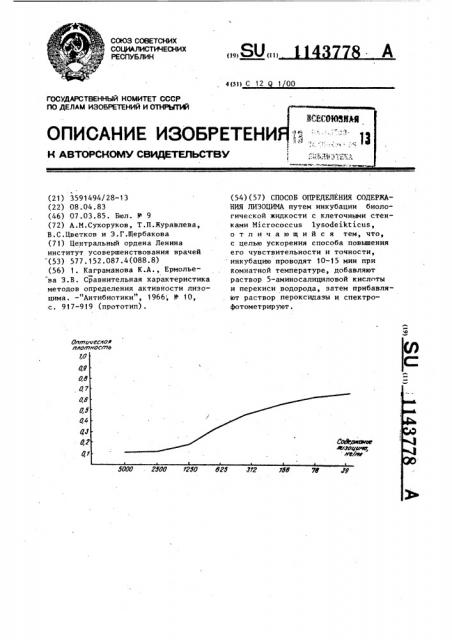
Через 2-3 мин инкубации к полученной смеси добавляют 0,05 мл 0,047-ного раствора пероксидазы. В контроле светложелтый раствор субстрата 5-АСх хН О после взаимодействия с пероксидазой через 15-20 мин становится темнокоричневого цвета. В процессе взаимодействия лизоцима с клеточными стенками ,icrococcus lysodeikticus выделяется продукт разрушения, который является конкурентным восстановителем перекиси водорода, входящей в другую фермент-субстратную систему (пероксида- за — 5-ACх Н20 ). В результате такого конкурентного восстановления перекиси водорода степень срабатывания второго субстрата (5-AC х Н О ) зависит от количества продуктов разрушения стенок Micrococcus lysodeikticus, которое пропорционально количеству определяемого лизоцима. По мере уменьшения концентрации лизоцима происходит нарастание интенсивности окрашивания конечных продуктов реакции, которые через 15-20 мин регистрируются спектрофотометрически при 450 нм. На основании полученных данных строят калибровочную стандартную кривую лизоцима, откладывая на оси абсцисс концентрацию лизоцима в нг/мл, а на оси ординат — оптическую плотность растворов.
На чертеже представлена калибровочная кривая.
Пример. Определение содержания лизоцима начинают с разведения сыворотки физиологическим раствором в соотношении 1: 10, В лунки пластикового планшета вносят по 0,1 мл разведенной сыворотки и добавляют по 0,05 мл взвеси тщательно растертых в физиологическом
Предлагаемый способ
Исследуемые образцы
Время
Содержание лизоцима, нг/мл
Содержание лизоцима, мкг/мл
Время проведения испытаний, ч проведения испытаний, мин
Сыворотка крови
45-60
5000
4,8
20-22
3150
3,0
1000
0,8
2600
2,5
4150
3,8
7,5
8000
1550
1,5
3150
3,0
9 лимфа
6250
6,0
4200
4,0
3 1143 растворе стенок Micrococcus 1.ysodeikticus в концентрации 1 мг/мл. После
10-15 мин инкубации при комнатной температуре к реакционной смеси добавляют 0,5 мл субстрата на пероксидазу: 0,08Х-ный раствор 5-АС с
0,05Х-ным раствором перекиси водорода в соотношении 9:1 и через 2-3 мин
0,05 мл 0,047.-ного раствора пероксидаэы. Интенсивность окрашивания 10 конечных продуктов через 15-20 мин измеряют спектрофотометрически при
450 нм. Концентрацию лизоцпма в сыворотке находят по стандартной кривой. Найденную концентрацию умножают на степень разведения и получают содержание лиэоцима в нг/мл.
Оптическая плотность исследуемой сыворотки равна 0,3. По стандартной ,кривой находят, что это соответству- 2р ет 830 нг/мл лизоцима. Полученную концентрацию умножают на разведение (10) и находят содержание лизоцима в испытуемой сыворотке, которое равно ,8300 нг/мл или 8,3 мкг/мл.
В таблице приведены результаты опытов по определению содержания лиэоцима в биологических жидкостях
778 4 и тканях предлагаемым способом и известным — методом диффузии в агар.
Результаты этих исследований показывают явное преимущество предлагаемого,способа по сравнению с известным. Об эффективности предлагаемого способа свидетельствует и его более высокая чувствительность, позволяющая выявить наличие лизоцима в образцах, которое базовым способом не улавливается.
Таким образом, предлагаемый способ является экспресс-методом, так как позволяет провести определение содержания лиэоцима в испытуемых образцах в течение 45-60 мин, в то время как известным способом — на протяжении 20-22 ч. Предлагаемый способ по сравнению с известным в 10-20 раз чувствительнее, так как позволяет определить содержание лиэоцима в нг/мл по сравнению с мкг/мл известным способом. Кроме того, предлагаемый способ позволяет проводить быструю и точную инструментальную оценку реакции, что особенно важно в практике клинико-диагностических лабораторий.
Метод диффузии в агар
1143778
Продолжение таблицы ю
Метод диффузии а агар
Предлагаемый способ
Исследуемые образцы
Гомогенаты органов
1 1500
45-60
9500
9,0
7250
7,0
6250
6,0
9350
9,9
Молоко
20-22
770
45-60
Следы
4700
4,0
11
6700
6,0
4 пастеризованное
560
Следы
5,0
5 нативное
5750
П р и м е ч а н и е Исследования проводят, используя сыворотки человека, животных и гомогенаты тканей животных.
Редактор Н.Яцола Техред А.Бабинец Корректор И.Эрдеи
Заказ 855/23 Тираж 525 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
11303S, Москва, Ж-35, Раушская наб., д.4/S
Филиал ППП "Патент", г.ужгород, ул.Проектная,4
1 пастеризованное
2 нативное
Содержание лизоцима, нгlмл
Время проведения испытаний, мин
Содержание лйзоцима, мкг/мл
Время проведения испытаний, ч