Способ получения растительного полимера-эпигалохина
Иллюстрации
Показать всеРеферат
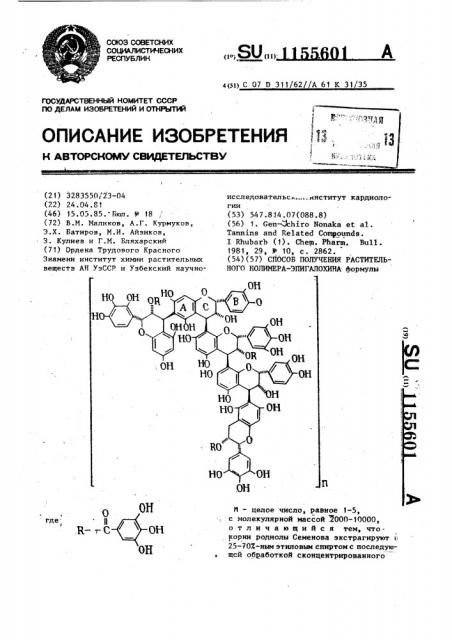
СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО ПОЛИМЕРА-ЭПИГАЛОХИНА формулы (Л ел :л з: гдеи - целое число, равное 1-5, с молекулярной массой 5000-10000, отличающийся тем, чтокорни родиолы Семенова экстрагируют А 25-70%-ным ЭТИЛОВЫМ спиртом с последующей обработкой сконцентрированного
СООЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИН (go) (ф g) 4(s)) С 07 0 311/62//A 61 К 31/35
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТНРЫТИЙ (P ",":;."ä÷,1 g
ОПИСАНИЕ ИЗОБРЕТЕНИЯ 1. "., ц
H ABTOPCHOMV СВИДЕТЕЛЬСТВУ
°
НО 0Н
ОН
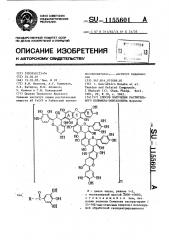
0 где. Il.R- C (21) 3283550/23-04 (22) 24.04.81 (46) 15.05.85. Бюл. М 18 (72) В.М. Маликов, А.Г. Куриуков, Э.Х. Батиров, М.И. Айзиков, 3. Кулиев и Г.М. Бляхарский (71) Ордена Трудового Красного
Знамени институт химии растительных веществ АН УЗССР и Узбекский научноисследовательс ...., институт кардиологии (53) 547.814 07(088.8) (56) 1. Gen hiro Nonaka et al.
Tannins and Related Cmnyounds.
I Rhubarb (1) . Chem. Pharm. Bull .
1981 29, Р 10, с. 2862. (54)(57) СЧОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО НОЛИИЕРА-ЭПИГАЛОХИНА формулы п — целое число, равное 1-5, с молекулярной массой 2000-10000, отличающийся тем, чтокорни родиолы Семенова экстрагируют
25-70Х-ным этиловым спиртом с последующей обработкой сконцентрированного!
1155601 экстракта этилацетатом, высушиванием, нзмельчением экстракта в порошок с последующей ечисткой его от низко.молекулярных примесей трехкратным кнпяченнием с этилацетатом и высушиванием полученного порошка при темпера-.
I о г туре 30-60 С н остаточном давлении
1-10 мм рт.ст. до постоянного веса. таоксифлаван: (-) -2, З-цис-(2К, 3R)—
-3, 4-транс-(3k, 4S) -3-0- галло-3, 4, 5,, 6, 7-пентаоксифлавана (эпигалохина), формулы
0Н
Изобретение относится к способу получения нового растительного полимера -(4,8), (4,6) (-)-2,3-цис-(2К,ЗЙ)-3, 4-транс- (3 Р, 4 Ь) -3, 3, 4, 5, 7-пе нОЯ
ll
30 где Я С ОИ
И вЂ” целое число,, равное 1-5, с молекулярной массой 2000-10000, который проявляет противогипоксическую активность и может найти применение в медицине.
Эпигалохин является высокомолекулярным катехином.
Известен способ получения поликате. хина-таннина экстракцией иэ корней ревеня ацетоном, затем экстракцией суммы таннинов из сырья метанолом и затем экстракцией из водно-метаноль ного экстракта этилацетатом, с последующим промыванием метанольного экстракта на хроматографической колонке с сеФадексом марки 4Н-20 последовательно водой,, смесьв этанола с водой (1: 1}, этанолом и смыванием с колонки метанолом. Выход целевого продукта 2,85Х от веса сырья 113.
Однако этот способ является много стадийиым, требует использования токсических растворителей: метанола и ацетона.
Целью изобретения является способ получения нового растительного полимера эпигалохина - ноликатеяииа, 3 11556 обладающего противогипоксической активностью.
Цель достигается тем, что согласно предлагаемому способу корни родиолы Семенова экстрагируют 25?YJX-ным этиловым спиртом с последующей обработкой сгущенного экстракта этилацетатом, высушиванием, измельчением экстракта в порошок с последующей очисткой его от низкомолеку- fo лярных примесей трехкратным кипячением с этилацетатом и сушкой полученного порошка при температуре
/ о
30-60 С и остаточном давлении
1-10 мм рт.ст. до постоянного веса.
Способ осуществляют следующим образом.
Воздушно-сухие измельченные корни родиолы Семенова при комнатной температуре экстрагируют 25-70Х-ным эти- щ ловым спиртом порциями, взятыми в соотношении к сырью 1:5-1:6 (весобъем) четыре- шестикратно, каждый раз по 12-24 ч. Затем концентрированные в ЗО раз упариванием в вакууЮ ме при 30-60 С объединенные экстракты пятикратно обрабатывают порциями этилацетатом, взятыми в соотношении к экстракту 1:0,4-1:1 (объем-объем) °
Этилацетатные фракции отделяют, очи- 30 щенный водно-спиртовый экстракт упаривают в вакууме при 30-60 С, остаток измельчают в порошок и повторно обрабатывают этилацетатом взятым в соотношении к порошку
1:1,5-1:3 (вес-объем), в колбе с об35 ратным холодильником на водяной бане в течение 15 мин при кипячении. После охлаждении и отстаивания этилацетатный раствор сливают. Обработку порошка этилацетатом повторяют 3 раза. Очищенный порошок высушивают о при 30-60 С и остаточном давлении
1-10 мм рт.ст. до постоянного веса.
Выход целевого продукта 5-15Х от веса воздушно-сухих корней, зависит от места сбора сырья и режима обработки (количества экстракции, крепости используемого для экстракции спирта). Полученный эпигалохин представляет собой аморфный порошок .,светло-коричневого цвета с характерным запахом, растворимый в воде, этаноле, метаноле, диметилформамиде, диметилсульфоксиде, разлагается . при 290-300 С L43 +40 (c
Э нол) .
При использовании для экстракции этилового спирта крепостью менее
257. наряду с эпигалохином извлекаются гидрофильные балластные вещества (моно- и полисахариды, минеральные соли и т.п.), что затрудняет очистку целевого продукта.
Экстракция сырья этиловым спиртом крепостью вьппе 707. приводит к ° значительному снижению выхода эпигалохина и увеличению содержания гидрофобных низкомолекулярных балластных веществ в экстракте.
Предпочтительно использовать этиловый спирт концентрации 30-40Х.
При получении целевого продукта эпигалохина упаривать и сушить ирак" тически возможно при любой температуре до 60 С. Температура в этих пределах практически не влияет на качество и количество получаемого целевого-продукта, а лишь ускоряет процессы упаривания и сушки. Длительное воздействие на препарат темпео ратурой более 60 С приводит к ухудшению фармакологического действия препарата. Остаточное давление определяется температурой сушки.
Пример 1. В. перколятор емкостью 20 л вносят 2000 г воздушносухих мелкоизмельченных корней родиолы Семенова и шестикратно экстрагируют при комнатной температуре смесью вода — этиловый спирт (25X по объему) порциями по 12, 10, 10, 10, 10, 10 л, каждой порцией в течение 24 ч. Полученные экстракты, хранящиеся в темноте при комнатной температуре, объединяют и упаривают в роторном испарителе под ваку." умом (при остаточном давлении
30 мм рт.ст., который обеспечивается водоструйным насосом) при 40-50 С
4 до 2 л. Сгущенный экстракт обрабатывают этилацетатом (5 раз но
500 мл}. Этилацетатные фракции выбрасывают. Экстракт упаривают на водяной бане в фарфоровых чашках. Остаток высушивают под вакуумом в сушильном шкафу (10 ми рт.ст., иасля", ный вакуумный насос) при 50-60 С и измельчают в порошок. Последний в колбе емкостью 1 л заливают этилацетатом (300 ип) и кипятят на водяной бане с обратным холодильником в течение 15 иин. После охлаждения и отстаивания этилацетатный раствор сливают. Обработку зтилацетатои пов торяют 3 раза. Затеи порошок высушивают в сушильном вакуумном шкафу вакуумом (30 мм рт.ст.) при 40-50 С до 2 л. Сгущенный экстракт обрабатывают этилацетатом (5 раз по 500 мл), Этилацетатные фракции выбрасывают.
Экстракт упаривают на водяной бане в фарфоровых чашках. Остаток высушивают под вакуумом в сушильном шкафу (10 мм рт.ст.) при 50-60 С и измельчают в порошок. Последний в колбе емкостью 1 л заливают этилацетатом (300 мл) и кипятят на водяной бане с обратным холодильником в течение
15 мин. После охлаждения и отстаивания этилацетатный раствор сливают. Обработку этилацетатом повторяют 3 раза. Затем порошок высушивают в сушильном вакуумном шкафу (1 мм рт.ст.) при 50-60 С до постоянного веса и изчезновения запаха этилацетата Получают 100 r (57 от веса исходного сырья) эпигалохина (целевой продукт), представляющего собой аморфный порошок светло-коричневого цвета с (Ì) 40 (e 1,0, этанол), разлагающийся при 290-300 С. МИ=
=2000-10000.
Эпигалохин является смесью растительных полимеров с различной степенью полимернэации, где 11 = 1-5 (примеры 1-3 получения эпигалохина).
Структура общей формулы,эпигалохина подтверждена химическими превращения ми и данными УФ-, ИК-спектров, сравнением этих данных с данными, полученными при изучении полимера с
11-1, выделенного из самого эпигалохина, Разделение полимеров г1 -2, И-3, Fl-5 не представляется возможным с технической точки зрения. Активность целевого продукта проявляется суммой конденсированных катехинов с различной степенью полимеризации — энигалохнном.
Определение молекулярной массы эпигалохина.
Иолекуляриую массу (ИИ} устанавли" вают методом гель-фильтрации на колонке с сефадексом марки Ь Н-20, растворитель и элюент — смесь диметилформамид " вода (9: 1). Образец берут в виде 0,5Х-ного раствора в указанной смеси растворителей и наносят на колонку (143 см) с сефадексом. Скорость элюации 6-7 мп/ч. Фракции собирают по 1 мл, концентрацию вещества в них определяют на спектрофотометре СФ-16 при 278 нм.
6 1155601 (1 мм рт.ст.) при 50-60 С до постоянного веса и исчезновения запаха этилацетата. Получают 300 г (15X от веса исходного сырья) целевого продукта, представляющего собой аморф- 5 ный порошок светло-коричневого цве-,а с >1 " +40 (с 1,0, этанол), разлагающийся нри 290-300 С, МИ = б
2000-10000.
П р и и е р 2. В перколятор ем- 10 костью 20 л вносят 2000 г воздушносухих мелкоизмельченных корней родиолы Семенова и шестикратно экстрагируют при комнатной температуре
20-25 смесью вода — этиловый спирт 15 (35X но объему) порциями по 12, 10, 10, 10, 10 л, каждой порцией в течение 24 ч. Полученные экстракты, хранящиеся в темноте при температуре
20-25 С, объединяют и упаривают в 26 роторном испарителе под вакуумом (30 мм рт.ст.) при 40-50 С до 2 л.
Сгущенный экстракт. обрабатывают этилацетатом (5 раз по 500 мл) . Этилацетатные фракции выбрасывают. Экст- 25 ракт упаривают на водяной бане в фарфоровьх чашках, Остаток высушивают под вакуумом в сушильном шкафу (";О мм рт.ст.) при 50-60 С и измельчают в порошок. Последний в 39 колбе емкостью i л запивают этилацетатом (300 мл) и кипятят на водяной бане с обратным холодильником в течение 15 мин. После охлаждения и отстаивания этилацитатный раствор сли-Э вают. Обработку этилацетатом повторяют 3 раза. Затеи порошок высушивают в сушильном вакуумном шкафу при
50-60 С до постоянного веса и исчезновения запаха зтилацетата. Полу- © чают 200 r (1ОЖ от веса исходного сырья) эпигалохина (целевой продукт), представляющего собой аморфный пово 4 шок светло-коричневого цвета с Щ +40
Э (с ".0, этанол), разлагающийся при 4
290-300 С, ИИ = 2000-10000.
П р ц м е р 3. В перколятор емкостью 20 л вносят 2000 г воздушносухих мелкоизмельченных корней родиолы Семенова и шестикратно экстра- © гируют при комнатной температуре смесью вода - этиловый спирт (70X по объему) порциями по 12, 10, 10, 10, 10Ä 10 л, каждой порцией в течение
24 ч. Полученные экстракты, хранящиеся в темноте при комнатной температуре (20-25 С), объединяют и упаривают в роторном испарителе под
1155601
На гель-хроматограмме (элюограмме) целлюлозой (5 х 140 см, 400 r). Элюираэграничивают области димеров, три-. Руют водой, водным этанолом (1:1), меров, олигомеров и полимеров раз- этанолом, метанолом, собирая фракличной степени полимериэации. Под- ции по 20 мл .1-45 вода, 46-90 (восчитав площади этих фракций на 5 да-этанол), 91-134 (этанол), 135. элюограмме, установили, что соедине- 160 (метанол). Упариванием раствония с MM меньше 2000, т.е. составляет рителя из Фракций 1-52 и 58-160 б от суммы соединения с MM до получают соединения различной сте5000 — 2,5 . 5100-5900 — 20Х; 5900- пени полимеризации (в граммах):
6600 — 50 ; 6600-7400 — 15 „ ïî 10 0,61; 5,87; 14,53, 4,50, 0,85; Q,52
10000 — 3,5Х и более 10000 — З . процентное соотношение которых совИз элюограммы и подсчетов видно, падает с результатами, полученнычто основную часть суммы составляют ми гель-фильтрацией. полимеры с ММ 5100-7400 (85 ) . При сгущении фракций 52-57 выдеРасщепление эпигалохина. 15 ляют 1,72 r вещества состава - Н О, И 75 5 °
В четырехгорлую круглодонную кол- ММ 1947 (ультрацентрифуга), при бу емкостью 50 мп помещают 1,0 эпи- 290-300 С разлагается, Pt 0,01 в галохина и 5,0 е 1кого калия. При системе р --бутанол — уксусная киспостоянном пропускании тока азота лота — вода (3:1:5) и Rf 0,54 в и перемешивании нижнюю часть колбы 20 этаноле p) +40 (с 1,О; этанол).
24 о погружают в баню с Легкоплавким Вычислено, : С 59,16 Н 3,87; сплавом при 155-160 С. Температуру О 36,97. поднимают в течение 5 мин до 230 С Найдено Х: С 59 17 Н 3 86 и затем реакционную смесь быстро О 36,97. охлаждают, подкисляют 20Х-ной сер- ;у уф cneKTp:I1 215 245 278
tTl Ф
310 нм (Я 5,43, 4,89, 4,45, 4,7). бавляют водой и экстрагируют этил Спектр снят на снетрофотометре Ерацетатом (50 мл х 5 раз) »ил- ЭТ Фирма "Hitachi" (Япония). ацетатное извлечение сушат безвод- ИК-спектр 9 3500-3200 2935 ным сульфатом натРиЯ, Фильтруют щ 1657, 1610, 1535, 1515, 1495, 1440. и отгоняют. Остаток хроматографи 1320, 1250, 1200, 1150, 1105, 1040, рувт на колонке с полиамидом . 1038 83, 830, 800, 770, 737 см . (элюент — смесь хлороформа с мета- Спектр снят на приборе HR-20 иолом 9:1). Получают следующие соеди "Карл-цейс-Иена" (ГдР). нения: С,Н<О» М 126, т.rq. 218- Иолекулярная масса и гомогенS
219 С, И 0,64, C H 0g, M 170э ность определена на ультрацентрифу т. пл. 220 (с разл.) Ц0,56, ге ИОМ 3170 (Венгрия), скорость
Су Н О, И 154, т. пл. 200 С (с Раз- 8000 об/мин, = 20 С, угол 30 ложением), Ц 0,72 (значения ве- время 30 мин 5= 1 7 10 13
Ф 3 ° ществ определены методом бумажной Е = 8,4 10 хроматографии в системе H-бутанол- Спектр ЯИР@ С снят на спектро85Х-ная муравьиная кислота — вода метре Varian XL-100 в растворе
95:10:20). ВИБО d g (1 !1), внутренний стандарт
Полученные соединения по физико- ТИЯ, сигнал которого принят за 0 химическим константам спектральным 45 (д"-шкапа). данным (ИК-, Уф- и масс-спектры) и непосредственным сравнениям с исСтруктура общей Формулы эпигалопытанными образцами идентифицировали хина подтверждена химическими превсоответственно с Флороглюцином, галло- Ращениями и данными УФ ИК и ЯИР вой и протокатеховой кислотами. При C-с ектроскоиии для полимера с11 1 ° действии соляной кислоы íà pas- В Уф-спектре иются мксиумы
56 вдавленный водный раствор эпигалохина при 220 240» 310 нм. В ИК-спектре образуются актоцианидины — цианидин- появляются полосы поглощения при и дельфинидин 3200-3500 см (колебания гидроксильных грУпп), 1657 см (Я;ООС-Арил), из эпи 55 1610 1535 1515 1440 галохина.
У ные колебания ароматического ядра), 30 г зпигалохина смешивают с 20 г 1535, 1515, 1150, 1040 и 830, 800, целлюлозы и помещают в,колонку с 770, 737 см (плоскостные и внеплос1155601
10 костные деформационные колебания
1,3,4- и 1,3,4,5-замещенных аромати. ческих колец), 1320, 1200 см (О-Н в фенолах и колебаниях = С-О связи), 1
1250 1038 см (=С-О-С-группы) 5
1033 см" (С-О), 1105, 1050 см (С-0-M этерифицированной вторичной
ОН-группы).
В SIMP С-спектре полимера обнаружены резонансные сигналы: при 154157 м.д. (С-9, С-5, С-7 кольца А эпикатехином), 145,9 м.д. (С-З и
С-4) кольца В эпикатехинов, С-3 и
С-5 кольца эпигаллокатехина); 133, 9 м.д. (С-4 кольца В эпигаллока- 15 техина); 131,5 м.д. (С-1 кольца В эпикатехинов) при 119,5 м.д. (С-6 кольца В эпикатехина) при 110,7 м.д (С-2, С-5 эпикатехина и С-2, С-б эпигаллокатехина), при 166,9; 145,9; 20
121,9 и 110,7 м.д. (соответ. С-, С-3 и С-4, С-5; С-1; С-2 и С-6 остатка галловой кислоты), при
107,7 м.д. (С-б, С-8 и С-10 замещенных колец А эпикатехияов), 25
105,4 м.д. (верхний конечный
С-10, примыкающий к замешенному
С-4), яри 100,5; 96,5 и 98,5 м.д. (соответ. С-10, С-8,и С-б конечных
А-колец эпикатехинов), 76,8-78,6 30 .(С-2 эпикатехинов), 72, 1-75,2 (С-3 эпикатехинов), при 37,9, 27,8 м.д. (соответ. С-4 замещеняых и С-4 конечного эпикатехинов).
Распределение фракций с различ- ным молекулярным весом в эпигалохине установлено методом гель-фильтрации на сефадексе марки AH-20.
Фармакологическое исследование эпигалохина.
Доза 100 мг/кг. Экспериментальны- мя животными являлись белые беспород,ные мыши весом 18-22 r. Представленные данные получены на 800 животных;
Гяпоксическая нормобарическая
45 гипоксия вызывалась помещеяием животных в герметически закрывающийся эксикатор. Препараты вводились внутрибрюшяняо за 30 мин до помещения в эксикатор. Полученные данные показа5 ли высокую противогипоксическую активность эпигалохина на этой модели гипоксии. Статистически достоверное удли.. некие продолжительности жизни мышей начиналось уже с дозы 1 мг/кг. В дозе
10 мг/кг продолжительность жизни мышей, получивших эпигалохин, составила 156Х к контрольной группе, в дозе 20 мг/KI — 165Х и дозе 40 мг/кг
207Х.. Противогипоксическая активность гутамина оказалась значительно слабее: в оптимальной дозе 100 мг/кг он удлинил жизнь животных на 145Х, т.е. меньше, чем эпигалохина в дозе
10 мг/кг, т.е. эпигалохин значительно активнее гутимина по защитному действию при гипоксической нормобарической гипоксии.
Гипоксическая гипобарическая гипоксия создавалась в барокамере. Животные "поднимались" до высоты 11 км со скоростью 1 км/мин. На "высоте"
11 км мыши наблюдались в течение
45 мин, Животные, преодолевшие этот временной барьер, считались выжившими. Препараты вводились sa 30 мин до помещения мышей в барокамеру.
Эпигалохин проявляют высокую противогипоксическую активность и на этой модели гипоксии. В дозе
20 мг/кг (внутрибрюшинно) он предохраняет гибели 60Х животных (в контрольной группе все мыши погибли
Ю за 3, 2-0, 58 мин) и статистически достоверно удлинил продолжительность жизни на 92,5Х по отношению к контролю. Активность гутимина была меньшей: в дозе 100 мг/кг (внутрибрюшинно) он удлинил продолжительность жизни животных на 650Х и не предохранил от гибели ни одного животное.
Таким образом, эпигалохин превосходит гутимин по защитному действию от гипоксической гипоксии.
Цитотоксическая гипоксия вызывалась подкожным введением цианистого натрия в дозе 8 мг/кг. Препараты вводились внутрибрюшиняо за 30 мин до инъекции цианистого натрия. Эпигалохин в дозе 40 мг/кг статистически достоверно удлинил продолжительность жизни животных в 5,-74 раза. Действие гутимина быпо значительно слабее: в дозе 100 мг/кг ой удлинил продолжительность жизни лишь в 3 раза.
Эпигалохин превосходит гутимия по .защитному действию от цитотоксической гипоксии.
Гемическая гипоксия вызывалась внутрибрюшиниым введением нитрита натрия в дозе 160 мгlкг. Препараты вводились на 30 мин до инъекции нитрита натрия, внутрибрюшинно.
В контрольной группе погибли все животные. Эпигалохин в дозе 20 мг/кг предохранил от гибели 17Х мышей
1155601
Составитель И. Дьяченко
Редактор Т. Веселова Техред С.Легеза корректор С. Шекмар
Заказ 3037/22 Тираж 384 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35; Раушская наб., д. 0/5
Филиал ППП "Патент", г. Ужгород, ул. Проектная, 4 и на 157Х удлинил продолжительность жизни остальных животных. Гутимин не только не проявил защитного эффекта, а статически достоверно уменьшил время их жизни в 2 раза по срав- 5 нению с контролем.
Эпигалохин оказывает защитное действие от гемнческой гипоксии в отличие от гутнмина, ухудшающего ее течение. 10
Изучение общего действия и токсичности эпигалохина показало, что при внутрибрюшинном введении вещество не вызывает изменений в поведе. нии животных до дозы 50 мг/кг, от 15 которой наступает небольшое уменьшение спонтанной двигательной активности и урежение дыхания. С увеличением дозы эти явления становятся более выраженными, животные группи- 20 руются, появляется птоз и расслабление шейных мышц. Спонтанные движения!
I почти отсутствуют, однако на звуковое и болевое раздражение животные реагируют писком и реакцией и1бегания. ЛД >, рассчитанная по Ференсу, составляет 325 мг/кг. При введении внутрь действие препарата аналогично но начальная угнетающая доза составляет 200 мг/кг, а ЛД по Беренсу — 833 мг/кг. Следовательно, широта фармакологического действия эпигалохина при внутрибрюшинном введении в оптимальной дозе (20 мг/кг) составляет 16,2, ЛД гутимина при подкожном введении составляет
1325 мг/кг, т.е. широта фармакологического действия для оптимальной дозы 100 мг/кг составляет 13,2.
Таким образом эпигалохин превосходит гутимин по широте фармакологического действия.