Способ иммобилизации микросом печени
Иллюстрации
Показать всеРеферат
СПОСОБ ИММОБИЛИЗАЦИИ МИКРОСОМ ПЕЧЕНИ путем их ковалентного связывания на полиэтилене с привитык сополимером с помощью поперечносшивающего реагента, отличающийся тем, что, с целью повышения монооксигеназной активности целевого продукта и удешевления способа , в качестве привитого сополимера используют полиаллиловый спирт в количестве 4-9%, а в качестве поперечно-сшиваящего реагента 15-35%-ный п-бензохинон, причем массовое соотношение белка микросом и носителя составляет
СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИК (19) () 1) 4(si) С 12 N 11 18
ОПИСАНИЕ ИЗОБРЕТЕНИЯ;
ГОСУДАРСТ8ЕННЫЙ НОМИТЕТ СССР
IlO ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТНРЫТИЙ
H ABTOPCHOMV СВИДЕТЕЛЬСТВУ (21) 3642160/28-13
{22) 28.07.83 (46) 15.06.85. Бюл. У 22 (72} Т.И. Давиденко, О.В. Севастьянов, А.Д. Помогайло и С.А. Андронати (71) Физико+химический .институт
AH УССР (53) 517. 15 (088.8) (56) 1 ° Патент ГКР Ф 113013, кл. С 07 С 7/02, 1975.
2. Авторское свидетельство. СССР
В 1057536, кл. С 12 N 11/18,, 1981. (54) (57) СПОСОБ ИИИОБИПИЗАЦИИ ИИКРОСОИ ПЕЧЕНИ путем их ковалентного связывания на.полиэтилене с привитым сополимером с помощью поперечносшивающего реагента, о т л и ч а юшийся тем, что, с целью новьппения монооксигеказной активности целевого продукта и удешевления способа, в качестве привитого сополимера используют полиаллиловый спирт в количестве 4-93 а.в качестве поперечно-сшивающего реагента—
15-35Х-ный п-бензохинон, причем массовое соотношение белка микросом и носителя составляет (0,3:10)(1: 10) .
161553 2
10
Цель изобретения — повышение монооксигеназной активности целевого продукта и удешевление способа получения иммобилизованных микросом.
Поставленная цель достигаешься тем, что согласно способу иммобилизации микросом печени путем их ковалентного связывания на полиэтилене с привитьик сополимером с помощью поперечно-сшивающего реагеита, в качестве привитого сополимера исполь
1,1
Изобретение относится к биотех-,.: нологии, в частности к способам получения иммобилизованных микро. сом печени животных, и может быть применено в медицине и биохимии для изучения метаболизма и ток, сического действия лекарственных веществ, в аналитической промышлен1 ности (для создания ферментных элементов) в тонком органическом синтезе (для направленного получения продуктов окисления, обладающих оптическай активностью).
Известен способ иммобилизации микросом печени, заключающийся в ковалентном связывании с матрицей
BrCN-активированной сефароэой j1) .
Недостатками данного способа являются необходимость разделения монооксигеназной системы микросом печени на компоненты: цитохром
P-45О, НАДФН-зависимую редуктазу и фосфатидилхолин перед иммобилизацией для получения стабильного продукта, обладающего активностью, так как при иммобилизации самой системы микросом наблюдается полное исчезновение монооксигеназной активности, низкая активность и стабильность целевого продукта.
Наиболее близким к предлагаемому по технической сущности и достигаемому положительному эффекту является способ иммобилизации микросом печени путем их ковалентного связывания на полиэтилене с привитым сополимером с помощью попвречно-сшивающего реагента, в качестве привитого сополимера используют полиакриловую кислоту в количестве 6-10, а s качестве поперечно-сшивающего реагента карбодиимид f2) °
Недостатками способа является низкая активность монооксигеиаэы у целевого продукта (25X от исходной). а также необходимость использования дорогостоящего карбодиимида.
3$
4$
$0
$$ зуют полиаллиловый спирт в количест-. ве 4-9, а в качестве поперечно-сшивающего реагента 15-35 -ный и-бензохинон,причем массовое соотношение белок микросом и носителя составляет (О 3.10)-(1 10)
Сущность способа заключается в использовании полиаллилового спирта в количестве 4-9% в качестве привитого сополимера и 15-55%-ный и-бензохинона в качестве поперечно-сшивающего реагента. Преимущества при этом возникают как за счет изменения структуры полимера, так и вследствие увеличения расстояния от микросом до матрицы при замене карбодиимида на бензохинон. Важным параметром при этом является соотношение белок микросом: носитель, которое должно быть в диапазоне от (0,3:10) †(1:10). Ионооксигеназная активность в указанном интервале соотношений максимальна (таблица 1), при соотношении 1,25: 10 значение активности также несущественно изменяется, однако при этом резко падает процент связывания белка микросом. При весовом соотношении
0,2:10 монооксигеназная активность составляет 70%. В таблице приведены также возможные интервалы параметров, касающихся концентрации и-бензохинона и полиаллилового спирта.
Оптимальное значение количества привитого полиаллилового спирта составляет 4-9%. При использовании носителя с 2 полиаллилового спирта монооксигеназная активность составляет
58-59 от максимальной, верхний предел {9 ) полиаллилового спирта обусловлен воэможностями метода радиационной прививки. Использование низких концентраций и-бензохннона приводит к снижению активности препарата, а era увеличение свыше 35 нецелесообразно.
Способ позволяет полностью сохранить монооксигеназную активность целевого продукта и удешевить процесс за счет использования доступного поперечно-сшивающего реагента.
Пример 1. Активация полиэтилена с 5,6Х привитого полиаллилового спирта осуществляется следующим образом. К 9,0 r полиэтилена с 5,6 привитого полиаллилового спирта в 560 мл О,i И KH PO /NaOH буфера, рН 8,0 (комнатная температура, перемешивание на магнитной
1161553
Иммобилизовайную фракцию микросом
35 суспендируют в буфере А, рН 7,4.
Монооксигеназная активность IIo анилину 6,66 нмоль субстрата/нмоль цитохрома P-450 в мин при 37 С (сохранение активности в Х от исход40 ной 142,6Х) в присутствии гидроперекиси кумола 0,49 нмоль субстрата/нмоль цитохрома P-450 в мин о при 37 С (сохранение активности от исходной — 207,1X) в присутствии
НАДФН генерирующей системы и О и
0,77 нмоль субстрата/нмоль цитохрома P-450 в мин при 37 С (сохранение активности от исходной
257,2X) в присутствии НАДФН и О з мешалке) добавляют 139 мл 0,25 М раствора и-бензохинона в 96Х-ном этаноле. Суспензию перемешивают
1 ч при комнатной температуре, затем переносят на воронку Бюхнера и промывают 20Х-ным этанолом, дистиллированной водой, 1 M NaC6 и сно ва дистиллированной водой.
Используют нативные микросомы со следующими характеристиками: выход микросомального белка 24,5 мг белка/г печени, активность по анилину 4,7 нмоль субстрата/HM0JIb цитохрома P-450 в мин при 37 С.
1 г полученного полиэтилена с привитым полиаллиловым спиртом, активированным п-бензохиноном
1 суспендируют в охлажденном буфере А, рН 8,0 (О, 1 M КН РО /ИаОН) со
100 мМ КСР, 1.мМ ЭДТА, мМ дитиотреитола, приготовленном на 20Х-ном (по объему) глицерине. При перемешивании на магнитной мешалке к суспензии носителя добавляют суспензню фракции микросом, содержащую
30 мг белка. Полученную суспензию инкубируют при перемешивании на магнитной мешалке 24 ч при 4-5o(. Э .затем промывают на воронке Бюхнера буфером Б, рН 7,4 (0,1 M KH>Pg/haOH) с 0,5 М КС1, 1 мМ ЭДТА и t мМ дитиотреитола, приготовленном на 20Х-ном глицерине, а затем аналогичным буфером без КС6 .
Иммобилизованные по данному способу микросомы стабильны при хранении в течение 6 мес при 4-5 С, за это время падение монооксигеназной активности составляет 20Х
Температурный оптимум микросом печени, иммобилизованных на полиэтилене с привитым полиаллиловым о спиртом 37 С, а рН вЂ” оптимум — 7,6.
10 Пример 2. Порядок выполнения операций аналогичен примеру 1..
Отличие заключается лишь в том, что к 1 r полиэтилена с привитым полиаллиловым спиртом, активированным п-бензохиноном, добавляют при перемешивании суспензию фракции микросом, содержащую 100 мг белка.
Монооксигеназная активность по анилину 6,90 нмоль субстрата/нмоль
20 цитохрома P-450 в мин при 37 С (сохранение активности в Х от исходной
147,6) в присутствии гидроперекиси кумола, 0,51 нмоль субстрата/нмоль цитохрома P-450 в мин при 37 С
25 (сохранение активности в Х от исходной — 214.6) в присутствии
НАДФН вЂ” генерирующей системы и 0 г и 0,80 нмоль субстрата/нмоль цитохрома P-450 в мин при 37 С (сохранение активности в Х от исходной
266,5) в присутствии НАДФН и О, .
Применение предлагаемого способа позволяет отказаться от использования дорогого и сложно синтезируемо"
ro карбодиимида-р-1-циклогексил-3-(2-морфомикоэтил)карбодиимид-мето-P-толуолсульфоната и заменить его более доступным и дешевым и-бензохиноном, что значительно упрощает и удешевляет способ иммобилизации.
Использование предлагаемого способа иммобилизации позволяет повысить моноксигеказкую активность до
142-148Х вместо 25Х в прототипе (s присутствии гидроперекиск кумола)
207-215Х (в присутствии НАДФН генерирующей системы и 0 ) и 257-267Х (s присутствии НАДФН и О,).
Способ прост в осуществлении, не требует особых условий при модификации носителя.
1161553
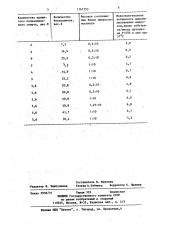
Количество бензохинона, вес.Х
Весовое соотношение белок микросом: носитель
Количество привитого полиаллилового спирта, вес.Х
Моноокснгенаэная активность иммобилизованных микросом,нмоль субстрата/нмоль цитохрома Р-450 в мин при
37 С
3,9
0,3:10
О 3310
0,3:10
I:10
1:10
1:10
0 2:10
0,3 310
1:10
7,5
14,9
6,3
6 5
35,2
6,7. 14,9
35,2
4,&
20,8
20,8
6,7
6,9
t 25:10
20,8
5 6
6,8
5,6
41,7
1:1О
1:10
S 3
Тирам 525 Подписное
ЭЯИЙПИ Государственного комитета СССР по делам изЬбретений и открытий f13035, Москва, Ж-35, Раушская наб., д. 4/5
Заказ 3938/31
Филиал ДПП "Патент", г. Умгород, ул. Проектная,4
Составитель В. Иуронец
"Редактор Н. Киштулииец, Техред А.Бабииец Корректор С. Шекмар