Бромзамещенные хинолины как промежуточные продукты для синтеза ингибиторов моноаминооксидазы
Иллюстрации
Показать всеРеферат
Бромзамещенные хинолины общей формулы (I) 7-Вг 8-Вг i 7-Вг как промежуточные продукты для синтеза ингибиторов моноаминоксида ы. (Л
СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИН (19) ())) 4(») С 07 0 215/f8
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К ABTOPCHOMV СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР
Il0 ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТНРЫТИЙ (21) 3704668/23-04 (22) 29.02.84 (46) 30.06.85, Бюл. У 24 (72) А,И,Точилкин, И.P.Êîâåëüìàí, И.Н. Грачева, Е.П.Прокофьев, И.В.Веревкина, Д.И.Иоффина и В.Ç.Горкин (71) Институт биологической Ъ» медицинской химии АМН СССР (53) 547.781.785.07 (088.8) (56) 1. Грачева И.Н., Точилкин А,И.
Синтез и бромирование 8-метил-5-хинолинкарбоновой кислоты.. ХГС, 1980, 1 3, с. 366. (54) БРОМЗАМЕЩЕННЫЕ ХИНОЛИНЫ КАК
ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ СИНТЕЗА
ИНГИБИТОРОВ МОНОАМИНОКСИДАЗЫ (57) Бромзамещенные хинолины общей формулы (1) и,.1)
+) Rf = 8Me, Rz= 58r, R>=.7 Вг б) Р(— — 6-Ме, R = 5-8r, R> --- 8-Br в) Rf =-7Ие, и = 58г, R =8 Br г) Rf = 8-Me, Rz 5-N0z йз 7-Br как промехуточные продукты для синтеза ингибиторов моноаминоксидазы.
1 1164231 2
СНз
Вг
Br
CH2Br
3r сн,и — сн,с = — сн
СН
Изобретение относится к производ-. ным хинолина, а именно к бромзамещенным хинолинам общей формулы а) RI =8Ме, К =5Br, R>=7Br б), = 6-Me = 5 Br, R =.8-Br
a) R = 7Ме R = 5Br, йз = 8 Br
1 У у г) й, = 8Ме, R = 5NO<, R = 7Br.
Эти соединения могут быть использованы для синтеза ингибиторов моноаминоксидазы (ИАО).
NA0 является важным ферментом, который катализирует дезаминирование важнейших нейромедиаторов и био1генных аминов, участвующих также в регуляции функций сердечно-сосудистой системы, роста и деления клетки.
Ингибиторы ИАО находят применение в медицине как лекарственные средства.
Известен 5-бром-8-метилхинолин, из которого через 5-бром-8-бромметилхинолин получают 5-бром-8-(N-метил-N-2-пропинил)аминометилхинолин— ингибитор МАО 11) .
Основным недостатком излучения ЗО этого ингибитора является использование на стадии синтеза промежуточного 5-бром-8-метилхинолина - дорогостоящего и дефицитного серебра.
Целью изобретения является поиск З5 новых промежуточных продуктов для синтеза ингибиторов ИАО более простым и доступным способом.
Поставленная цель достигается .получением новых соединений общей формулы (11, которые могут быть использованы как промежуточные продукты в синтезе ингибиторов МАО.
Соединения общей формулы (1 1 получают взаимодействием соответствующих производных хинолина с N -бромсукциимидом (БСИ) в концентрированной серной кислоте в мольных соотношениях хинолин-БСИ I:2 при 50-60 С, о
Полученные соединения применяют в качестве промежуточных продуктов в ! синтезе ингибиторов МАО. Для получения ингибиторов, например, форму-:: лы (III, соединение Iа обработкой
БСИ Ъ четыреххлористом углероде в . .присутствии перекиси бензоила превращают в бромметильное производ,ное III, которое при реакции с И -метилпропаргиламином дает соответствуюший бромзамещенный ингибитор ИАО формулы II по реакции
Ингибиторы, полученные на основе производных la-г обладают выраженной антимоноаминоксидазной активностью и избирательностью по отноше-нию к различным субстратам МАО. Так, 5,7-дибром-8-(N-метил-N-2-пропил)аминометилхинолин (II) в концентрат ции I I0 моль практически полностью (97-0,97) ингибирует дезаминирование серотонина митохондриями печени крысы и только частично (42-8,157)дезаминирование 2-фенилэтиламина. Величины. о для этих субстратов различаются почти на два порядка:
3,3 1О 8моль и 1,5 ° 10 моль соответственно. Такой избирательностью не обладает выбранный в качестве наиболее близкого аналога 5-бром-8-(11"метил-N-2-пропинил)аминометилхинолин.
Величины 3< для серотонина и 2-фенилэтиламина составляют 2,5 IO u
-3
4 10 моль соответственно. Следовательно, соединение формулы (Il), содержащее два атома брома в молекуле, является мощным избирательным ингибитором МАО типа А .митохондрий печени крысы.
Таким образом, изобретение позво- ляет удешевить и упростить способ получения промежуточных соединений для синтеза мощных избирательных ингибиторов МАО. через 40 мин реакционную смесь упаривают, остаток растворяют в эфире, осадок отделяют, после упаривания маточного раствора получают ингибитор. Навеску ингибитора обрабатывают
5 мл 0,1 н. НСl, в течение 10 мин упаривают, сушат над пятиокисью фосфора при 1 мм 2iч, получают дигидрохлорид 5,7-дибром-8-(й-метил-М-2пропинил)-аминометилхинолина.ИКспектр: 2130 (С=С),, 2308 (С=-СН) см
Найдено, Х: С 38.5; Н 3,4.
С14Н1 8г С lz Nz
Вычислено, Х: С 38,0, Н 3,2.
П р н м е р 5. Антимоноаминоксидазная активность дигидрохлорида
5,7-дибром-8-(й-метил-й-2-пропил)аминометилхинолина.
В качестве источника МАО испольэо" вали фракции митохондриальных мембран печени крысы. Инкубационные пробы объемом 1,8 мл содержали 50 мМ фосфатный буфер рН=7,4, 3 мг белка митоI хондриальных мембран, ингибитор и субстрат. Контрольные пробы ингибитор не содержали. Суспензию митохондриальных мембран в буфере преинкубировали с исследуемыми соединениями в течение 30 мин при 37 в атмосфере кислорода. В качестве субстратов использовали амины в оптимальных концентрациях: серотонин креатинсульфат10 мкмоль, гидрохлориды 2-фенилэтиламина — 0,8 мкмоль, содержание белка определяли по методу Лоури. Соединение ингибирует дезаминирование
-6 серотонина при концентрации 1 10 моль на 97-0,9Х и при этой же концентрации на 42-8,!5Х ингибирует дезаминирование 2-фенилэтиламина. 1 о для серотонина 3,3.10 8моль, Э для 2-фенилэтиламина — 1,5 ° 1(смоль.
Таким образом, на основе предлагаемых новых. соединений общей формулы (1), полученных простым и доступным способом, могут быть синтезированы мощные избирательные:инриби торы MAO.
Таблица 1 з 1 1-64231
Пример 1. Бромирование 6- "„а,;,..
7-, 8-метилхинолинов посредством
БСИ.
Перемешивают 3 ч при 50-60 смесь
0,015 моль соответствующего хинолина и 0,03 моль БСИ в 20 мл 93-94Х
Н Ь04. После завершения реакции смесь охлаждают, выливают в 500 мл воды и при рН=! отделяют осадок, который экстрагируют хлороформом, су- 10 шат MgS04, растворитель упаривают и получают хроматографически чистый продукт (система для хроматографирования — бензо) -этилацетат-уксусная кислота, 100:50:1/А). Маточный раствор подщелачивают 45Х-ным раствором КОН до pH=10 охлаждают и экстракцией хлороформом выделяют дополнительное количество 6 7- или
8-метилбромзамещенных хинолинов
lа-в, очищенных хроматографией на пластинках с силикагелем в системе А.
Выходы и свойства полученных соединений см. в табл. 1 и .2.
Пример 2. Бромирование
5-нитро-8"метилхинолина.
Нагревают при 60 смесь 1,98 г (0,01 моль) 5-нитро-8-метилхинолина и 1,96 г (0,011 моль).БСИ в 20 мл
100Х-ной серной кислоты, обрабатывают, как описано в примере 1, выделенное производное кристаллизуют из н-пропилового спирта.
Пример 3. 5 7-дибром-8"бромметилхинолин (111). 35
Кипятят 5 ммоль 5,7-дибром-8-метилхинолина и 5 ммоль БСИ в 40 мл четыреххлористого углерода при облучении лампой 200 Вт через 2 ч < осадок отделяют, растворитель упа- 40 ривают и получают производное IlT (табл. 1).
Пример 4. 5,7-дибром-8 (й-метил-й-2-пропинил)аминометилхинолин (11). 45 а
Перемешивают при 20 С раствор
1,5 моль 5,7-дибром-8-бромметилхинолина и l мп К-метилпропаргиламина, 23
lа
53,9 4,7
102-103 54,8 4,84 С, Н Вг и
119-120 54э8 5 в 1 Сяйч Br N
O
Соеди- Выход, X Т,пл., С кение, (из спирта)
1164231
Продолжение табл.1
Найдено, Х и
Вычислено, Х
Бр ут то-формула
Br й
115-116 53,9 5,1 C, Н Вг й
1в
53,9
4,7
1г
1 27,5-129 29,87 0,8
1 и 7 2
С Н Вг2С1 М
29,9 10,8
П 63
I JZ 80
155-158
151-153 63,3
63,2 3,7
4,0
Сю" 68 3 14
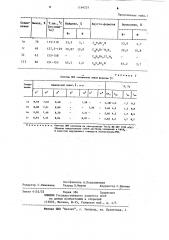
Таблица 2
Спектры ПМР соединений обней формулы (1) Химический сдвиг, а и д. Хо Гц
j" Г
Сое нен н 1 н н и 1 123 1И tÔÔ
7,98
7,96
7,74
1а 8,93 7;49 8,48 .
1б 8,98 7.,51 8,60
С,287 4,2
1,7 8,5
2,60 4,2
l,7 8,6
l i7 8,5
1,7 8,7 н
2,66 4,2
2,83 4,2
)s 9,02 7,49 8,50
8,25l г 8,93 7,55 8,84
П р н м е ч а н и е. Спектры ПМР получены на спектрометре Тез1а 85-567 (180 мГп)
Образцы представляли собой растворы соединенй в CQC11> .
В качестве внутреннего стандарта использовали ТМС. и
Составитель А.Подхалюзина
Техред Л.Микеш Корректор С.Шекмар
Редактор С.Тимохина
Заказ 4152/22 Тираж 384 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент", r. Ужгород, ул. Проектная, 4.