Способ определения концентрации ионов в растворах
Иллюстрации
Показать всеРеферат
СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ИОНОВ В РАСТВОРАХ, заключающийся в избирательном вьщелении их в раствор-носитель с последующим определением в нем концентрации, отличающийся тем, что, с целью повышения точности определения , избирательное выделение анализируемых ионов в раствор-носитель осуществляют электродиализом, при этом концентрацию анализируемых ионов в растворе-носителе поддерживают постоянной путем регулирования напряжения на электродах электродиализной ячейки, а концентрацию ионов определяют по вапичине тока ячейки.
СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИК (19) (I1) (5()4 G 01 N 27/26
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К ABTOPCHOMY СВИДЕТЕЛЬСТВУ
4ф "-4;4у фЦ 7
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР
ПО ДЕГАМ ИЗОБРЕТЕНИЙ И ОТНРЫТИЙ (21) 3436101/18-25 (22) 07.05.82 (46) 15.09.85. Бюл. N - 34 (72) В.Г.Динкель, ".Н.Салахов, M.Þ.Ïðàõoâà и А.Э.Динкель (53) 541. 13 (088. 8) (56) 1.. Патент США Р 2832734, кл. G 01 N 27/26, опублик. 1968 °
2. Формен Дж. и др. Автоматический химический анализ. M.: Мир, 1978, с. 184-185. (54) (57) СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ИОНОВ В РАСТВОРАХ, заключающийся в избирательном выделении их в раствор-носитель с последующим определением в нем концентрации, отличающийся тем, что, с целью повьппения точности определения, избирательное выделение анализируемых ионов в раствор-носитель осуществляют электродиализом, при этом концентрацию анализируемых ионов в растворе-носителе поддерживают постоянной путем регулирования напряжения на электродах электродиализной ячейки, а концентрацию ионов определяют по величине тока ячейки.
Известен электрохимический метод автоматического определения содержания ионов, например ионов хлора, в водном растворе, в соответствии с которым к анализируемому раствору добавляют водорастворимый йодид до образования его концентрации, стехиометрически эквивалентной количеству подлежащего определению хлора, Получившийся раствор подают в электролитическую ячейку, работающую по принципу деполяризации катода. Мерой концентрации хлора в анализируемом растворе является значение тока, проходящего через я ейку (1).
Недостатками данного способа являются введение реагента (йодида) непосредственно в анализируемый раствор, большое время анализа и неприменимость для концентрированных растворов.
Наиболее близким по технической сущности к предлагаемому является способ определения концентрации ионов в растворах, заключающийся в избирательном выделении их в раствор-носитель с последующим определением в нем концентрации P2 ).
35
Недостатком этого способа является невысокая точность определения, что обусловлено следующими факторами: требуется точное дозирование пробы; транспортирование анализируе" 45 мых ионов за счет диализа подчиняется закону Фика (это приводит к тому, что с уменьшением разности концентраций уменьшается поток ионов и при некотором малом значении разнос- 50 ти концентраций поток ионов будет меньше предела обнаружения их в растворе-носителе). Указанный фактор приводит к полной потери чувствительности приборов. Кроме того, устрой- 55 ство имеет нелинейность статической характеристики в широких пределах изменения анализируемого компонента.
1 11791
Изобретение относится к электрохимии, предназначено для непрерывного измерения малых концентраций компонентов в слабых, сильно концентрированных растворах и может S быть использовано, например, при производстве каустической соды мембранным способом для непрерывного определения содержания в ней хлоридов натрия NaC1. 10
95 2
Цел. изобретения — повышение
I точности определения.
Поставленная цель достигается тем, что согласно способу определения концентрации ионов в растворах, заключающемуся в избирательном выделении их в раствор-носитель с последующим определением в нем концентрации, избирательное выделение анализируемых ионов в раствор-носитель осуществляют электродиализом, при этом концентрацию анализируемых ионов в растворе-носителе поддерживают постоянной путем регулирования напряже. ния на электродах электродиализной ячейки, а концентрацию ионов определяют по величине тока ячейки.
При наложении на диализ электрического поля (электродиализе} .поток ионов увеличивается за счет миграционной составляющей, которую можно регулировать напряжением на электродах электродиализатора, а следовательно, повысить точность измерения при малых значениях концентрации анализируемых ионов. Кроме того, поддержание концентрации ионов в растворе-носителе постоянной позволяет спрямить статическую характеристику, а следовательно, повысить точность измерения в широком пределе изменения концентрации анализируемого компонента.
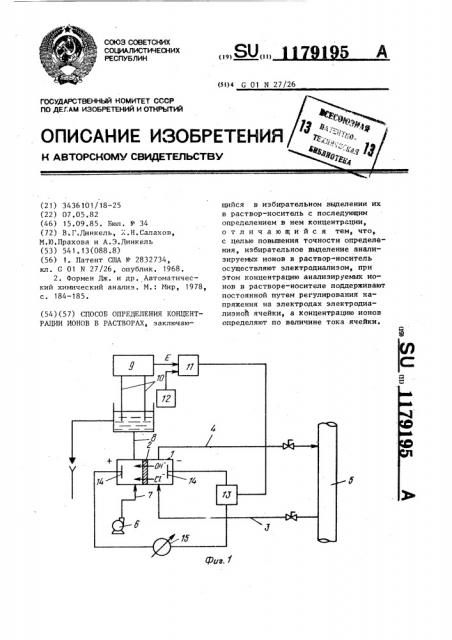
На фиг. 1 приведена схема осуществления способа; на фиг. 2 — экспериментальная зависимость тока электродиализа от концентрации ионов хлора в анализируемом растворе.
Схема состоит из электродиализной ячейки 1, которая ионообменной мембраной 2 разделена на две камеры. Катодная камера соединена линией 3 подвода и линией 4 отводй с трубопроводом технологического потока 5. В рабочую камеру электродиализной ячейки дозатором 6 подается раствор-носитель 7. Рабочая камера электродиализной ячейки соединена линией 8 отвода раствора-носителя с измерительной ячейкой 9, в которой размещены индикаторные электроды 10, ЭДС которых подается на вход преоб-разователя ЭДС .индикаторных электродов в унифицированный сигнал, который подается в элемент 11 сравнения, связанный также с задатчиком требуемого значения потенциала 12. Выход79195
Аб солю центра хлорид
10 рия в ке, г/л
О/200 !
220 .
0,7/200
1,46/200
2, 92/200
О, 238 180
0,497
140
0,989
3 11 ной сигнал элемента сравнения является управляющим для регулируемого источника 13 тока, позволяющего регулировать напряжение на генераторных электродах 14 электродиализной ячейки. В эту же цепь включен индикатор 15 тока электродиализной ячейки., Пример. Измерение. концентрации хлорида натрия в каустике.
Анализируемый раствор, представляющий собой совокупность компонентов NaOH+NaC1+H>0 с концентрациями NaOH 20-40%; NaC1 0 Ф 0,1%; Н Оостальное, подают в катодную камеру электродиализной ячейки 1, откуда током электродиализа транспортируют ионы Cl u OH через ионообменную мембрану 2 в поток раствора-носителя 7, в качестве которого используют, например, разбавленный раствор (10 н.) азотнокислого натрия NANO> .
Затем поток раствора-носителя 7, содержащего исследуемые ионы, пропускают через ячейку 9 с измерительными электродами 10. Генерируемая на этих электродах ЭДС E будет функционально. связана с концентрацией исследуемых ионов Cl в раствореносителе. Эту ЭДС используют в качестве управляющего сигнала, в соответствии с которым изменяют ток электродиализа 1.(его значение все время изменяют таким образом, чтобы генерируемая на измерительных электродах ЭДС Е оставалась равной заданному значению E ). Таким. образом, ток электродиализа I в любой момент времени будет являться мерой концентрации ионов хлора в растворе-носителе, т.е. в конечном счете мерой концентрации хлористого натрия в анализируемом растворе.
В таблице представлены результаты, полученные при экспериментальном определении зависимости силы тока в электродиализной ячейке от концентрации хлорида натрия в каустике.
Эквивалентная -концентрация хлори да натрия в каустике определялась д как отношение. концентрации NaC1 (r-экв./л) к концентрации NaOH (r-экв./л), величина потенциала электродной, системы поддерживалась постоянной и равной 290 мВ.
Построенная характеристика (фиг. 2) подтверждает линейный характер зависимости Т=Е(4) и высокую чувствительность. способа, которая составляет 120 мА/% концентрации.
Предлагаемый способ позволяет
35 концентрацию. анализируемых ионов в растворе-носителе поддерживать постоянной и на уровне максимальной чувствительности анализатора.
При этом анализатор в целом, реализующий предлагаемый способ, обладает линейной статической характеристикой с максимальной чувствительностью.
zoo
Составитель Г.Дамешек
РедактоР М.ПетРова ТехРед Т.ДУбинчак КоРРектоР В.Сини ая
Заказ 5655/43 Тираж 897 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент", r.Óærîðîä, ул.Проектная, 4