Способ получения производных 6,7-диаминоиндолов
Иллюстрации
Показать всеРеферат
СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 6,7-ДИАМИНОИНДОЛОВ общей формулы RuCGNM РцСОЫН R, где R, - водород или бензоил; Rg - метил, фенил, этоксикарбонил или карбоксил; В - водород, низший алкил, или Я.и Я вместе-(СН,,),,-(СН)-. (CH,)CH,,-; метил или фенил, отличающийся тем, что производные 1,2,5-тиазоло
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК
I 19> (I I) SU
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
1, ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЭОБРЕТЕНИЙ И ОТКРЬП ИЙ (21) 3673861/23 — 04 (22) 15.12.83 (46) 23.11.85. Бюл. tP 43 (71) Новокузнецкий научно-исследовательский химико-фармацевтический институт (72) Г. А. Титов и В. П. Четвериков (53) 547.752.07 (088.8) (56) Эфрос Л. С. и Левит P. М. Нитрование пиазтиола.-ЖОХ, 1953, т. 23, Й"-..9, с.1152. (54) (57) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 6,7-ДИАМИНОИНЯОЛОВ общей формулы
RNCONH R
2 йчСОМН R( где а, — водород или бензоил; а — метил, фенил. зтоксикарбонил или карбоксил; (5l)4 С 07 З 209/08, 209/82, 471/Щ а,— водород, з и лкил, ww а,и R> вместе - (СН ), - (СН ) —, — СН СН N(CH )CH —;
R 4 — метил или фенил, отличающийся тем, что производные 1,2,5-тиазоло13,4-о1 индолов общей формулы где R<-r > имеют указанные значения, .обрабатывают цинком и соляной кислотой в среде низшего алифатического спирта при кипении с последующим ацилированием образую щегося продукта уксусным ангидридом или хлористым бензоилом и выделением целевого продукта известными Методами.
1193ISI
К (1) Изобретение относится к способам получения новых производных индольного ряда, а именно производных 6,7-диаминоиндолов общей формулы а>СО 1Н Rã „соин где Я вЂ” водород или бензоил;
R — метил, фенил, этоксикарбонил или карбоксил;
R — водород, низший алкил, или R и Я вместе — (СН ) з —, — (СН ) — СН СН N(CH )СН
Я4 — метил или фенил, которые могут найти применение как полупродукты для синтеза биологически активных веществ.
Цель изобретения — получение новых соединений 1гроизводньгх индола, содержащих аминогруппы в положении 6 и 7, которые невозможно синтезировать известньгми способами.
Пример 1. Получение 67 диацетиламиноиндолов И- и (общая методика), /
К кипящему раствору 0,01 моль (1,2,5 (тиадиазоло) 3,4-g) индола (11) в изо" пропиловом (в этиловом — в случае соединения 1и) спирте добавляют 10 г цинковой пыли и 5 мл разбавленной (1:1) соляной кислоты (порциями по 5 — 6:лл), кипятят
8 — 5 мин, фильтруют, к фильтрату добавляют
14 мл (0,15 моль) уксусного ангидрида и оставляют при комнатной температуре на ночь. Затем реакционную смесь разбавляют
5-кратным объемом воды и через 5 — 6 ч (0-5 C) фильтруют (в случае соединения Те пглученный раствор предварительно подщелачивают водным раствором аммиака и насыщают хлористым натрием). Осадок промывают водой и высушивают в вакууме при
80 — 90 С. Получают соединения T a -u.
Пример 2, Получение 6,7-дибензоиламиноиндолов 1 к -р (общая методика).
К кипящему раствору 0,01 моль (1,2,5(тйадиазоло) 3,4- g) индола (1 1) в изопропиловом спирте добавляют 10 r цинковой пыли и
25 мл разбавленной (1:1) соляной кислоты (порциями по 5 — 6 мл), кипятят 8 — 5 мин, фильтруют (в случае соединения T h спиртовый фильтрат охлаждают и отделяют осадок гндрохлорида), к фильтрату добавляют равный обьем концентрированной соляной кисло5
10 l5
50 ты и через 16 ч (0 — 5" C) отфильтровывают осадок гидрохлорида 6,7-диаминоиндола. Этот осадок немедленно растворяют в 40 — 50 мл пиридина, прибавляют к полученному раство. ру 3 мл (0,025 моль) бензонлхлорида и оставляют при комнатной температуре на ночь. Затем полученную суспензию разбавляют
5-кратным объемом воды, подкнсляют соляной кислотой (рН 3 — 2), фильтруют, осадок промывают 5 o-ным раствором едкого патра, затем водой и высушивают в вакууме при о
80 — 90 С. Получают соединения Iк-р.
Пример 3, 6,7-дибензоиламиноиндол-.
-.2-карбоновая кислота (1с) .
2,2 г (0,01 моль) (1,2,5 (тиадиазоло) 3,4- g) нндол-7-карбоновой кислоты, 100 мл этанола и 6,5 г цинковой пыли нагревают до кипения, добавляют 20 мл разбавленной (1:1) соляной кислоты (порциями по 4 — 5 мл), кипятят 10 — 15 мин, фильтруют, к фильтрату добавляют 50 мл пиридина и 3 мл (0,025 моль) бензоилхлорида и оставляют при .комнатной температуре на ночь, Затем реакционную смесь разбавляют 5-кратным объемом воды, подкисляют соляной кислотой (pH 3-4) и через 16 ч (Π— 5 С) осадок отфильтровыо вают, промывают водой и высушивают в вакууме при 80 — 90 С.
Получают 1 г (22,9%) дигидрата 6,7-дибензоиламиноиндол-2-карбоновой кислоты (1с).
Пример 4. Этиловый эфир 6,7-дибенэоиламиноиндол-2-карбоновой кислоты (Trn).
2,5 г (0,01 моль)этилового эфира (1,2,5 (тиадиаэоло) 3,4- ч )-индол-7-карбоновой кислоты, 50 мл этанола и 6,5 г цинковой пыли нагревают до кипения, добавляют 20 мл разбавленной (1: 1) соляной кислоты (порциями по 4 — 5 мл), кипятят 3-5 мин, фильт- руют, к фильтрату прибавляют 50 мл пири дина и 3 мл (0,025 моль) бензоилхлорида и оставляют при комнатной температуре на ночь.
Затем реакциогпгую смесь разбавляют 5-кратным объемом воды, подкисляют соляной кислотой (pH 3-4), смолистый осадок отфильтровываюг, расгирают с разбавленным раствором аммиака, фильтруют, осадок промывают водой и высушивают в вакууме при 80-90ОС. Получают 2,2 г (47,5%) дигидрата этилового эфира
6,7-дибенэоил- амино индол- 2- карбоновой кислоты (Tm) .
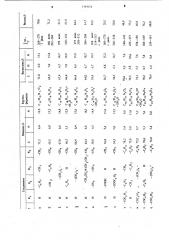
Выходы, температуры плавления и данные элементного анализа соединений 1и -rn приведены в таблице.
«оо :1 о
М
CA сг а.
О ) ф м
С)
С> м1
<> г о О сГ оО О г о м
Я
oow а ц > с.4 м о г4 в г
4s
6l о о
Ф м
Ф
O С» ц:> (о И
М
О оо
Ф гч !
С» г О оо гч оо
t,„. гч м г v м О . <р м а О И5
i !
Ф оо О
В О а сч с г
I (g М1
5о
Но
О оО
« . \ о г-" е" щ г г
QO Ф
О т3 С 4 ю
ch г чэ и О ч о со„г-„г л а, ь
° Ф Ф„чф С) (t О О . oo
° О О О О н а
oo, г
Z х фО ох х о о
cf ф
z z
\ 4 « х х ю
Z 4!
М х х
Мъ N
v о \
Я х
v о
vR! !О4
° б
OQ c г4
lA г4
О О оо оо а О оо т (р г «« Ф г а - м а л ц Оо оо г t с х х
EO сч оо г 1 оо а С г г оо 6 О м г4 г! o ! цс д, х х ф1 х
v ! х о
V х х
v o х
О х
СЧ о
I х х
v ! х
v I
N х
О
I х
v !
v ! х
v ! х
v !
kl
Ф ! v о о
l ( х о
О О о о
I х х х х х х
1 — — 4
I
Ф(51 с»
О х
Ф
v 4 и о о„ (4 ъ
О O х .х ц Ф о
t4
Р
Л ь х
\ о м о о
Z Z ь> о х хо м чт о с х х о
I х
И х Ф х
z o ч I х о х
I х
Z о х х х х v!
Ы х о о о! х х 8 х! х
v !
v" а а
С 4
I/l ф Ф
С 3
ill
Ф/Ъ («I
° °
О а мъ Ф„
М Ъ
IA
<4
ОО
С 4
lA о
v х
С (А х
v х
v х о О д
tV <
I со
Д а о
Ch и, 3/1 ч 1 и о о
Ф
z х хо
v оЖ т-Ч -< л о
Ch л ri С Ch а <ч р ж
I о
z хо ь
} 193|51