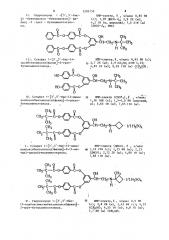
Способ получения производных аминоэтанола или их солей
Иллюстрации
Показать всеРеферат
Способ получения производных аминоэтанола общей формулы ОН vcai-CH2.-NH-Hi, КзО где R, - третбутил, циклобутил, 1-метипциклобутил; Rj,,Rj- бензоил, замещеиный в положении 4 гидроксилом, алкилкарбонилоксигруппой, содержащей 1-4 атома углерода в алкильиой части, бензоилоксигруппой, алкоксикарбонилом , содержащим 1-3 атома углерода в апкоксильной части,, или их солей, отличающийс я тем, что соединение общей формулы ОН сн-сн х, где R, и R имеют указанные значения , а X - галоид, подвергают взаимодействию с соединением общей формулы HN / i, где В.-имеет указанные значения; -водород, и выделяют целевой продукт в свободном виде или в виде соли. Приоритет по признакам 09.07.80при R,- трет-бутил 29.05.81при гщклобутил, 1-метиЛциклобутил.
СОЮЗ СОНЕТСНИХ
COINMI
РЕСПУБЛИК (19) (И) ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н IlATEHTY
0Н
СН вЂ” СН Х, г ю ф си — ыи-,, R3 трет-бутил, циклобутил, 1-метилциклобутил; бензоил, замещенный в положении 4 гндроксилом, алкнлкарбонилоксигруппой, содержащей 1-4 атома углерода в алкильной части, бенэоипоксигруппой, алкокгде К, Я,К
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 3419745/23-04 (62) 3308460/23-04 (22) 13.04.82 (23) 08.07.81 (31) 8022440; 8116440 (32) 09.07.80; 29.05.81 (33) СВ (46) 15.01.86. Бюл. В 2 (71) Актиеболагет Лрако (SE) (72) Отто Агне Торстен Олссон, Лейф Аке Свенссон, Кйелл Ингвар
Леопольд Веттерлин (БЕ) (53) 547.233.07(088.8) (56) Патент США Ф 4011258, кл. С 07 С 93/26, опублик. 1977. (54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
АМИНОЭТАНОЛА ИЛИ ИХ СОЛКИ. (57) Способ получения производных аминоэтанола общей формулы
R,o on
y)) 4 С 07 С 93/26 А 61 К 31/13 сикарбонилом, содержащим
1-3 атома углерода в алкоксильной части, или их солей, о т л и ч а ю щ и йс я тем, что соединение общей формулы где R и Я имеют укаэанные эначей 9 ния, а Х вЂ” галоил„ подвергают взаимодействию с соединением общей формулы б где R -имеет указанные значения;
Ц - водород, Ф и выделяют целевой продукт в свободном виде или в виде соли.
Приоритет по признакам
09.07.80 при К, — трет-бутил
29.05.81 при К, — циклобутил, 1-метиКциклобутил.
12057
Изобретение относится к получеа нию новых производных аминоэтанола, обладающих бронхоспазмолитической активностью, в частности к способу получения производных аминоэтанола общей формулы
0Н !
СН СИ2 1ЯИ 81 где Я, — трет.-бутил, циклобутил, 1-метилциклобутил, — бензоил, замещенный в по-, ложении 4 гидроксилом, алкилкарбонилоксигруппой, содержащей 1-4 атома углерода в алкильной части, бензоилоксигруппой, алкоксикарбонилом, содержащим 1-3 атома углерода в алкоксильной части, или.их солей.
Целью изобретения является способ получения новых производных аминоэтанола, обладающих бронхоспазмолитической активностью, с улучшенными свойствами.
Пример. Получение гицрохлорида 1 — (3,5 -бис(4-пивалоилокси25
30 снЗ о о
I Il снз — с — с — о — с — о ! с 3
СН3
СН3-С С-О- С-О ! Il II
С ИЗ О
ЯМР-спектр, 8, ч/млн.: 1,4 18Н (синг.), 1,5 9Н (синг), 3,2 2Н (м), 5,6 1Н (м), 7,7 11Н (м) (СССР, TMC).
Аналогично получают следующие соединения.
1 . Гидрохлорид 1- l3, 5 — бис 4 — изобутирилоксибензоилокси )—
58 2 бензоилокси)фенил)-2-трет-бутиламиноэтанола.
Раствор 3,2 r (0,005 моль) 1- (3
5 -бис(4-пивалоилоксибензоилокси) фенил)-2-бромэтанола и 1,1 r (0,015 моль) трет-бутиламина в
I00 мл хлористого метилена нагревают с обратным холодильником в течение 18 ч. После упаривания досуха к остатку добавляют простой диэтиловый эфир. Осаждаемый гидробромид трет-бутиламина фильтруют и упаривают досуха. Получаемый остаток растворяют в теплом изопропаноле, после чего добавляют 50 мл петролейноо
ro эфира с т.кип. 40-60 С. Размешивая, раствор охлаждают на ледяной бане. Образуется белый осадок, к которому через час добавляют петролейный эфир с т.кип. 40-60 С, Образующийся осадок собирают фильтрацией.
Получают 1,8 r (50Х) 1 — (3,5 --бис(4-пивалоилоксибензоилокси)фенил)?-трет-бутиламиноэтанола, который подкисляют этанольной хлористоводородной кислотой с последующим выделением целевого продукта (соединение Р 1).
Выход гидрохлорида 1,4 г (39K). он сн ! I
3 сн — сц;я — с,-сн нс
Н СН3
-фенил) — 2 — трет — бутиламиноэтанола.
ЯМР-спектр, о, ч/млн.: 0,85 9Н (синг.), 1,0 12Н (д), 1,6 (СР СОСО );
2,45 2Н (м); 2,8 2Н (м) ; 5, 15 1Н(д);
5,9 1Н (широкий), 7,35 11Н (м), (СЛ СОСЛ„ тмс).
Нс с — о си> сн, Hc — c— - о -c-o сн, о
QH I+3
СН-m -М-С-СН3
2а н сн, 1205758
О . О
С вЂ” О С-О
С вЂ” О (=0 — 1
0 0
HO c — О н сн,! н — сн;.и-с-сн
СН3
HO С— II
3
11. Гидрохлорид 1 -(3, 5 — бис1 4 -бензоилокси -бензоилокси)- фенил) -2 -трет — бутиламигоэтанола.
1 1 11, Сульфат 1 — (3,5 -бис-(4оксибензоилокси)фенил)-.2-третбутиламиноэтанола, 1V . Сульфат 1-(3,5 -бис-(4-пивалоилоксибензоилокси)фенил)-2-циклобутиламиноэтанола.
СН21 0
СНЗС СО/ СО
I си, сн, 1
СН,-С С вЂ” О- -C-0
II II
СНЗ О О
А
V . .Сульфат 1-(3,5"-бис-(4-пивалоилоксибензоилокси)фенил) -2-(1-метил)-циклобутиламиноэтанола.
СН3 о
СН>-С С-О- -С-О
СИЗ сн, l
/ сн;с с-о с-о
II — 11
СИ 0 О
V1. Гидрохлорид 1- (3,5 -бис(4-кярбоксиметилбензоилокси) фенил)2-трет-бутиламиноэтанола, ЯИР-спектр, 6, ч/млн.2 0,85 9Н . (с), 1,95 ДИСО- 4<, 2,9 2Н (м), 4,2 1Н (м, широкий); 7,4 21Н (м) (ДМСО-4„тМС). он Сн, CH-СН;Х-(-СН, H CH, ЯЙР-спектр, 6, ч/мпн.: 0,95 9Н (с);
2,7 2Н (м); 2,9 CD,0P; ЭОН 4,45;
4,85 1Н (м), 6,95 11H (M) (CLOD) .
2S ЯИР-спектр (CDCe ), f,,ч/мпн.:
1,36 18Н (с); 1,5-4,0 9Н (широкий, м); 5,65 1Н.(м), 7,65 11Н (м).
ОН 1/2Н2$0Ц
ЯМР-спектр (ДМСО), 6, ч/млн:
4р 1, 16 21Н (с); 1,55 6Н (м); 2,33 (ДМСО); 2,72 2Н (M); 4,80 1Н (M), 7,68 11Н (м). он снз
СИ-CH N И И,ЬО„
ЯИР-спектр, 6, ч/млн,2 0,9 9Н (с), 2,8 2Н (м), 3,45 6Н (с); 4,25 (СЮЗОН), 4,55 1Н (м); 6,8 ЗН (м);
7,7 8Н (м) (CD OI7) .
1205758
1g си) фенил1- 2 — трет — бутиламиэтанола.
<фармакологические опыты. 20
1. Исследуемые соединения растворяли в 8 мл дистиллированной воды и давали орально собакам весом 1318 кг при помощи трубки с последующей дачей 6 мл воды.(за ночь до на- 25 чала эксперимента собакам не давали корм) °
Кровь бралась из подкожной вены плеча передней ноги при помощи вакуум-трубок. К крови добавляли ин- 1р гибитор эстеразы — диизопропилфторфосфат, пробы центрифугировали при о э С с последующим определением содержания тербуталина в плазме (содержание тербуталина в сыворотке указывает на степень бронхоспазмолитической активности исследуемых соединений).
Исследуемые соединения давали в количестве, обеспечивающем содер- 4О жание тербуталина в сыворотке, равное по меньшей мере 2 нг/мл, Зто содержание должно сохранять=я по меньшей мере в течение б ч для обеспечения эффективной бронхо- 4 спазмолитической активности.
Для сравнения применяли извест(( ные соединения: 1-(3,5 -дипивалоилэксифенил)-2-(трет-бутиламино)этанол (А) и торговый продукт тербуталин — 1-(3,5-диоксифенил)-2трет-бутиламиноэтанол (Б).
Для каждого исследуемого соединения определяли срок эффективной бронхоспазмолитической активности
Соединение
1 — основание
1 — НСР
12,3
12,5
11,8
IЧ
Ч 71 . Сульфат 1 — (3, 5 — бис — (4 -бензолоксибензоилок
Ч1 12,1
Ч 13,4
А 9,5
Б 8,0
Как видно из приведенных данных новые соединения имеют больший срок эффективной бронхоспазмолитической активности, чем известные соединения. Новые соединения имеют ту же токсичность, что и известные соединения, т.е. ) 1000 мг/кг мыши (орально). Их терапевтическая доза составляет 0,05-250 мг.
1i. Исследуемые соединения растворяли в 8 мл дистиллированной воды и давали орально собакам весом 1318 кг при помощи трубки с последующей дачей 8 мл воды. Исследуемые соединения давали в дозах, обеспечивающих бронхоспазмолитическую активность. При этом до и после дачи исследуемых соединений измеряли частоту сердцебиений в минуту. JTocле дачи исследуемых соединений наблюдали повышение частоты сердцебиения и определяли время, через которое повышение частоты сердцебиения состав,пяло менее 1О биений в минуту. Чем больше срок повышенной частоты сердцебиения, тем больше срок активности исследуемых соединений.
Для сравнения применяли те же известные соединения, что и в опыте 1.
Время, через которое повышение частоты сердцебиения составляет менее 10 биений в минуту, ч:
Соединение
Ш 26
А 23
Б 22
Составитель Л.Иоффе
Редактор Л.Веселовская Техред T.Òóëèê
Корректор, О.Луговая
Заказ 8548/61 Тираж 379
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, W-35, Раушская наб., д. 4/5
Подписное
Филиал ППП "Патент", r. ужгород, ул. Проектная, 4
1205758 8
Как видно из приведенных данных, . бронхоспазмолитической активности, новое соединение 1П имеет больший срок чем известные соединения.
I !