Реактив для электрохимического изолирования неметаллических фаз из аустенитных сталей
Иллюстрации
Показать всеРеферат
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИН,51, 4 С О1 И 1/32
j Р
ОПИСАНИЕ ИЗОБРЕТЕНИЯ "8 н a4lQpCHOMV СЕИДЕТЕГЬСТВУ
I у/
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 3763149/22-02 (22) 28.06.84 (46) 28.02.86. Бюл. и 8 (72) М.Н. Образцова, М.Г. Киткина, Н.П. Капитонова и В.В. Обуховский (53) 620. 186. 14:669. 15(088.8) (56) Фазовый состав, структура и свойства легированных сталей и сплавов/Под ред. С.3. Бокштейна, M.:, Машгиз, 1965, .с. 181.
Физико-химический фазовый анализ сталей и сплавов /Под ред. Н.Ф.Лашко, Л.В. Заславской и др. М.: Металлур-. гия, 1978, с. 115. (54) (57) РЕАКТИВ ДЛЯ ЭЛЕКТРОХИИИЧЕСКОГО ИЗОЛИРОВАНИЯ НЕМЕТАПЛИЧЕСКИХ
„„SU„„1215016 А
ФАЗ ИЗ АУСТЕНИТНЫХ СТАЛЕЙ, содерхащий метанол и соляную кислоту, отличающийся тем, что, с целью полного изолирования нитридных и карбонитридных фаз и исключения загрязнения изолируемых фаз продуктами вторичных реакций, происходящих на аноде, он дополнительно содермит бромнд аммония и зтиленгликоль при следующем соотношении компонентов:
Соляная кислота (1-1,19 г/смэ),мл 50-55
Бромид аммония, г 25-30
Этиленгликоль, мп 20-25
Метанол, мп 1000
4 1215016 2
15
-20
30
50
Изобретение относится к области фазового анализа азотсодержащих аусте-. нитных хромомарганцевых сталей, легированных медью.
Цель изобретения — полное изолирование нитридных и карбонитридных фаз и исключение загрязнения изолируемых фаз продуктами вторичных реакций, происходящих на аноде.
Электрохимическое изолирование нитридных и карбонитридных фаэ из азотсодержащих аустенитных хромомарганцевых сталей, легированных медью, в предлагаемом реактиве должно проводиться при плотности тока
О, l2-О, 15 A/см . Температура 0-4 С, продолжительность элекролиза 3040 мин.
Введение в реактив бромида аммония в количестве 25-30 г создает усло вия одновременного и равномерного электрохимического растворения компонентов твердого раствора сплава и достаточную концентрацию для связывания образующихся в процессе электролиза ионов меди в растворимые в метаноле комплексы. Введение бромида аммония в состав реактива в количестве 25-30 г определяется тем, что при более низких содержаниях не устраняется реакция диспропорционированйя, в результате которой происходит попадание частиц меди в осадок, при более высоком содержании бромида аммония в процессе электролиза происходит накопление солей в растворе, что затрудняет проведение фазового анализа стали.
Введение в реактив этиленгликоля в количестве 20-25 мл позволяет интенсифицировать процесс электрохимического растворения азотсодержащих аустенитных хромомарганцевых сталей с медью и повысить плотность тока при электролизе до 0,12-0,15 А/см,,что дает возможность увеличить производительность труда в 1,5 раза.
Введение в реактив этиленгликоля в количестве 20-25 мл определяется тем, что при количестве менее 20 мл не достигается полирующий эффект, электрохимическое растворение исследуемых образцов стали происходит недостаточно равномерно, а при содержании этиленгликоля свьппе 25 мл заметно увеличивается сопротивление раствора электролита, электролит в процессе электролиза сильно разогревается.
Более высокие плотности тока нецелесообразны, так как в процессе электролиза также происходит сильное разогревание раствора электролита и исследуемого образца.
Фазовый анализ был проведен для стали марки 06Х17Г17ДАИБ, в предлагаемом реактиве, состав которого приведен в табл.
Реактив готовили растворением химически чистых реагентов бромида аммония и этиленгликоля в метиловом спирте, в который добавляли соляную кислоту (уд. в. 1, 19). Электрохимическое изолирование нитридных и карбонитрндных фаз проводили при плотности тока 0,12-0,15 А/см . Темо пература 0-4 С, длительность 3040 мин.
Полученные анодные осадки отмывали от электролита метиловым спиртом, водой и обрабатывали смесью азотной и серной кислот (10:1). Растворы выпаривали до появления паров
ЯО разбавляли дистиллированной водой и переносили в мерные колбы.
В полученных растворах определяли содержание железа, марганца, хрома, молнбдена, ниобия и меди по обще-, принятым в аналитической химии методикам.
После выполнения химического анализа рассчитывали массовый процент каждого элемента в фазовом осадке и суммарное содержание элементов в осадке.
Изучение структуры изолированных фаз осуществляли рентгеноструктурным методом на анодных осадках, выделенных с параллельных образцов. Исследование проводили на установке УРС60 в медном С и К -излучении. Идентификацию фаз проводили по картотеке ASTM.
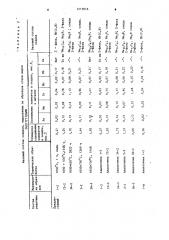
Результаты анализа приведены в табл. 2.
Предлагаемый реактив обеспечивает полное и количественное электрохимическое изолирование нитридных и карбонитридных фаз из аэотсодержащей аустенитной хромомарганцевой стали, легированной медью, равномерное растворение основы стали, а также повышение производительности труда в 1,5 раза вследствие повьппения плотности тока прн электролизе.
1215016
Таблица 1
Содермание компонентов
Состав реактива
Метанол, мл
Бромид аммония, г
Этиленгликоль, мл
Предлагаемый
1000
25
22,5
1000
52,5
27,5
1000
25
Известный
Глицерин
100
I
Использование предлагаемого реактива обеспечивает по сравнению с из-, вестным более полное изолирование нитридных и карбонитридных фаз
MeqN, Z — фазы, Nb(C,N) и Ме зС6 из оляная кисота (j=
1, 19 г/см ) аустенитных хромомарганцевых сталей, легированных медью, что позволяет повысить качество и достоверность фазового анализа исследуемых
5 сталей.
Лимонная кислота
Ф
Ц
td
1л к с
5 л
Х л
О а
v о
Ч5 х л
О к еч
Х
О
° v л
Ф
Щ
° е
I л
Э д
О m д ф
Ф Р
° л
Ч1 3
u m
Ф !
Ф д
u m в Ф
С4 тв
Ф 1
Х !Ч
О
CV
Ф й
Ф
Н о л О л
Ю
СЧ л
СЧ
СЧ л
D л л
00 л
00 л
СЧ л ь
СЧ л
Ю л
Ю л
СЧ л ь
СЧ л
Ю л
D л ь л
Ю л
ЯЬ
О л
СЧ
D л
СЧ
О л
СЧ
Ю л
Ю л ь
Ю л.Ю л
00
Ю л
Ю О
Ю л
»
Ю
СО л
00 л
D ь л
СЪ л л
С Ъ
Ю л ь
ОЪ л
СЧ л
СЧ
Ю л
СЧ
Ю л
ОЪ
Ю л
Ю л
РЪ ь л
00
Ю л ь (РЪ
Ю л ь
С Ъ л
Ю л
Ю л
Ю л
"В и=. !
Ф о
СЧ
D л
С Ъ л
СЧ
О л
СЧ
Ю л
СЧ л
D л ь
СЧ л ь
СЧ л
О л
C4
С!Ъ л
Ф
СЧ . л лл
СЧ л
Ю л
СЧ л
РЪ л л
СЧ л
КР
СЧ л
Ю л
СЧ
p I,00
С Ъ
С Ъ л
О о
Ю и
К0
3 о
В(В л
0 л
СЧ
СЧ
СЧ
CV л
СЧ !
СЧ
О о
Ю
МЪ
+
Ю
МЪ
D и о
Ю О
D
МЪ
О
Э
Ю
Ю л
О иЪ
5
О
Р
О мЪ
С1
+ ь
С Ъ
СЧ л
СЧ
СЧ
СЧ
РЪ
СЧ
СЧ
СЧ
СЧ
12
1 0 cd
I И й
О Ф
u o л о
Ж Q !
С
Е
Ж л ж
И о
6) IC
Ц ос
aj
E о
3 е!
Ц л
О Ф
Е» И
dI g o g Q °
ФОФ
1215016
Ц
Д
R
»» ю 3
u m
Ф!1
R л
О
g л
1 и о О Я Cd
um m
Ф . ! с4 ж
4 и о
° л к м
kf
Э
Ц о л
Э
K ю 3 о m
cq CII
4l Р м
Э 73
u m оФ
g4 Е (U I
X ы.1
1 л
1 ь
СЧ л о
СЛ л о
СЧ л о
С4 л о
ОО о л о л о л
D л ь л ь л о и о
Ф о
С ) О1 л
О л о
Ф л
C.
1 и
ОЭ
D л о
CIÎ о л ь
3/Ъ л
< 3 л
О х х
CCI
И
Cf о (Э ("Ъ л о х х
Щ
И
С4
Ф о.1
1
1
1. О С Ъ х о
Р х
Ы
С4
CV л
1 ф; !
1 Ф
1 Е
1
Е
О о о
Е
5
cII 1
Э 1
1 Р 1
Щ л о е хб
III 63
Ц °
eOVI
1» е
1
I
1
I
1 з
1
1
1
1о
В 1 йй
1215016
lC Э 1
Р О iK
4 М g4
&ю х
33" ер5
С4 3 g
3 к о хе х Р
ClI I Q
f4Þ A
IO O Ct о е л g о м
Д Э 0 оре