Способ получения растворов сахаров
Иллюстрации
Показать всеРеферат
СООЭ С08ЕТСНИХ
РЕСПУБЛИК
Ш4С13К102
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
ГОСУДАРСТЯЕННЬЗЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (2i) 3782883/28-13 (22) 15.08.84 (46) 30.08.86. Бюл. № 32 (71) Ордена Трудового Красного Знамени институт химии древесины (72) P.Ã. Каткевнч, О.Б. Иитченко и И.Е. Гневашева (53) 633.534(088.8) (56) Патент ГДР ¹ 155681, кл. С 13 К 1/02, 1978.
Тоуааа N., 0gava K. — Biotechaol.
Bioeng. Symp. 1975, № 5, 225-244.
„SU„„1254012 А 1 (54)(57) CIIOCOF ПОЛУЧЕНИЯ РАСТВОРОВ
САХАРОВ, предусматривающий ферментативный гидролиз полисахаридного сырья в буферной среде, состоящей из уксусной кислоты и соли слабой кислоты в концентрации О 05-0,1 И, с введением консерванта, отличающийся тем, что, с целью упрощения процесса и повышения качества целевого продукта, в качестве соли слабой кислоты и одновременно консерванта используют бенэоат натрия.
I 12
Изобретение относится к биохимическому получению пищевых и кормовых сахаров из растительного сырья и преимущественна может быть использована
9 гидрализнай и микробиологической промышленности.
Цель изобретения — упрощение процесса и повышение качества целевого продукта.
Способ осуществляют следующим образом.
Качество буфера определяют буферной емкостью р которая характеризует способность раствора сохранять постоянное значение рН при добавлении к нему кислоты или основания. 0,050,1 И раствор, состоящий из смеси бензоата натрия и уксусной кислоты, имеет высокое значение р (максимальное значение р по отношению к НС1 при рН 4.,8 составляет 0,051, а по отношению к NaOH при рН буфера 4,2 значение равно 0,047), что приравнивают предлагаемый буфер к широко употребляемому буферу, состоящему из ацетата натрия и уксусной кислоты. Кроме того, 0,1 M и тем более 0,05 M раствор буфера„ состоящий из бенэаата натрия и уксусной кислоты, при значении рН ч-5 не снижает активности геми целлюлаэных и целлюлаэных ферментов, имеющих оптимальные эначенин рН-действия в этом интервале. Это огределяо ет возможность использования предлагаемого буфера для поддержания значения при рН при ферментативном гидролиэе палисахаридов. Бензоат натрия является кансервантом, что предохраняет реакционную среду, в которой проходит ферментативный гидролиз растительного сырья, ат микробного заражения.
Для получения буферного раствора берут от 0 05 до 0,1 М раствор уксусной кислоты и бенэоата натрия, так как.при употреблении буфера ниже этой концентрации он не проявляет стабильное консервирующее действие, а выше —— нестабилен ввиду выпадения бензойной кислоты при низких значениях рН, Для определения объемньгх соотношений растворов выбранной молярности компонентов буфера и получения требуемого значения рН, которое определяется применяемым для гидролиэа комплексом фермента, компоненты взаимно титруют до получения тр=áóåìîãî рН буферного раствора. Таким образом, 54012 3 можно составить таблицу для определе" ния взаимных соотношений малярных растворов бенэоата натрия и уксусной кислоты, обеспечивающих любые искомые значения рН (см, табл. 1).
Дальнейшим этапом подготовки реакционной среды к ферментативному гидропиэу является включение в буферный раствор фермента и субстрата, количество которых определяют < конкретным случаем. Ферментативный гидролиз проводят в ферментерах в статических условиях, в реакторах, снабженных диалиэирующей мембраной для отвода ниэкомолекулярных продуктов реакции,или в ферментерах колоночного типа с не- . ограниченной продолжительностью без опасности заражения реакционной среды или отобранных растворов сахаров микроорганизмами.
Пример 1. 1,0 г соломы с размерами частиц меньше 2 мм и влажностью 67., обрабатанной 1,0Х-ным раствором NaOH помещают в колбу на 200 Мл с резиновой пробкой. Для осахаривания этого субстрата используют ферментный комплекс целлокандин, имеющий оптимальное действие при значении рН 5,0, Сначала приготавливают буферный раствор, состоящий иэ ч3,5 мл О, 1 И раствора бенэаата натрия и 6,5 мл
О, 1N уксусной кислоты. Для перевода
0,1 М раствора в 0,05 И к приготовленному раствору прибавляют равное количество (50 мл) дистиллированной воды, имеющей значение рН 6,5; 1,0 г фермента растворяют в приготовленном буфере путем медленного перемешивания в течение 10 мин магнитной мешалкой, потом нерастворимую часть фермента отделяют на стеклянном фильтре. Приготовленный ферментный раствор, имеющий значение рН 5,0, наливают на субстрат, колбу закрывают и помещают в
7åðìîñòàò при 10 С. В начале и в конпе опыта измеренное значение рН реакггионной спелы равно 5,0+0,2. Через
3, 6, 2ч и 168 ч колбу вручную встряхивант и отбирают пробы в количестве мл, которые немедленно прибавляют к 2 мл дисктилпированной воды, нагретой до 98 С, и выдерживают 10 мин на водяной бане для инактивации фермента.
В такай пробе, учитывая трехкратное ее разбавление, определяют количество редуцирующих веществ методом Шомодьи и подсчитывают их количество на абсолютно сухой исходный субстрат..1 125
Таким образом параллельно станят три опыта. Количество PB после 3 ч составляет в параллельных опытах 14,2, 18,6 и 21,47, после 6 ч — 35 9 33,6 и 37,3 ; после 24 ч — 52,9, 46,8 и
52,47; 168 ч — 68,9, 71,6 и 70,37. соответственно (см, табл. 2,среднее значение опыта 4).
Пример 2. Осуществляется аналогично примеру 1, концентрация 20 используемого бензоатного буфера составляет 0,1 И. Выход PB через 3, 6, 24 и 168 ч гидролиза составил соответственно 13,6, 34,9, 52,5 и
70,6Х (приведено среднее значение, 25 см табл. 2, опыт 3).
Пример 3. Субстратом является ксилан, выделенный из овса, а ферментом - ксидавомарин Г-10Х,имеющий оптимум действия при рН среды, 20 равном 4. Приготавливают 100 мл
0,1 И буферного раствора, имеющего рН 4,0, смешиванием 79,2 мл О, 1 М раствора уксусной кислоты и 20,8 мл
0,1 M раствора бензоата натрия, до- 25 бавляют 0,1 r фермента и 0,1 г субстрата, перемешивая все компоненты
10 мин магнитной мешалкой, Приготовленная реакционная среда имеет рН
4,0. Аналогичным образом, как в при- 30 мере 1, закрытая колба помещается s термостат при 40 С. Через 3, 6, 24 и
168 ч отбирают пробы для анализа и измеряют рН среды. Значения рН в трех параллельных опытах во время непре- 35 рывного гидролиза составляет 4,0+0,2, Количество PB после 3 ч составляет в трех. параллельных опытах 21,1, 29,7 и 28,1Х; через 6 ч — 46,8, 49,6 и
55 2Х; 24 ч — 56 9, 62 4 и 63,97;
168 ч — 73,6, 67,6 и 74,27. соответст-. венно (см. табл. 2, среднее значение опыта 7).
П р и и е р 4. Осуществляется аналогично примеру 3, концентрация используемого ацетатного буфера составляет 0,05 М. Выход PB (средние значения) через 3, 6, 24 и 168 ч составляют соответственно 27,5; 50,7;
64,9 и 72,17. (см. табл. 2, опыт 8), Пример ы 5 6. Проводят ферментативный гидролиэ в 0,05 И ацетатном буфере, приготовленном известным способом,со значением рН 5. Субстрат и фермент, а также их концентрация —, 4012 4 такие же, как н примере 1, Опыт проводится по примеру 1, но как консервант применяется толуол. Расход толуола на 100 мл реакционной среды—
5 мм.Выход PB в трех параллельных опытах после 3 ч составляет 15,3, 19,1 и 16,07; 6 ч - 33,2, 36,6 и 32,97.
24 ч — 59,4, 51,3 и 46,87; !68 ч—
64,8, 67,4 и 60,17 (cM, табл. 2, средние значения опыта 2).
Аналогичный эксперимент осуществляют в 0,1 М ацетатном буфере. Выход
PB (средние значения) через 3, 6, 24 и 268 ч составил соответственно 23 О, 33,9, 49,5 и 60,5Х (см. табл. 2, опыт 1) .
Пример ы 7-8. Осуществляются аналогично примеру 3. Согласно прототипу гидролиз проводят в 0,1 М ацетатном буфере (рН 4) с добавлением толуола (5 мл/100 мл реакционной смеси). Выход PB (средние значения) через 3, 6, 24 и 168 ч составил соответственно 25,9, 53,9, 64,5 и
66,37 (см. табл. 2, опыт 5).
Аналогичный эксперимент осуществляют в 0,05 М ацетатном буфере. Выход
PB (средние значения) через 3, 6, 24 и 168 ч составил соответственно 26,9, 55,9, 62,2 и 69,3Х (см. табл..2, опыт 6).
Таким образом, для составления реакционной среды создания требуемого значения рН среды и ее консервирования по предлагаемому способу требуются только компоненты буфера, что обеспечивает упрощение процесса гидролиза.
Присутствие бензоата натрия н среде ферментативного гидролиза полисахаридсодержащих субстратов не снижает активности ферментов, а в некоторых случаях даже способствует повьппению выхода PB по сравнению со средами, содержащими ацетатный буфер и толуол.
Полученные растворы сахаров в присутствии бензоата натрия не содержат токсичное соединение — толуол, что поньппает их качество, и поэтому могут быть использованы для кормовых и пищевых целей без особой очистки, так как бензоат натрия допущен, как консервант, в пищевой и кормовой промышленности.!
254012
Таблица 1 рН (20 С) 0,1 М бензоат натрия„ мл
О,! И уксусная кислота, мл
Содержа"ие бензоата в буферной смеси, 7.
По НС1
25,0
0,06
1 э!2
3,4
63,0
5,0
0,22
3,6
5 0
32,0
20,0
76 0
0,30
4,0
20,0
20,0
38,0
4,2
0,50
0,027
0,038
22,0
4,4
0,66
20,0
11,0
0 93
20,0
6,0
20,0
3,0
1,25
5,0
5,2
20,0
1,9
5,4
20,0
20,0
1,37
0,7
1,44
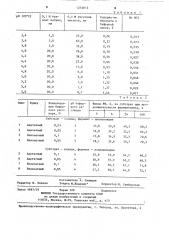
Таблица 2
Выход РВ, 7, на.субстрат при продолжительности ферментолиза, ч рН буферного ðàствора
Концентрация буфер ного растsopa, И
Опыт Буфер .
6 1 (24 168
0,01
13,0
33,9
49,5
60,5
64,2
0,05
16,8
34,2
52,5 о,!
34,9
13 6
18,1
52,5
70,6
0,05
35,6
50,7
70,3
0,1
25 9
64,5
53в9
66,3
26,9
55,9
62,2
69,3
0,1
0,05
26,3
27,5
50 5
5Q,7
71,8
64,9
72,1
Составитель A. Синицын
Техред N.Ходанич Корректор М. Самборская
Редактор Л. Повхан
Заказ 4687!29
Тираж 328 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва„ Ж-35, Раушская наб ., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
1 Ацетатный
2 Ацетатный
3 Бензоатный
4 Бензоатный
5 Ацетатный
6 Ацетатный
7 Бензоатный
8 Бензоатный
Субстрат — солома, фермент — целлокандин
Субстрат -- ксилан, фермент — ксилавомарин
0,013
0,013
0,015
0,019
0,046
0,051
0,048
0,040
0,029
0,021