Способ получения производных дигидропиридина (его варианты)
Иллюстрации
Показать всеРеферат
1. Способ получения производных дигвдропИрйдина общей формулы Be Вз -А--цГ)н-(СШп-АР {) (Ь2Ъ , где R, , R и R одинаковые или разные и каясдый из них - алкил, циклоалкил или алкоксиалкил; одинаковые или разные и каждый из них - водород , галоген, нитрогруппа, трифторметильная группа, алкил, циклоалкил , алкоксигруппа, цианогруппа, алкоксикарбонильная группа или алкилтиогруппа; RJ - водород, алкил, циклоалкил , аралкил, арип или А - алкиленовая группа; Аг - арильная или пиридильная группа; m - целое число 1-3; п - простое целое число О 2, отличающийся тем, что на соединение общей фopмyJa l СО /СООНг 1 IV) где R, и Rj имеют указанные значения, действуют аммиаком, образовавшийся продукт подвергают взаимодействию с соединением общей формулы (V) и с соединением общей формулы ы СОО-А-Ъ1(СНЪ-АГ - iCHjb (VI)
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИК
ОЭ (ll) SU
А3
1бц 4 С 07 D 211/90 401 14
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н flATEHTV
O (Ц) или N (53) 54? . 822. 3. 07 (088, 8) (56) Патент ФРГ - 2995772, кл. С 07 D 211/90, 1980.
C008g
О R1
00-А- - (QOy,-At (j ) (Зъ в6 где R,, к и R>
Я5
Rl, X (ч) R u R
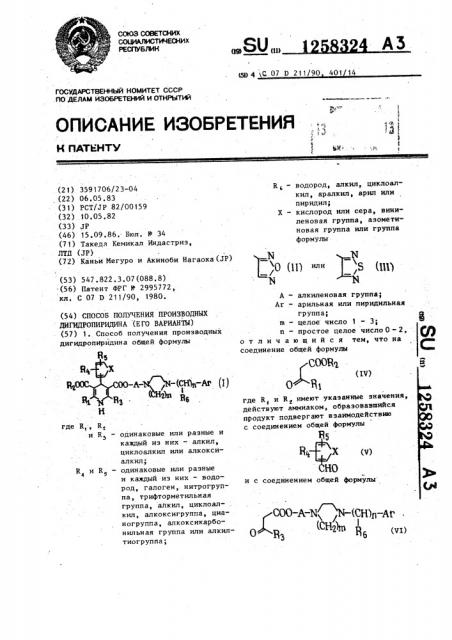
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР . ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТНРЫТИЙ (21) 3591706/23-04 (22) 06.05.83 (31) РСТИР 82/00159 (32) 10.05 82 (33) 1Р (46) 15.09,86. Бюл, Ф 34 (71) Такеда Кемикал Индастриз, ЛТД (3P) (72) Каньи Иегуро и Акиноби Нагаока(1Р) (54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ДИГИДРОПИРИДИНА (Е ГО ВАРИАНТЫ) (57) 1. Способ получения производных дигидропиридина общей формулы
Rg одинаковые или разные и каждый из них — алкил, циклоалкил или алкоксиалкил; одинаковые или разные и каждый из них — водород, галоген, нитрогруппа, трифторметильная группа, алкил, циклоалкил, алкоксигруппа, цианогруппа, алкоксикарбонильная группа или алкилтиогрупла;
R — водород, алкил, циклоалкил, аралкил, арил или пир идил;
Х вЂ” кислород или сера, винилен ов ая группа, аз оме тиковая группа или группа формулы
А - алкиленовая группа;
Ar — арильная или пиридильная группа;
m — целое число 1 — 3;
g и — простое целое число Π— 2, Q) отличающийся тем, что на соединение общей формулы где R u R имеют указанные значения, 1 действуют аммиаком, образовавшийся продукт подвергают взаимодействию с соединением общей формулы и с соединением общей формулы -(сн)п-АГ
О 8 (сн2Ъ В
12583
3 .фх
СНО (v) Н где R<,R и Кэ— сООН 1
К4и К.R
6 где К,, К и R
4 " % (Ц) или
К6 где К, К, R, ß
Х,А,ш и и имеют указанные значения, 2. Способ получения производных дигидропиридина общей формулы одинаковые или разные и каждый иэ нихалкил, циклоалкил или алкоксиалкил; одинаковые или разные и каждый иэ них— водород, галоген, нитрогрупна, трифторметильная группа, алкил, циклоалкил, алкоксигруппа, цианогруппа, алкоксикарбонильная группа или алкил тиргруппа; водород, алкил, циклоалкил, аралкил, арил или пиридил; кислород или сера, виниленовая группа, азометиновая группа или группа формулы
А — алкиленовая группа;
Ar — арильная или пиридильная группа;
m — целое число — 3;
n — простое целое число
0-2, о .т л и ч а ю шийся тем, что на .соединение общей формулы соо-А-,, -(сн).-л, 3 б гд(К>, R4, А, m и и имеют указанные значения, 24 действуют аммиаком, образовавшийся при этом продукт подьергают взаимодействию с соединением общей формулы и с соединением общей формулы
R(, К i R4, R и К имеют указанные эна9 чения.
3. Способ получения производных дигидропиридина общей формулы
Я»
Rg СОО A Ì (((H)((( ((, „э, () одинаковые или разные и каждый из них - алкил, циклоалкил или алкоксиалкил; одинаковые или разные и каждый иэ них — водород, галоген, нитрогруппа, трифторметильная группа, алкил, циклоалкил, алкоксигруппа, цианогруппа, алкоксикарбонильная группа или алкилтиогруппа; водород, алкил, циклоалкил, аралкил, арил или пиридил; кислород или сера, виниленовая группа, аэометиновая группа или группа формулы
A — - алкиленовая группа;
Ar — арильная или пириднльная группа;
1258324 соо, {тЧ) 1 (Ч) c008 (} р (zv) А- -(Саь-Ar
/ 6 {<) где К,, К и R
-(СН) д-At
1m R (Ч|) !
О 5
COO-Ао. ц, m - целое число 1 - 3;
n - простое целое число 0- 2, отличающийся тем, что.на соединение общей формулы
С00-л-ъ, Б — (CH)ä-Аг
О 8 (CH2) 8 (vI) 6 где К5» » А»
m и п имеют указанные значения, действуют аммиаком, обазовавщийся при этом продукт обрабатывают соединением, полученным при взаимодействии соединения общей формулы
8g с соединением общей формулы
Где R<» R<». »
R и Х имеют укаэанные зна5 чения.
4. Способ получения производных цигидропиридина общей формулы одинаковые нли разные и каждый из них - алкил, циклоалкил или алкокси алкил; одинаковые или разные и каждый из них — водород» галоген, нитрогруппа, трифторметильная группа, алкил, циклоалкил, ал.коксигруппа, цианогруппа, алкоксикарбонильная группа илн алкилтиогруппа;
R — водород, алкил, циклоалкил, аралкил, арил или пир идил;
Х вЂ” кислород или сера, виниленовая группа, аэометиновая группа или группа формулы
А — алкиленовая грУппа;
Ar - арильная или пиридильная группа;
m - целое число 1 - 3;
n - простое целое число О - 2, отличающийся тем, что на соединение общей формулы где R и R имеют указанные значения, действуют аммиаком, образовавшийся при этом продукт обрабатывают соединением, полученным при взаимодействии соединения общей формулы с соединением общей формулы где R5» К R5» Rg
Х, А, m и п имеют указанные значения, 1 1258
Изобретение относится к области получения новых производных дигидропиридина общей формулы (I) где К,, К К и R — одинаковые или разные и каждый из них - алкил, циклоалкил или алкоксиалкил;
К4 и Кз — одинаковые или разные и каждый из них — водород, галоген, нитрогруппа, трифторметильная группа, алкил, циклоал" кил, алкоксигруппа, циа- 20 ногруппа, алкоксикарбонильная группа или алкилтиогруппа;
R — водород, алкил, циклоалкил, аралкил, арил или пиридил;
Х вЂ” кислород или сера, виниленовая группа, азометиновая группа или группа формулы (Т1) 30 или (I II ) А — алкиленовая группа;
Аг — арильная или пиридильная группа;
40 ш — целое число i - 3; п - простое целое число 0- 2.
Цель изобретения — разработка на основе известных методов способа получения новых производных дигидропиридина, обладающих выраженным сосудо" расширяющим действием и низкой токсичностью
Пример 1 Смесь м -нитробензальдегида (2,66 г),, 2-(4-бензгидрил1-пиперазинил)этилацетоацетата (6,09 r), метил-3-аминокротоната (2,03 г) и изопропилового спирта (25 мл) кипятят с обратным холодильником в течение 6 ч. Затем растворитель отгоняют и остаток очищают колоночной хроматографией на силикагеле (250 г) при использовании в качестве
324 2 элюента системы растворителей гексанэтилацетат (i:1) . Полученное в результате маслянистое вещество растворяют в небольшом количестве изопропилового эфира и при охлаждении на ледяной бане и перемешивании прибавляют к полученному раствору гексан.
При этом происходит выпадение порошкообразного осадка (7,35 г; 75,27. от теории} 2-(4-бенэгидрил-1-пиперази1 н ил) э тил-ме тил-2, 6-диме тил-4- (3 "н итрофени) -1, 4-дигидропиридин-3, 5-дикарбоксилата. Часть этого порошкообразного продукта перекристаллизовывают из смеси изопропиловый эфир— гексан, получив в итоге светло-желтое кристаллическое вещество с т.пл.
1О2-104 С.
Спектр протонного магнитного резонанса (ПИР-спектр) в дейтерированном хлороформе (CDCl>) P 2-26-2,49 (8Н, мультиплет); 2,33 (6Н, синглет);
2,57 (2Н, триплет, J=6); 3,60 (ЗН, синглет); 4,15 (2Н, триплет, J=6);
4,IS (2Н, синглет); 5,08 (1Н, синглет); 5,77 (1Н, синглет); 7,118,12 (14Н, мультиплет).
Вычислено, 7: С 68,83; Н 6,27;
Н 9,17.
С„Н„1,0
Найдено, 7: С 68,97; Н 6,27;
И 9,.05.
Полученное таким образом свободное основание (3,90 г) растворяют в дихлорметане (10 мл) и к этому раствору прибавляют небольшой избыток раствора хлористого водорода в диоксане. После охлаждения на ледяной бане к реакционной смеси прибавляют несколько капель воды и перемешивают ее также при охлаждении на ледяной бане. Образовавшийся при этом кристаллический осадок отделяют фильтрованием и промывают диэтиловым эфиром, в результате чего получают желаемый 2-(4-бензгидрил-1-пиперазинил)этил-метил-2,6диметил-4-(3-нитрофенил)-1,4-дигндропиридин-3,5-дикарбоксилатдигидрохлорид с выходом 4,23 r (94,47 от теории). Этот продукт растворяют в дихлорметане, содержащем небольшое количество метанола. Затем растворитель отгоняют, остаток растворяют в этил". ацетате и после прибавления воды смесь оставляют выстаиваться на ледяной бане. Результатом процедуры пефекристаллизации является получение
1258 светло-желтого кристаллического продукта, имеющего т.пл. 167-170 С.
Вычислено, Х: С 59,90; Н 6,03;
N 7,99.
См Н м Иа О 2НС1 Нг О 5
Найдено, Х: С 60,06; Н 5,97;
N 7,84.
Пример 2. Смесь м -нитробензальдеrида, 2-(4-бензгидрил-1-пиперазинил)этилацетоацетата и этил-3-аминокротоната нагревают в изопропиловом спирте в режиме кипячения с обратным холодильником аналогично примеру 1, в результате чего получают 2-(4-бенз1 идрил-1-пиперазинил)этил-этил-2,6- 5 диметил-4-(3-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразного вещества с т.пл, 80-82 С (спекание). ВыР ход продук та 48, ЗХ от теоре тически возможного.
Инфракрасный спектр (ИК-спектр), снятый для дисперсии продукта в вазелиновом ма"ле, см : 3320, 1695, 1680. 25
ПМР-спектр (CDC1>), 8: 1, IS (ЗН, триплет, J=6, -СНг СЙз); 2,33 (6Н, синглет, =("-СНа); 4,08 (2Н, квадруплет, .1-6, -CH-СН. ); 4.,15 (2Н, триплет, J6, -СООСН-СН -); 4,18 (IН, синглет, 30
М-СН ); 5,08 (1H, синглет, С< -H);
5,79 {1Н, синглет, ИН).
Вычислено, Х: С 69,21; Н 6,45;
N 8,97.
Сз Нао ИаО
Найдено, Х: С 68,81; Н 6,63;
N 8,72.
Пример 3. Смесь о -нитробензальдегида, 2-(4-бен згидрил-1-пиперазинил) этилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте аналогично примеру 1, затем полученный продукт обрабатывают метанольным раствором хлористого водорода, получив в результате желаемый
2-(4-бензгидрил-1-пипераэинил)этилметил-2,6-диметил-4-(2-нитрофенил)- 50
1,4-дигидропиридин-3,5-дикарбоксилатдигидрохлорид моногидрат в виде светло-желтого кристаллического вещества, имеющего т.пл. 162-164 С. Выход
1194Х. 55
Вычислено, Х: С 59,90; Н 6,03;
И 7,99.
C
324 4
Найдено, Х: С 60,12; Н 6, 15;
И 7,89.
П р и и е р 4. Смесь о-хлорбенэальдегида, 2-(4-бен s гидрил-1-пиперазинил) этилацетоацетата и метил-3-аминокротоната нагревают в изопропило" вом спирте аналогично примеру 1, получив в результате целевой 2-(4-бенэгидрил-1-пиперазинил) этил-метил-4(2-хлорфенил) -2, б-диметил-1, 4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразного продукта с т.пл. 81-83 С (спекается).
Выход продукта 30,8Х от теоретически возможного.
ИК-спектр в вазелиновом масле ° см : 3320, 1680, ПИР-спектр (СОС1 ),8 ; 2,26 (6Н, синглет, =С-СН5 ); 3,56 (ЗН, сии глет, СООСН,, ); 4, 12 (2Н, триплет, 3 6, -СООСЙ;СН,-); 4,17 (1Н, сннглет, Я-СН ); 5, 36 (1 H синглет, С(,) «H)
5,63 (1Н, синглет, NH) .
Вычислено, Х: С 70,04; Н 6,38;
И 7,00.
Сз, Н qsС1ИзОа
Найдено, Х: С 69,84; Н 6,45;
И 6,83.
Пример 5. Смесь о -хлорбенэальде гида, 2- (4-бен згидрил-1-пиперазинил) этилацетоаце тата и этил-3"аминокротоната нагревают в изопропиловом спирте аналогично примеру 1, получив в результате целевой 2-(4-бензгидрил-1-пиперазинил)этол-этил-4-(2хлорфенил)-2,6-диметил-1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразного вещео ства с т.пл. 76-78 С (со спеканием).
Выход 34,7Х.
ИК-спектр в вазелиновом масле, см : 3320, 1690, 1680.
ПИР-спектр (CDC1> ), В: f, 17 (ЗН, триплет, J=?, -СН"СН ); 2,20 (6Н, синглет, =С-СН }; 4,20 (1Я, синглет, И-СН ); 5,40 (1Н, синглет, С -H)
6,37 (1Н, синглет, NH), Вычислено, Х: С 70,40; Н 6,56;
N 6,84.
С5б Н®, С1И Оа
Найдено, Х: С 70,12; Н 6,77;
N 6,57.
П р и и е р 6. Смесь 2,3-дихлор" бензальдегида, 2-(4-бензгидрил-1-пипераэинил) этилацетоацетата и метил3-аминокротоната нагревают в иэопропиловом спирте аналогично примеру получив в итоге целевой 2-(4-бензгидS 12583 рил-1-пипераэинил) этил-метил-4-(2, 3дихлорфенил) -2, 6-диме тил-1, 4-дигидропиридин-3,5-дикарбоксилат в виде .светло-желтого порошкообраэного вещества с т.пл. 84-88 С (со спеканием).
Выход продукта 31,6% от теоретически возможного.
ИК-спектр в вазелиновом масле, см : 3320, 1730, 1690.
ПИР-спектр (в дейтерохлороформе); 1п
3: 2,28 (6Н, синглет, С-СН„); 3,58 (ЗН, синглет;-СООСНЙ ); 4,15 (2Н, .триплет, J 6, -СООСН-СН -); 4,19 (1Н, синглет, N-.ÑÍ,, ); 5,45 (1Н, сииглет, С< -Н); 5,61 (1H, синглет, Н).
Вычислено, %: С 66,24; Н 5,88; Ы 6,62.
05m Н3104 О%
Найдено, %: С 66,38; Н 5,99; 20
М 6 37, П р и и е р 7. Смесь 2,3-дихлорбензальдегида, 2-(4-бензгидрил-1-пиперазинил)этилацетоаце ата и зтил-3аминократоната нагревают в изопропиловом спирте аналогично примеру получив в итоге целевой 2-(4-бензгидрил-t-пиперазинил)зтил-зтил-4(2,3-дихлорфенил)-2,6-диметил-t,4дигидропиридин-3,5-дикарбоксилат ЗО в виде светло-желтого порошкообраэного вещества с т.пл. 87-89 С (со спеканием). Выход 30,7%.
ИК"спектр s вазелиновом масле, см . 3335, 1695, 1680.
БИР-спектр (в дейтерохлороформе), 3: t 15 (ЗН, триплет, J=7, -PH;CH
3,25 (6Н, еинглет, =C-CH>); 4,16 (tH, синглет, N-СН ); 5,41 (1Н, синглет, С<4 -Н); 5,96 (tH синглет, NH), Вычислено, %: С 66,66 ; Н 6,06;
N 6,48.
С Н С1 И Ое
Найдено, %; С 66,32; Н 5,97; 45
N 6,27 °
Пример 8. Смесь мета-нитро-! бензальдегида, 2- (4-(4,4 -дифторбензгидрил) -1-пипераэинил) зтилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте аналогично примеру 1 получив в итоге целевой
2-(4-(4,4 -дифторбензгидрил)-1-пипера зинил) э тил-ме тил-2, 6-диме тил-4(3-нитрофенил) -1, 4-дигидропиридин3,5 "дикарбоксилат в виде светло-желтого порошкообразного вещества с т.пл. 68-72 С (со спеканием).
24 б
Выход продукта 33,3%. Этот продукт обрабатывают раствором хлористого водорода в метаноле и получают бес" цветные призматические кристаллы соответствующего дигидрохлорида с т.пл. 190-.193 С.
Вычислено, %: С 58,42; Н 5,35:
N 7,?9.
С; Н . N,O ° 2HC1
Найдено, %: С 58,45; Н 5,38;
N 7,44.
П р и и е р 9. Смесь мета-нитробенэальдегида, 2- (4-(4,4 -диметилбензгндрил) -1-пиперазинил) этилацетоацетата и метил-3-аминокротоната нагревают в изопропнловом спирте в условиях, аналогичных примеру 1, .получив в итоге целевой 2-t4-(4,4 диме тилбен з гидрил ) -1-пипера зинил) э тил-ме тил-2, 6-диме тил-4- (3-н итрофенил)-1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого nopoaricoo образного. вещества с т.пл. 83-87 С (со спекаиием). Выход 5361%.
ИК-спектр в вазелиновом масле, см :3330, 1695, 1680 (плечо) .
ПИР-спектр (в дейтерохлороформе), 8: 2,32 (6Н, синглет, 1;-СНз) е 2,36 (60. сНнглег, -Я -Сне); 3,60 (ЗН, синглет,-СООСЯ ); 4, 10 61Н, синглет,,N-CH ); 4, 14 (2Н, триплет, Я=6, -СООСН СН -); 5,09 (IH, синглет
С(1-") 5,84 (1Н, уширенный синглет, NH) .
Вычислено, %: С 69,57; Н 6,63
N 8,77.
СР Нн И О
Найдено, %: С 69,88; Н 6,82;
И 8,42.
Пример tO. Смесь мета-нитро«
Н бензальдегида, 2-(4-(4,4 -диметоксибензгидрил) -1-пиперазинил) зтилацетоаце тата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях,аналогичных примеру 1, в результате чего получают целевой 2-(4(4,4 -диметоксибензгидрил)-1-пиперазинил) э тил-ме тил-2, 6-диме тил-4- (3ни трофеи ил) -1, 4-диг идр о пир идин-3,5дикарбоксилата в виде светло-желтого порошкообразного вещества с т.пл.
76-80 С (со спеканием) ° Выход продукта 39,3%.
ИК-спектр в вазелиновом масле, см :3330, 1695, 1680 (плечо).
ДИР- спектр (в дейтерохлороформе), 8: 2,36 (6Н, синглет, = -СНн);" 3,57
1258324 8 гидрохлорид). Перекристаллизация этой соли из смеси этанол — диэтиловый эфир дала светло-желтые призматические кристаллы с т.пл. 208-211 С.
7 (ЗН, синглет, -СООСН ); 3,75 (6Н, синглет, -ОСН ); 4,11 (1H синглет, N-CH);. 4,15 (2Н, триплет, J=á, -СООСН "СН -); 5,08 (1Н, синглет, C(4f-Н); 5,80 (1Н, уширенный син- 5 глет, NH) .
Вычислено, Х: С 66 25; Н 6,319
N 8,35.
Сц Нд М40
Найдено, Х: С 66,22; Н 6,41;
N 8,12.
П р и. и е р 11, Смесь орто-нитробензальдегида, 2- f4-(4,4 -дифторбензгидрил) -1-пипер азинил э тилаце тоаце тата и метил-3-аминокротоната нагревают15 в изопропиловом спирте в условиях, аналогичных примеру 1, в результате
1 чего получают целевой 2-(4-(4,4— дифторбензгидрил)-1-пиперазинил) этилме тил-2, 6-диме тил-4- (2-н итр офе н ил) — 20
1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразного вещества с т.пл. 90-93 С (со снео канием). Выход продукта 21,3Х от теоретически возможного. 25
ИК-спектр, снятый с образца, полученного прессованием тонкодисперсного продукта с бромистым калием, см : 3350, 1695.
ПИР-,спектр (в дейтерохлороформе), 30
8: 2 26 (3Н, синглет, g СНз); 2 31 (ЗН, сииглет, = СН ); 353 (ЭН, синглет, -СООСН ); 4,0-4, 3 (ЗН, мультиплет, N-СН + -СООСН-СН -); 5,72 (1Н, синглет, С< > -Н); 5,77 (1Н, уши- 5 ренный синглет, NH) . Вычислено, Х: С 65,01; Н 5,61;
М 8,66. г
Найдено, %: С 65,40; Н 5,СО;
М 8,39.
Пример 12. Смесь мета-нитро-! бензальдегида, 2- (4-(4,4 -дихлорбензгидрил)-1-пиперазинил) этилацетоацетата и метил-3-аминокротоната нагрева- 45 ют в изопропиловом спирте в условиях примера 1, в результате чего получают целевой 2-(4-(4,4 -дихлорбензгидрил)-1-пиперазинил) этил-метил-2,б-диметил-4-(3-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразного веще-. ства с т.пл. 83-87 С (со спеканием), о
Выход продукта 57,8Х от теоретически возможного. Затем этот продукт обра >5 батывают раствором хлористого водорода в этаноле, получив .в итоге соот-. ветствующую дисолянокислую соль (диВычислено, Х: С 55,86; Н 5,09;
N 7,45.
С1 Н С1М40 ° 2НС1
Найдено, Х: С 56,00; Н 5,34;
N 7,38.
Пример 13 ° Смесь 2,3-дихлорбензальдегида, 2- (4-(4,4-дифторбензгидрил)-1-пипераэинил)-этилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях примера 1, в результате чего
S получают целевой 2-$4-(4,4-дифторбенэгидрил)-1-пиразинил) этил-метил4- (2, 3-дихлорфен ил) -2, 6-диме тил-1, 4" дигидропиридин-3, 5-дикар бок силат в виде светло-желтого порошкообразного вещества с т.пл. 90-93 С (со спео канием) . Выход указанного продукта
52,9Х от теоретически возможного.
ИК-спектр образца, полученного таблетированием с KBr, см: 3340, 1695.
ПИР-спектр (в дейтерохлороформе), 6: .2,28 (6Н, синглет, g-СН ); 3,57 (ЗН, сии глет, -СООСН > ); 4, 12 (2Н, триплет, J=6, -СОЮСН-СН -); 4, 16 (1Н, синглет, N-СН,,); 5,42 (lH, синглет, С«> -Н); 5,70 (1Н, уширениый синглет NH) .
Вычислено, Х: С 62,69; Н 5,26;
N 6,27.
С >> Н q> С1 Е, Мз04
Найдено, Х: С 62,77; Н 5,50;
М 6,06.
Пример 14. Смесь 2,3-дихлор1 бензальдегида, 2-(4-(4,4 -дихлорбензгидрил) -1-пиперазинил этилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях аналогичных примеру 1, в результате ! чего получают целевой 2-(4-(4,4 -дихлорбензгидрил)-1-пипераэинил этнлметил-4-(2,3-дихлорфенил)-2,6-диметил-1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкоо образного вещества с т.пл. 104-107 С (со спеканием) . Выход продукта 43,2Х от теоретически возможного.
ИК-спектр образца, полученного таблетированием тонкодисперсного продукта с KBr, см : 3340, 1695.
ПИР-спектр (в дейтерохлороформе), 3; 2,27 (6Н, синглет, =$-СН ); 3,57 (ЗН, синглет, -C00CH ); 4,12 (2Н, 9 1258 триплет, 36, -СООСН;СН,-); 4, 18 (1Н, синглет, N-СН ); 5,43 (1Í, синглет, С« -Н).; 5,70 (1Н, униренныи синглет, НЙ:
Вычислено, Е: С 59,76; Н 5,01; 5
N 5,97.
С Н C1ИО„
Найдено, 7: С 59,52; Н 4,97;
И 5,75.
Пример 15. Смесь мета-нитро- О ензальдегида, 2-(4-бензгидрил-гомопипера зин-1-ил) этилаце тоаце тата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой 2-(4-бензгидрилгомопиперазин-1-ил}этил-метил-2,6-диметил-4-(3-нитрофенил)-1„4-дигидропиридин-3,5-днкарбоксилат в виде светло-желтого порошкообразного веще- 20 ства с т.пл. 60-63 С (co спеканием), Выход продукта 3 1,7Х.
ИК-спектр образца, полученного
-! прессованием продукта c KBr, см
3330, l690.
ПИР-спектр (в дейтерохлороформе), 8: 2,33 (6Н, синглет, = С-СН ); 3,60 (ЗН, синглет); 4,12 {2Н, триплет, З=б); 4,57 (1Н, синглет, И-СН );
5, 10 (1Н, синглет, С< -Н); 5,92 (1H, синглет, NH).
Вычислено, Х: С 69;21; Н бь459, И 8,97.
СьН Нуо N406
Найдено, Х: С 69,24; Н 6,51
N 8477 °
Пример 16, Смесь мета-нитрабензальдегида, 2-(4-(4-фторфенил)-1пиперазинил)этилацетоацетата и метил3-аминокротоната нагревают в изонро- 4б лиловом спирте в условиях, аналогичных примеру 1, затем полученный продукт обрабатывают раствором хлористого водорода в дноксане, в результате чего получают целевой гидрохлорид
2-(4-(4-фторфенил)-1-пиперазинил) этил-метил-2,6-диметил-4-(З-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоксилата в виде светло-желтого порошкообразного продукта, имеющего т.пл.
108-110 С. Выход продукта 76,4Х от теории.
ПИР-спектр в дейтерированном диметилсульфоксиде (DMCO-d< ),о : 2,30 (3H, синглет, =С-СН ); 2,38 (ЗН, син- 5 глет, = -СН ); 3,60 (ЗН, синглет, -СООСН );. 4,48 (2Н, мультиплет, -СООСН;СН -); 5,03 (1H, синглет, С, Н).
324 !О
Вычислено, Е: С 56,71; Н 5,.78;
9,45.
С Н,FN О НС1Н О
Найдено, X: С 56,78; Н 5,85;
N 9ь35.
Пример 17. Смесь мета-ннтробензальцегида, 2-(4-(3-хлорфенил)-1пиперазинил этилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой 2-(4-(3-хлорфенил)-1-пиперазинил -этил-метил2,6-диметил-4-(3-нитрофенил)-1,4днгидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразо ного вещества с т.пл. 65-68 С (со спеканием), Выход указанного продукта 29,0 7 от теоретически возможного.
ИК-спектр в вазелиновом масле, см : 3300.
ПИР-спектр (в дейтерохлороформе), о: 2,34 (ÇH, сииглет, =С-СН ); 2,36 (ЗН, синглет, С-СН ); 3,63 (ЗН, синглет, -СООСНь); 4,21 (2Н, триплет, 3=6, -СООСН -СН1-); 5, 12 (1Н, синглет, С(4) -Н), 5,89 (1Н, синглет, ИН).
Вычислено, Х: С 63,26; Н 6,22;
И 10,18.
С Н, С1И40
Найдено, Х: С 63,33; Н 6,43;
N 9,83, П р и и е р 18е Смесь мета-нитробензальдегнда, 2-(4-{3-трифторметилфенил) -1-пнперазинил) этилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой метил 2-(4-{3трифторметилфеннл)-1-пиперазинил) этил-2ьб-диметил-4-(3-нитрофенил)1,4-дигидропиридин-3 5-дикарбоксилат в виде светло-желтого поровкообразного вещества с т.пл. 95-97 С (со о спеканием) . Выход продукта 82, 7 X.
HK-спектр дисперсии продукта в вазелиновом масле, см : 3345, 1695, 1645.
ПИР-спектр раствора продукта в дейтерохлороформе; 3: 2,34 (6Н, синглет, = -СН1); 3,64 (ЗН, синглет, -СООСН ); 4,21 (2Н, триплет, J=5,5, -СООСН1СН1-)ь 5ь11 (1нь синглеть
С<> -Н) 6,39 (1Н, синглет, NH).
Вычислено, 7: С 59,18; Н 5,31;
N 9,52, С1<УН 1 Р И40
1258
Найдено, Х: С 59,15; Н 5 53;
М 9,43.
Н р и м е р 19. Смесь мета-нитробензальдегида, 2- (4-(2-метокснфенил)1-пиперазннил) этилацетоацетата и
5 метил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой 2-f4-(2-метоксифенил)-1-пиперазинил)этил-метил- 10
2,6-диметил-4-(3-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразного вещества с т.пл. 58 С (спекается}.
Выход продукта 55,6Х. 5
ПМР-спектр (в дейтерохлороформе), .о: 2,34 (6Н, синглет, =С-СН ); 3,63 (ЗН, синглет, -ОСН );. 3,83 (ЗН, синглет, -ОСН ); 4,21 (2Н, триплет, J=6, -СООСЙ,СН -); 5,14 (1Н, синглет, 20
С(41-Н); 6,60 (1Н, синглет, NH) .
Вычислено, Х: С 63,26; Н 6,22;
N 10,18.
С„Н„И,О-,, Найдено, Х: С 63,33; Н 6,43;
N 9,83.
Пример 20. Смесь мета-нитробензальдегида, 2-(4-бензил-1-пиперазинил)этилацетоацетата и метил-3аминокротоната нагревают в изопропи- 30 ловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой 2-(4-бензил-1-пиперазинил) . этил-метил-2,6-диметил-4-(3-нитрофенил).-1,4-дигидропиридин-3,5-дикарбо- 5 ксилат в виде светло-желтого порошкоо образного вещества с т.пл. 106-108 С (со спеканием). Выход продукта 86,0Х.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3325.
ПМР-спектр (в дейтерохлороформе), 3: 2,33 (6Н, синглет, С-СН ); 3,46 (2Н, синглет, С Н-СН -); 3,61 (ЗН, синглет, -СООСН ); 4, 14 (2Н, триплег, J=6, -СООСН;СН -); 5,09 (1Н, синглет,g5
С«41-Н), 5,82 (1Н, синглет, NH).
Вычислено, Х: С 65, 15; Н 6,41;
N 10,48.
С„Н.„Н, О, . Найдено, .Х: С 64 93; Н 6 57; 50
N 10,48.
Пример 21. Смесь мета-нитробеизальдегида, 2-(4-(2-пиридил)-1пиперазинил)этилацетоацетата и метил3-аминокротоната нагревают в изопрб-" 55 пиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой метил 2-(4-(2-пиридил)324 12
1-пиперазинил) этил-2,6-диметил -4-(3нитрофенил)-1,4-дигидропиридин-3,5дикарбоксилат в виде светло-желтого порошкообразного вещества, имеющего т.пл. 53-56 С (со спеканием), Выо ход 54,5Х.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3280.
IMP-спектр (в дейтерохлороформе), 2,35 (ЗН, синглет, $-СНэ); 2,37 (ЗН, синглет, =С-СН ); 3,64 (ЗН, синглет, -COOCH ) 4,21 (2Н, триплет, J=6, -СООСН;СН -); 5, 13 (1Н, синглет, C()-Н); 5,77 (1Н, синглет, ЯН)-.
Вычислено, Х: С 62,.18; Н 5,99;
N 13,43.
С„Н„М,О6
Найдено, %: С 62,20; Н 6,07;
N 13,03.
Пример 22. Смесь мета-хлорбензальдегида, 2-(4-бензгидрил-1-пиперазинил)этилацетоацетата и метил3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой 2-(4-бензгидрил-1-пиперазинил)этил-метил-4-(3-хлорфенил)2,6-диметил-1,4-дигидропиридин-3,5дикарбоксилат в виде светло-желтого порошкообразного вещества с т.пл. о
74-80 С (со спеканием). Выход указанного продукта 28 3Х от теоретически возможного.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3325, !695, 1680.
ПМР-спектр (в дейтерохлороформе), 2,32 (6Н, синглет, С -СН ); 3,60 (ЗН, синглет, -СООСНз); 4,96 (1H, синглет, C(1 -Н); 5,64 (1Н, уширеиный синглет, NH
Вычислено, Х: С 70,04; Н 6,38;
N 7,00.
С1 H a «1N O4
Найдено. Х: С 70,15; Н 6,29;
N 7,18.
Пример 23. Смесь мета-трифторметилбензальдегида, 2-(4-бензгидрил-1-пиперазинил}этилацетоацетата и метил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают целевой 2-(4бензгидрил-1-ниперазинил)этил-метил2,6-диметил-4-(3-трифторметилфенил)-
1,4-дигидропиридин-3,5-дикарбоксилат в виде светло-желтого порошкообразноо го вещества с т.пл. 70-72 С. Выход
Вычислено, Х:
N 6â21
С«ВН «С1 И«О
Найдено, Х: С
И 6,00.
67,29; Н 6,27;
13 12583 продукта 52,5Х. Затем этот продукт подвергают обработке раствором хлористого водорода в метаноле и выделенный дигидрохлорид перекристаллизо» вывают из смеси метанол — диэтиловый
5 эфир. Получают желаемую дисолянокислую соль указанного продукта в виде бесцветного кристаллического вещества, имеющего т.пл. 168-170 С.
Вычислено, X: С 60,42; Н 5,77; 1в
И 5,87.
С« H «g F«@«0 ° 2НС1 1/2Н О
Найдено, Х: С 60,52; Н 5,49;
И 5,66.
Пример 24. Смесь 2,3-дихлорбензальдегида, 2-t4-(4,4 -диметилбензгидрил)-1-пиперазинил) этилацетоацетата и этил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1„ в результате чего получают целевой 2-(4-(4,4 -диметилбензгидрил)-1-пипераэинил) этилэтил 4-(2,3-дихлорфенил)-2,6-диметил1 4-дигидропиридин-3,5-дикарбоксилат в вида светло-желтого порошкообраз- 2S ного вещества с т.пл. 85-88 С (со б
I спеканием). Выход продукта 27,3Х от теоретически возможного.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3330, 30
1690.
П11Р-спектр (в дейтерохлороформе), 5: 1,14 (ЗН, триплет, 3=7, -СН-СН«);
2, 25 (12Н, синглет, =С-СН«)," 4,05 (2H, квадруплет, J=7, -СН-СН«); 4,08 (1Н, синглет, N-CH(); 4,08 (2Н, триплет, 3=6, -СООСН-СН -); 5,41 (1Н, синглет, С<,1-Н); 5,68 (1Н, уширенный синглет, МН), С 67,45; Н 6,41;
Пример 25, Смесь никотинового альдегида, 2-(4-бензгидрил-i-пиперазинил)этилацетоацетата и метил-3аминокротоната нагревают в изопропиловом спирте в условиях„ аналогичных примеру 1, в результате чего получают целевой 2-(4-бензгидрил-1пиперазинил)этил-метил-2,6-диметил4-(3-пиридил) — 1,4-дигидропиридин-3,5дикарбоксилат, Перекристаллизация полу енного продукта нз метанола дала бесцветные кристаллы с т,пл.
227-228 С, Выход продукта 46,3Х.
24 14
Вычислено, Х: С 72,06; Н 6,76;
И 9,89 °
С « Н«8 И О
Найдено, Х: С 72,08; Н 6,73;
И 9,94.
Пример 26. Первая стадия.
1. К смеси мета-нитробензальдегида (307 мг), 2-(4-бензгидрил-1-пиперазинил)этилацетоацетата (668 мг) и бензола (20 мл) прибавляют пиперидин (2 капля) и смесь кипятят в течение
2 ч с насадкой Дина-Старка для отгонки воды методом азеотропной дистил" ляции с бензолом. После охлаждения реакционную смесь промывают водой и cymar над безводным сульфатом натрия, после чего растворитель отгоняют в вакууме. В остатке получают сырой
2-(4-бензгидрил-1-пиперазинил)этил2-(3-нитробензилиден) ацетоацетат в виде масла.
АКР-спектр продукта (в дейтерохло роформе), 3 : 2,38 (ЗН, синглет, СОСН«); 4,14-4 53 (ЗН, мультиплет, -СООСН,-СН -) И-СН,); 7,10 8,75 (14Н, мультиплет) ° Этот продукт используют для проведения следующей стадии реакционного процесса без дополнительной очистки.
Вторая стадия. Иаслообразный продукт (все количество), полученный на предыдущем этапе, и метил-3-аминокротонат (280 мг) растворяют в изопропиловом спирте (10 мл) и раствор кипятят с обратным холодильником в течение 2 ч.. Затем растворитель отгоняют и остаток очищают колоночной хроматографией на силикагеле.
В итоге получают желаемый 2-(4-бензгидрил-1-ниперазинил)этил-метил-2,6диметил-4-(3-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоксилат с выходом
725 мг (67,6X). Далее этот продукт подвергают такой же обработке, как в примере 1, в результате чего получают желаемую дисолянокислую соль (дигидрохлорид). Перекристаллизация этой соли приводит к получению светло-желтого кристаллического вещества с т.пл. 166-169 С.
ИК-спектр и ПИР-спектр .этого сое» динения идентичны со спектрами моногидрата дигипрохлорнда продукта, полученного в примере 1, Пример 27. Первая стадия.
К раствору 2-(4-бензгидрил-1-пипера-, зинил)этилацетоацетата (3,21 г,,в этаноле (5 мл). прибавляют 20Х-ный раст1258324 !6
Вычислено, Х: С 62,93; Н 6, 16; и- N 6,12. о- С1ьНа C1N 0,, 2НС1
Найдено,X: С 62,67; Н 6,44;
), N e,ÎÎ.
П р н м е р 29. Смесь и -хлорбензальдегида, 2-(4-бензгидрил-1-пипераз- зинил)этилацетоацетата и этил-3-амит нокротоната нагревают в изопропило10 вом спирте в условиях, аналогичных б- примеру 1, в результате чего получают желаемыи 2-(4-бенэгндрил-1-пинеель разинил)этил-этил-4-(4-хлорфенил)2,6-диметил-1,4-дигидропиридим-3,515 дикарбоксилат в виде желтого порошо д- ка с т.пл. 75-79 С (со „спеканием). о- Выход продукта 32,8Х от теоретически возможного.
ИК-спектр диснерсии продукта в ва2о зелиновом масле, см :3300, 1685, а 1670.
ПИР-спектр (в дейтерохлороформе), 8: 1, 17 (ЗН, триплет, J7,5, -СН-СН );
2,28 (6Н, синглет, ("-СН. ); 4,95 и).25 (1Н, синглет, С<,,-Н); 5, 77 (1H, уширенный синглет, NH). и- Вычислемо, Х: С 70,40; Н 6,56;
Н 6,84.
С1,Н4 С1Н,О4
ЗО Найдено, Х: С 70,04; Н 6,51;
N 6,82.
Пример 30. Смесь мета-ннтробензальдегида, 2-(4-бензгидрил-1-пиIX пераэинил) этилацетоацетата и . 2-метоксиэтил-3-аминокротоната нагревают в изопропнловом спирте в условиях, аналогичных примеру 1, в результате чего получают желаемый 2-(4-бейзгидрил-1-пиперазинил)этил-2-метоксиэтил2,6-диметил-4-(3-нитрофенил)-1 4-дигидропиридин-3,5-днкарбоксилат в виде светло-желтого порошкообразного вещества с т.пл. 62-66 С (со спеканием). Выход укаэанного продукта
45 19,5Х от теоретически возможного.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3300, 1685, 1675.
ПМР-спектр (в дейтерохлороформе), 3: 2,33 (6Н, синглет, 1,-СН ); 2,50 (2Н, триплет, J 6, -СН-.СН И,,); 3,29 (ЗН, синглет,-ОСИ ); 3,49 (2Н, триплет, 34,5, -СН;СН,О-); 5,08 (1Н, синглет, C(I--H); 5,77 (1Н, широкий
15 вор аммиака в этаноле (15 мл) и смесь оставляют на ночь в холодильн ке. Затем растворитель и аммиак отг няют в вакууме и в остатке получают сырой 2-(4-бензгидрил-1-пиперазинил этил-3-аминокротонат в виде масла °
Вторая стадия. Масло, полученное на предыдущей стадии, мета-нитробен альдегид (0,88 г) и метилацетоацета (1, 15 г) растворяют в иэопропиловом спирте (15 мл), раствор кипятят с о ратным холодильником при перемешива нии в течение 6 ч. Затем растворит отгоняют и остаток очищают колоночной хроматографией на силикагеле.
Полученный таким образом продукт по вергают дальнейшей обработке по мет дике, аналогичной в примере 1, для получения соответствующей солянокис лой сопи (дигидрохлорида). Получают кристаллы моногидрата дигидрохлорид
2-(4-бензгидрил-1-пипераэинил)этилметил-2, 6-диметил-4-(3-нитрофенил)—
1,4-дигидропиридин-3,5-дикарбоксила та с выходом 1,06 г (17,8Х от теори
Полученный продукт имеет т.пл. 166170 С. ИК- и IlNP-спектры этого соед кения идентичны спектрам соединения полученного в примере 1.
I1 р и м е р 28. Смесь мета-хлорбенэальдегида, 2-(4-бензгидрил-1-пи перазинил)этилацетоацетата и этил-3 аиинокротоиата нагревают в изопропи ловом спирте в условиях, аналогичнь примеру 1, в результате чего получа ют желаемый 2-(4-бензгидрил-1-пинераэинил)этил-этил-4-(3-хлорфенил)2,.6-диметил-1,4-дигидропиридин-3,5дикарбоксилат в виде светло-желтого порошкообразного продукта с т.пл.
72-75вC (со спеканием). Выход 43,3Х
Этот продукт растворяют в неболь шом количестве этанола и к получен ному раствору прибавляют небольшой избыток этанольного раствора хлорис
)tat о водорода, после чего смесь ос1 тавляют выстаиваться в холодильнике
Образовавшийся кристаллический оса„док растворяют в смеси хлороформметанол (3: 1 по объему) и раствор концентрируют в вакууме. Прибавлени этилацетата к сконцентрированному раствору приводит к образованию кристаллического. осадка дигидрохлорида 2-.(4-бензгидрил-1-пипераэинил) этил-этил-4-(3-хлорфенил)-2,6-диметил-1,4-дигидропиридин-3,5-дикарбоксилата,-имеющего т.пл. 179-182 С.
Вычислено, Х; С 67,87; Н 6,7;
N 8,56.
С1т H
17
1258
Найдено, %: С 67,69; Н 6,49;
И 8,30
Пример 31, Смесь мета-нитроI . бензальдегида, 2-(4-(4,4 -диметилбенэгидрил)-1-пиперазинил1 этилацето5 ацетата и этил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают желаемый 2|.4-(4,4 -диметилбензгидрил)-1-липеразинил)этил-этил-2,6-диметил-4-(3нитрофенил)-1,4-дигидропиридин-3,5дикарбоксилат в виде светло-желтого порошкообразного вещества с т.пл.
82-85 С (со спеканием). Выход указан- 1 ного продукта 50,8% от теоретически возможного.
ИК-спектр дисперсии продукта в ва" зелиновом масле, см : 3330, 1685.
ПИР-спектр (в дейтерохлороформе), 3: 1,19 (ЗН, триплет, J=7, -СН;СН );
2,26 (6Н, синглет, =C-СН ); 2,33 (6Н, синглет, =1-СН ); 4,05 (2Í, квартет, .УУ, -СН-СН ); 4,10 (1Ч, синглет, ЪИ-СН ); 4,12 (2Н, триплет, Л=б, 25
-СООСН;СН -); 5,07 (1Н, синглет, Ci„1-Н); 5,75 (1Н, широкий синглет, ИН) .
Вычислено, %: С 69,92; Н 6,79;
И 8,58.
С qg Н+ И4 О ь
Найдено, %: С 69,94; Н 6,75;
И 8,25.
П р н и е р 32. Смесь мета-трифторметилбензальдегида, 2-(4-(4,4З5 диметилбензгидрил)-1-пиперазинил этилацетоацетата и этил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, 40 в результате чего получают желаемый
2)4-(4,4 -диметилбензгидрил)-1-пиперазинил|этил-этил-2,б-диметил-4-(3трифторметилфенил)-1,4-дигидропиридин-3,5-дикарбоксилат в виде бесцвет45 ного порошкообразного продукта с т.пл.
74-77 С (со спеканнем). Выход продуко та 44, 1% от теории.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3320, 1680.
ПМР-спектр (в дейтерохлороформе), 50
3: 1, 17 (ЗН, триплет, J=7, -СН -СН );
2, 26 (6Н, синглет, =g-СН1 ); 2, 32 (6Н, синглет, g-СН ); 4,05 (2Н, квадруплет, Л=У, -СН-СН ); 4, 10 { 1H, син" глет, ъИ-CH ); 4,12 (2H, триплет, J=6, .-СООСН;СН -); 5,02 (1H, сннглет, С|,1 -Н); 5,65 (1Н, широкий синглет, NH) .
324 18
Вычислено, %: С 69 32; Н 6,56;
N 6,22.
С39Н 44 F3 N30
Найдено, %: С 69,23; Н 6,55;
N 6,07.
П р и и е р 33. Смесь мета-хлорбензальдегида, 2-(4-(4,4 -диметилбензгидрил)-1-пиперазинил)этилацетоацетата и этил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают желаемый 2I;, (4-(4,4 -диметилбензгидрил)-1-пиперазинил)этнл-этил-4-(З-хлорфенил)-2,6диметил-1,4-дигидропиридин-3,5-дикарбоксилат в виде бесцветного порошкообразного вещества с т .пл. 798i С (со спеканием). Выход указанного продукта 48,4% от теории.
ИК-спектр дисперсии продукта в вазелиновом масле, см : 3330, 1680.
ПИР-спектр (в дейтерохлороформе), 6:, 16 (ЗН, триплет, J=7, -СН-СН )»
2,22 (6Н, синглет, = -СН ); 2,28 (6H, синглет, С-СН ); 4,05 (2Н, квадруплет, J=7, -СН СН ); 4,08 (lR, синглет, И-CH(); 4,11 (2Н, триплет, J=6, -СООСН;СН -); 4,93 (1Н, синглет, C><)-Н); 5,64 (1Н, широкий синглет, NH).
Вычислено,%: C 71,07; Н 6,91;
И 6,54.
C1S H44%1N>0<
Найдено, %: С 71, 19; Н 6,87;
N 6 38.
П р и и е р 34. Смесь мета-анисоI вого альдегида, 2-f4-(4,4 -диметилбензгидрил)-1-пиперазинил)этилацетоацетата и этил-3-аминокротоната нагревают в изопропиловом спирте в условиях, аналогичных примеру 1, в результате чего получают желаемый 2-f4I (4,4 -диметилбензгидрил)-1-пиперазинил1этил-этил-4-(3-метоксифенил)2,6-днметил-1,4-дигндропиридин-3,5дикарбоксилат в виде бесцветного порошкообразного вещества с т,пл. 7578 С (со спеканием). Выход указано ного продукта 42,2% от теоретически возможного.
ИК-спектр дисперсии продукта в .вазелиновом масле, см : 3330, 1690.
ПИР-спектр (в дейтерохлороформе, 0: 1, 18 (ЗН, триплет, J=7, -СН;СНэ);
2,25 (6Н, синглет, =(-СН ); 2,27 (ÇH, синглет, =С-СН ); 2,29 (ЗН, синглет, С-СН1)„ 3,68 (ÇH, синглет, "ОСН ); 4,05 (2Н, квадруплет, !
9 1258
-СН-СН !); 4,09 (1Н, синглет, > N-СН );
4,14 (2Н, триплет, 7=6, -СООСН СН -);
4,96 (1Í, синглет, С 41-Н); 5,62 (1Н, уширенный синглет, NH).
Вычислено, Х: С 73,44; Н 7,43;
N 6,59.
С4зН4, Zse
Найдено, Х: С 73,09; Н 6,64;
N 6,41.
Пример 35. Смесь мета-меток-. ta сикарбонилбензальдегида, 2(4-(4,4— диметилбензгидрил}-1-пиперазинил) этилацетоацетата и этил-3-аминокрото" ната нагревают в изопропиловом спирте в условиях, аиалогичных примеру 1, 15 в результате чего получают желаемый
2-(4-(4,4 -диметилбензгидрил)-1-пиперазинил) этил-этил-4-(3-метоксикарбонилфенил)-2,6-диметил-1,4-дигидропиридин-3,5-дикарбоксилат в в