Способ определения нитрила гликолевой кислоты в водных растворах
Иллюстрации
Показать всеРеферат
Изобретение относится к аналитической химии, в частности к способу определения нитрила гликолевой кислоты. Целью изобретения является повышение избирательности определения . Цель достигается потенциометрическим титрованием пробы с помощью нитрата ртути в присутствии гидроксида калия, взятого в молярном сротношении с анализируемым веществом .(4-10):1. Способ избирателен, т.к. позволяет определять нитрил гликолевой кислоты в присутствии цианидиона. Определению не мешают и другие соединения: сульфиды (титруются дифференцированно), роданиды, фенолы , органические основания, нитрилы, сульфаты, ацетонитрил, лактононитрил, ацетонциангйдрины, гликолевая и муравьиная кислоты, ион NH. 2 табл. (Л
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (19) (111 (11 4 С Oi N 31/16 (ч 1 г ч т г ф>
j I
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
И АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 3959771/23-04 (22) 30.08 ° 85 (46) 07.01.87. Бюл, Ф 1 (71) Восточный научно-исследовательский углехимический институт (72) С.Г.Дятел и Т.К.Тейхриб (53) 543.24 (088.8) (56) Вейганд-Хильгетаг. Методы эксперимента в органической химии.
М.: Химия, 1968, с. 327.
Лурье Ю.Ю. Аналитическая химия промьппленных сточных вод. — М,: Химия, 1984, с. 66-69.
Эшворт. Титриметрические методы анализа органических соединений. Методы прямого титрования. — N.: Химия, 1968, с. 195, 498.
Berther С., Kreis К., Buchmann О. (}uantitative Bestimmungvon Cyanhydrxnen. — Fresenius Zeitschrift fur
analitischue Chemic, 1959, 169, Ф 3, р. 184-187. (54) СПОСОБ ОПРЕДЕЛЕНИЯ НИТРИЛА ГЛИКОЛЕВОИ КИСЛОТЫ В ВОДНЫХ РАСТВОРАХ (57) Изобретение относится к аналитической химии, в частности к способу определения нитрила гликолевой кислоты. Целью изобретения является повьппение избирательности определения. Цель достигается потенциометрическим титрованием пробы с помощью нитрата ртути в присутствии гидроксида калия, взятого в молярном соотношении с анализируемым веществом (4-10):1. Способ избирателен, т.к. позволяет определять нитрил гликолевой кислоты в присутствии цианидиона. Определению не мешают и другие соединения: сульфиды (титруются дифференцированно), роданиды, фенолы, органические основания, нитрилы, сульфаты, ацетонитрил, лактононитрил, ацетонциангидрины гликолевая и муУ
gl равьиная кислоты, HQH NH . 2 табл. 1281999
Изобретение относится к аналитической химии и может быть использовано для определения нитрила гликолевой (оксиуксусной) кислоты — формальдегидциангидрина, принадлежащего к классу оксинитрилов или циангидринов, в сточных водах коксохимического производства при формальдегидной очистке от цианидов, в сточных водах производства нитрилов, лекарственных веществ и др.
Целью изобретения является повышение избирательности определения.
Способ осуществляют следующим образом.
Аликвотную часть исследуемого раствора 1-20 мл, в зависимости от содержания нитрила гликолевой кислоты, помещают в стакан для титрования, добавляют 0,1 М раствор гидроксида калия до получения молярного соотношения с нитрилом гликолевой кислоты (4-10): 1 и титруют О, 1 н. раствором
Hg(N0>) потенциометрически с системой электродов: серебряный индикаторный (проволока толщиной 1-2 мм) хлорсеребряный на универсальном.иономере типа ЭВ-74, работающем в режиме милливольтметра. Первый скачок потенциала (V, Hg(NO>) ) отвечает титрованию цианида по 1-й ступени, второй скачок потенциала (Ч Н@(МОз) ) соответствует титрованию CN no II-й ступени и нитрила гликолевой кислоты. Расчет концентрации нитрила гликолевой кислоты проводят по формуле
С N57 а где Π— концентрация нитрила гликолевой кислоты, г/л, N t — нормальность раствора, Ч вЂ” объем Hg(NO>), затраченный на достижение второго скачка потенциала, мл, V, — объем раствора Нд(ИОз), затраченный на достижение первого скачка потенциала, мл;
57 — эквивалентная масса нитрила гликолевой кислоты; — аликвотная часть раствора, мл.
Продолжительность определения 1020 мин.
Пример 1. Анализ сточной воды коксохимического производства, подвергнутой формальдегидной цианоочистке (содержание ИН Н О 0,.4 г/л, CN 0,013 г/л, нитрила гпиколевой кислоты 0,15 г/л — найдено химическим методом с отгоном), 50 мл исследуемой воды помещают в стакан для тит5 рования, добавляют 0,5 мл О,! М КОН и титруют в соответствии с методикой 0,05 н. Н8(ИОз) . На достижение первого и второго скачков потенциала затрачено соответственно 0,52
10 и 3,55 мл Н8(ИО ) . На определение нитрила гликолевой кислоты израсходовано 2,51 мл. Найдено нитрнла гликолевой кислоты 0,143 г/л. Молярное
15 соотношение гидроксида калия и нитрила гликолевой кислоты 4: 1.
Пример 2. Определение нитрила гликолевой кислоты в растворе, содержащем, г/л: NH3 Í О 0,7; CN
0,65, нитрил гликолевой кислоты 2,2; гликолевокислый натрий 4; формальдегид 0,29; NaCl 5,85. 5 мл исследуемого раствора помещают в стакан для титрования, добавляют 14 мл 0,1 М
КОН и титруют 0,05 í. Hg(NO>) в соответствии с методикой. На достижение первого и второго скачков потенциала затрачено соответственно 2,45 и 8,9 мл Н (ИО ) . На титрование нитрила гликолевой кислоты затрачено
4,0 мл. Найдено нитрила гликолевой кислоты 2,28 г/л. Молярное соотношение гидроксида калия и нитрила гли.колевой кислоты 7:1.
Пример 3. Определение нитри-.
35 ла гликолевой кислоты в растворе, содержащем, г/л: МНз Н О 1,7; CN 2,6 (в виде KCN) нитрил гликолевой кислоты 12, фенол С6Н ОН 0,5. t мл исследуемого раствора помещают в стакан для титрования, добавляют 5 мл 1 М КОН и титруют 0,05 н.
Hg(N0>) в соответствии с методикой.
На достижение первого и второго скачков потенциала затрачено.соответст45 венно 2 и 8,25 мл. На титрование нитрила гликолевой кислоты пошло 4,25 мл.
Найдено нитрила гликолевой кислоты
12,1 г/л. Молярное соотношение гидроксида калия и нитрила гликолевой
50 кислоты 10:1.
Результаты определения нитрила гликолевой кислоты в присутствии цианида в зависимости от содержания
55 гидроксида калия в среде представлены в табл. 1.
Как видно из табл. 1, количественные результаты определения нитрила гликолевой кислоты достигаются в
1281999
Т а б л и ц а 1
Примечания
Ошибка, 7.
Определено нитМолярное соотношерила гликолевои ние гиднитрила гликолевой кисгидроксида калия цианида калия роксида калия и кислоты в его
0,1 М растворе, г/л нитрила гликолевой кислоты лоты
0,5:1
1,5
3,0
Медленно устанавливается равновесное значение потенциала (3-5 мин) 5 30
1, 1: 1
3,3
3,0
1,5
-5,1
-4,4
5,41
2:1
3,0
1,5
1,0
5,45
3:1
8,0
4,0
2,0
Быстро устанавливается равновесное значение потенциала (20-30 с) 4:1
8,0
2,0
1,0
4:1
20,0
5,0
3,0
8:1
16,0
2,0
1,5
8:1
24,0
3,0
2,0
10:1
15,0
1,5
1,0
10:1
40,0
4,0
2,5 среде гидроксида калия, взятом в молярном соотношении с нитрилом гликолевой кислоты от 4: 1 до 10: 1. При соотношении гидроксида калия и нитрила гликолевой кислоты, меньшем 4:1, 5 медленно устанавливается равновесное значение потенциала и нитрил не определяется количественно, При соотношении, большем 10:1, точность анализа понижается из-за уменьшения 10 скачка потенциала.
Результаты определения нитрила гликолевой кислоты в рабочем и модельном растворах, содержащих 0,3 и 0 65 г/л CN, 0,4 и 0,7 г/л NH HqO
-соответственно, полученные предлагаемым и известным способами, представлены в табл. 2, Таким образом, предлагаемый способ является более избирательным, чем известный, и позволяет опредеВзято О, 1 М раствора, мл лять нитрил гликолевой кислоты в присутствии цианид-иона, Кроме того, определению не мешают сульфиды (титруются дифференцированно), роданиды, фенолы, органические основания, нитраты, сульфаты, ацетонитрил, лактонитрил, ацетонциангидрины, гликолевая и муравьиная кислоты, ион ИН
Формула изобретения
Способ определения нитрила гликолевой кислоты в водных растворах путем титрования раствором соли, о тл и ч а ю шийся тем, что, с целью повышения избирательности определения, в качестве соли используют нитрат ртути (II) и титрование проводят потенциометрически в присутствии гидроксида калия, взятого в молярном отношении к анализируемому веществу (4-10):1.
2,70 -52,5 Неколичественно определяется
5,78 1,4
5,65 -0,9
5,68 -0,4
5,76 1,0
570 0
563 . -12
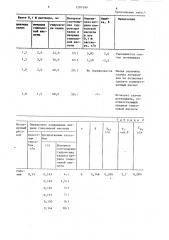
128! 999
Продолжение табл.!
Молярное соотношение гидроксида калия И нитрила гликолевой «ислоты
Ошиб ка, римечания цианидй йитрилй калия гликоле
ВОИ ЙИС» лотм. гидроксида калия
1,5
2,0
24,0
12:1 5,85 2,6 Уменьшается скачок потенциала
12:f 5 50 -3 5
1,5
3,0
36,0
2,0
1,0
40,0
20:1 скачка потенциала не позволяет сделать количественный расчет
1,0
60,0
1,5
50:1
Исчезает скачок потенциала, соответствующий нитрилу гликолевой кислоты
Т а б л и ц а 2
Исследуемый раствор
Определено содержание нитрила гликолевой кислоты
Гр г/л х
Я„, г/л
V, отн.7 предлагаемым способом известным способом, г/л г/л
Молярное соотношение тидроксида калия и нитрила гликолевой кислоты
Рабочий 0,15
6 0,148 0,036 2,7 0,004
4:1
О, 143
0,145 4,5: !
5:1
7:1
9:1
10:1
Эвято О, 1 и раствора, мл
0,152
0,151
О, 150
О, 144
Определено нитрепа гликолевой кислоты в его
0,1 N растворе, г/л
Не определяется Малая величина
1281999
Продолжение табл. 2.
Определено содержание нитрила гликолевой кислоты
$„, г/л предлагаемым способом
Модельный 2,2
2,24 0,056 2,6 0,06
4:1
2,28
5:1
2,17
7:1
2,25
2,18
9:1
10:1
2,21
10:1
2,32
Составитель В.Шкилькова
Редактор И.Николайчук Техред Л.Сердюкова: Корректор А. Ильин
Заказ 7258/41 Тираж 776 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва", Ж-35, Раушская наб., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
Исследуемый раств-. орр известным
caoCo"" . бом, г/л
r/ë Молярное соотношение гидроксидв калин я нит» рилв гликолевой кислоты