Липосомальная везикула для направленного транспорта биологически активных веществ
Иллюстрации
Показать всеРеферат
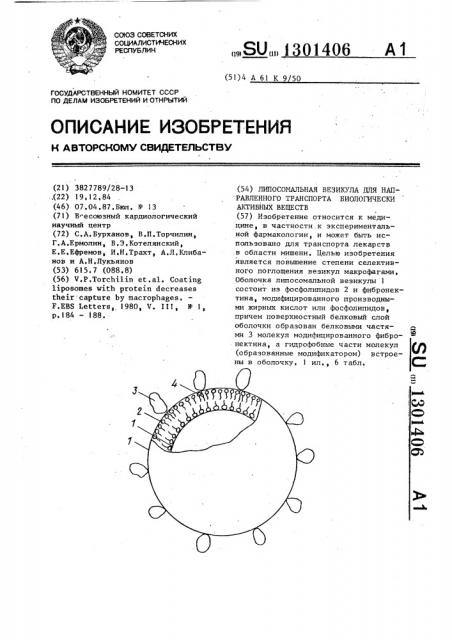
Изобретение относится к медицине , в частности.к экспериментальной фармакологии, и может быть использовано для транспорта лекарств .в области мишени. Целью изобретения является повьшение степени селективного поглощения везикул макрофагами. Оболочка липосомштьной везикулы 1 состоит из фосфолипидов 2 и фибронектина, модифицированного производными жирных кислот или фосфолипидов, причем поверхностный белковый слой оболочки образован белковыми частями 3 молекул модифицированного фибронектина, а гидрофобные части молекул (образованные модификатором) встроены в оболочку. 1 ил., 6 табл. р (Л с со 4 о О5
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (51)4 А 61 К 9 50
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К А ВТОВСНОМ,Ф СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 3827789/28-13 .(22) 19,12,84 (46) 07.04.87,Бюл. К 13 (71) Всесоюзный кардиологический научный центр (72) С.А.Бурханов, В.П.Торчилин, Г.А.Ермолин, В.Э.Котелянский, Е.Е.Ефремов, И.Н.Трахт, А.Л,Клибанов и А.Н.Лукьянов (53) 615.7 (088.8) (56) V.P.Torchilin et.al. Coating
liposomes with protein decreases
their capture by macrophages.
F.EBS I etters, 1980, V. III, Ф 1, р.184 — 188,Л0 I 301406 А 1 (54) ЛИПОСОИАЛЬНАЯ ВЕЗИКУЛА ДЛЯ НАПРАВЛЕННОГО ТРАНСПОРТА БИОЛОГИЧЕСКИ
АКТИВНЫХ ВЕЩЕСТВ (57) Изобретение относит ся к медицине, в частности.к экспериментальной фармакологии, и может быть использовано для транспорта лекарств, в области мишени. Целью изобретения является повьппение степени селективного поглощения везикул макрофагами, Оболочка липосомальной везикулы 1 состоит из фосфолипидов 2 и фибронектина, модифицированного производными жирных кислот или фосфолипидов, причем поверхностный белковый слой оболочки образован белковыми частя- д ми 3 молекул модифицированного фибронектина, а гидрофобные части молекул (образованные модификатором) встроены в оболочку. 1 ил., 6 табл. С:;
1 13014
Изобретение относится к медицине, в частности к экспериментальной фармакологии, и может быть использовано для транспорта лекарств в области мишени., 5
Цель изобретения — повышение степени селективного поглощения везикул макрофагами, На чертеже изображена лино-.омальная везикула, 10
Оболочка липосомальной везикулы 1 состоит из фосфолипидов 2 и фибронектина, модифицированного дитиодипропионил-фосфатидилэтаноламином причем поверхностный белковый слой оболочки образован белковыми частями 3 молекул модифицированного фибранектина, а гидрофобные части молекул, образованные модификатором 4, встроены в оболочку. 20
Таким образом, существенными признакамц предлагаемой липосомальной везикулы являются наличие конструктивных элементов — оболочка везикулы содержит специфический внешний поверх костный слой, сформированный молекулами модифицированного фибронектина; материалы, т.е. вещества, из которых состоят элементы везикулы — фосфолиыф.д а рН35 и ®
НООС
Модисрик ото (ДТДП-ФЗ) 1 беяиабая
NH . ость мопен злы — Рго е n — 1 Н вЂ” С
+ Pr0hei, РН 85 (И
О " 0О" " "" Моди(риццробонный фи д/юне тин
Гифорайная
ЧОCrnb МаЛакыры
Модификация фибронектина, Для связывания фибронектйна с липосомами использована предварительная гидрофобная модификация молекул белка дитиодипропионил-фосфатидилэтаноламином. Для этого 1 мг последнего растворяют в 100 мл -диметилсульфоксида и добавляют 1 мл 0,15 М МаС2. После
55 энергичного встряхивания к полученному раствору добавляют 2 мг 1-этил3-(3-диметиламинопропил)карбодиимид (рН 3,5), Через 10 мин добавляют
2 мг фибронектина, растворенного в
Цель изобретения достигается совокупностью указанных выше признаков, относящихся как к составу, так и строению объекта. При этом структура и строение липосомальной оболочки являются не менее существенным признаком, чем состав исходных компонентов, поскольку именно наличие поверхностного белкового слоя обуславливает эффективность поглощения веэикул макрофагами.
Липосомальные везикулы получают следующим образом.
06 2 пидный состав оболочки, фибронектин, модифицированный производными фосфолипидов (каждую из молекул которого можно условно разделить на белковую часть, образуемую остатком собственно фибронектина, и гидрофобную часть, образуемую модификатором) связь между элементами объекта, характеризующаяся тем, Ао одной своей частью (гидрофобной) молекулы модифицированного фибронектина встроены в фасфолипидную оболочку везикулы, а другой (белковой), экспонированной на поверхности оболочки, образуют поверхностный белковый слой.
Схема модификации фибронектина может быть условно выражена следующим образом (в качестве модификатора использован дитиодипропионил-фосфатидилэтаноламии - ДТДП-ФЭ), I. ДТДП-ФЭ активируют в водной среде водорастворимым карбодиимидом (рН 3,S).
К активированному ДТДП-ФЭ добавляют фибронектин в боратном буфере (pH 8,5), В результате аминогруппы фибронектина модифицируются остатками ДТДП-ФЭ, l301406
О
НООС вЂ” (СН СΠ— NH — СН вЂ” Π— P — P
ll
0,7 мл 0,1 M боратного буфера (рН 8„5) .
Липосомы готовят из яичного лецитина, общих фосфолипидов и ганглиозидов печени и холестерина методом об5 ращенных фаз, соотношение фосфолипида и холестерина 7:3. Для регистрации захвата в липосомальную мембрану встраивают необменивающуюся метку холестерил 14-С-олеат (фирма "Amers- ц1
ham"), Количество фосфолипидов оценивают по содержанию Р„, Белок измеряют по методу Лоури, 0 п ы т 1, 5 мг лецитина и 1,44 мг холестерина растворяют в хлороформе 15 и упаривают на роторном испарителе до получения пленки, Полученную пленку растворяют в 3 мл диэтилового эфира и добавляют 1,6 мг модифицированного фибронектина в 1 мл боратного 29 буфера. Полученный раствор обрабатывают ультразвуком, После удаления из раствора на роторном испарителе эфира получают однослойные липосомы, что контролируется электронной микроскопией.
0 п ы т 2, Получают фибронектин, модифицированный ДТДП- Э, Смешивают его с равным объемом предварительно сформированных липосом (концентра-, ция липида 3 мг/мл) и инкубируют
20 ч, При этом фибронектин встраивается своими гидрофобными остатками в мембрану уже готовых липосом за счет гидрофобного взаимодействия остатков фосфолипида в молекуле белка с липидной мембраной, 0 п ы т 3 ° Проводят аналогично опыту 2, но фибронектин смешивают с раствором липида (концентрация
5 мг/мл) в детергенте (2 7. хелат, 0,15 M NaC2, 10 MM 11аН РО, рН 7,4) и диализуют 18 ч против буфера не содержащего детергента, При этом об- . разуются липосомы,содержащие молекулы фибронектина на мембране липосом, причем остаток фосфолипида белка встраивается в мембрану липосомы, 0 п ы т 4, Проводят аналогично опыту 2, но вместо ДТДП-ФЗ используют глутарил-ФЭ. в тех же концентрациях и при том же времени инкубации.
0 п ы т 5. 1 мг фибронектина в
20 мг/мл хелатном буфере (1 мл), со-. держащем 0,15 M NaC2 и 0;1 M Na HPO рН 8,0, смешивают с 10 мл IOX-ного раствора пальмитоилхлорида в ацето-, о
40 не при 4 С, Через 1 ч осадок пальмитиновой кислоты отцентрифугирывают (12000, 15 мин) и отбрасывают, добавляют равный объем раствора липидов (концентрация 10 мг/мл) в том же буфере, Инкубируют 30 мин и диализуют 18 ч против такого же буфера, не содержащего хелата.
При этом самопроизвольно из смешанных мицелл липид — детергент белок образуются липосомы,в мембрану которых встроен фибронектин, За структурой образующихся комплексов фибронектин — липосома можно следить методом электронной микроско- пии.
Несвязавшийся белок может быть легко и быстро отделен бт липосом флотацией в ступенчатом фиколла или гель-фильтрацией в центрифуге на сефарезе CL 4B.
Используют трансформированные макрофаги мьппи линии 1774. На монослой
4 клеток (7 10 ) в лунке наносят аликвоту липосом и инкубируют при 37 С
1 ч. После удаления во флаконы с сцинтилляционной жидкостью ЖС-8 подсчитывают на счетчике RACKBFÒÀ 1215 (фирма L KB), Для определения эндоцитоза липосом макрофагами клетки преинкубируют 40 мин гликолитическим ингибитором эндоцитоза — йодацетамидом (100 мкмоль).
Пример 1. Сравнивают связывание и эндоцитоз макрофагами (? . 10 " клеток) липосом из лецитина без фибронектина и покрытых фибронектином.
Содержание липида 1,5 мг/мп и фибронектина 0,7 мг/мл, Данные приведены в табл, 1 и 2.
Пример 2. Сравнивают связывание и эндоцитоз макрофагами липосом из фосфолипидов и ганглиозидов
1406 ции е
Связывание липосом в
Эндоцитоэ липосом (пшо1 липида) Состав липосо Захват липосом (nmo 1 липида) присутствии йодацетамида (nmol липида
0,74+0,18 0,43+0,02
0,31
Лецитин
Лецитин + фибронектин 1,7 + 0,3
1,04
0 43 0,07
П р и м е ч а н и е: После гомогениэации липосом ло размеру ((4 »), Таблица 2
Захват
Эндоцитоз липосом (пп»о1 липида) Со ст ав лип о сом
Захват липосом в присутствии йодацетамида (гп ol липида) липо сом (nmo1 липида) 0,29+0,03 0,08
0,37+0,02
Лецитин
Лецитин + фибронектин 2,74+0,42 0,73+0,08
2,01
5 130 печени. Содержание липида 1,5 мг/мл, ганглиозидов, фибронектина 0,7 мг/мл.
Данные приведены в табл. 3 и 4 °
Пример 3. Проверка специфического взаимодействия макрофагов с липосомами, содержащими фибронектин, по сравнению с липосомами, содержащими бычий сывороточный альбумин.
Приготовляют липосомы, содержащие лецитин:холестерин (1:1), в которые встроены через гидрофобную "ножку" фибронектин и бычий сывороточный альбумин (БСА). Весовое соотношение компонентов то же, что в примере 1, Количество альбумина эквивалентно содержанию ФН, В табл.5 дано количество липосом, связавшихся с клетками макрофагов линии 1774 (распадов/мин С-холесте» » рико-олеата, связанного с липосомами), Исследуется кинетика связывания с макрофагами липосом, полученных на основе лецитина и лецитина с фибронектином.
В табл,б приведены данные о свя-, зывании липосом из лецитина и лецитина с фибронектином с макрофагами
Х774 в зависимости от времени инкуба6
Таким образом, фибронектин повышает фагоцитоз липосом макрофагами до 20 раз.
Использование изобретения .обеспечивает высокую степень захвата липо- сом макрофагами, стимуляцию фагоцитоэа липосом макрофагами, возможность применения липосомальных веэикул для транспорта БАВ, 10
Формула изобретения
Липосомальная везикула для направленного транспорта биологически активных веществ, содержащая оболочку, состоящую из фосфолипидов и внешнего белкового слоя, о т л и ч а ю— щ а я с я тем, что, с целью повышения степени селективного поглощения
20 везикул макрофагами, оболочка дополнительно содержит фибронектин, модифицированный производными жирных кислот или фосфолипидов, а внешний белковый слой образован белковыми частями молекул модифицированного фибронектина, при этом гидрофобные части его молекул, образованные модификаторо1», встроены в фосфолипидную оболочку.
Таблица 1
1301406
Т аблица 3
Эндоцитоз липосом (пшо1 липида) Захват лиСостав липосом осом в присутствии одацет амида (nmol липида) 1,44+0,ll
2,23
Фосфолипиды + 3 э67+ 0,09 г англио зиды
Фосфолипиды + ганглиозиды + 5э77+Оэ25 фибронектин
3,07
2э70+Оэ45
П р и м е ч а н и е. После гомогенизации липосом по размеру (< 4P), Таблица 4
Захват липоСостав липосо Захват липосом (nmol липида) сом в присутствии йодацет амида (nmo 1 липида) Оэ86+Оэ11
Фосфолипиды + 1э22+Оэ08
r англио зиды
0,36
5э61+Оэ59
Зэ47+Оэ34
2,14
Т аблица 5
Распад/мин при температуре, С
Э7 (4
Состав липосом
211 +32
97 э 7
Лецитин
Лецитин + 2967 + 111 фибронектин
304 +40
Лецитин +
БСА
600 59
126 +6
Фосфолипиды + .ганглиозиды + фибронектин
Захват липо сом (nmo1 липида) Эндоцитоз липосом (пшо1 липида) 1301406
Таблица 6
Состав липосом
Распад/мин при температуре, С
Время инкубации мин
68 14
Лецитин
86 8
120
180
Лецитин + фиб- 30 ронектин
120
180
Составитель Н. Кузенкова
Техред М.Ходанич
Редактор И.Горная
Корректор С, Шекмар
Тираж 596 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д,4/5
Заказ 1172/4
Производственно-полиграфическое предприятие, r.ужгород, ул.Проектная, 4
261 + 22
247 + 19
319 + 40
349 31
1305 + 210
2718 + 260
4106 + 140
4533 + 280
98 +12
97+ 13
152 < 19
200 +14
203 +20
261 +15