Способ спектрофотометрического определения алюминия
Иллюстрации
Показать всеРеферат
Изобретение относится к области аналитической химии. Целью является повышение чувствительности определения содержания алюминия от 1,35 до 135 иг/мл, расширение интервала определяемых его содержаний и упрощение способа в целом. Кристаллический фиолетовый сочетают с полученной при рН 3,2-5,1 по H2SO и выдержанной в течение 25 мин молибдоалюминиерой кислотой, отделяют центрифугированием полученное малорастворимое соединение , растворяют последнее в подкисленном ацетоне и полученный раствор спектрофотометрируют при 595 нм, 1 з.п. ф-лы, 4 ил., 2 табл. (Л 00 4 00 ОО
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (59 4 G 01 11 21/!7
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н А ВТОРСНОМУ СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ (21) 4066085/31-25 (22) 05.05.86 (46) 07 ° 10.87. Бюл. 11 37 (71) Институт общей и неорганической химии AH АрмССР (72) Ф. В, Мирзоян и С, М, Вартапетян (53) 543.42(088,8) (56) Mazzenko Z Janosz М. Formation of. ternary complexes of aluminium with some triphenylmethane reagents and cationic surfactants, Analyst, 1982, v. 107, N 1281, р, 1431-1438.
Sampson Barry, Fleck Adam Measurement of Alumimium in dialysis fluid
and water by à Spectrophotometric, Procedure — Analyst, 1984, ч. 109, М- 3, р, 369-37? °
„„SU„„1343308 А 1 (54) СПОСОБ СПЕКТРОФОТОМЕТРИЧЕСКОГО
ОПРЕДЕЛЕНИЯ АЛККИНИЯ (57) Иэобретение относится к области аналитической химии. Целью является повышение чувствительности определения содержания алюминия от 1,35 до
135 нг/мл, расширение интервала определяемых его содержаний и упрощение способа в целом, Кристаллический фиолетовый сочетают с полученной при рН 3,2-5,1 по H
1 э,п, ф-лы, 4 ил., 2 табл.
3308
134
Изобретение относится к области аналитической химии, а точнее к способам спектрофотометрического определения алюминия с использованием основного красителя, и может быть эффективно использовано при анализе материалов высокой чистоты, металлов, полупроводниковых материалов, руд,химических реагентов и других алюминийсодержащих объектов.
Целью изобретения является повышение чувствительности определения содержания алюминия от 1,35 до
135 нг/мл.
В качестве органического реагента используют краситель кристаллический фиолетовый (КФ), а в качестве анионного комплекса — анион многоосновной молибдоалюминиевой гетерополикислоты (MAK). Получают интенсивно окрашенный ионный ассоциат с девятью ассоциированными катионами КФ, и определение алюминия осуществляют по интенсивности светопоглощения его подкисленного ацетонового раствора, MAK получают при 3,84 10 M Na MoO
РН 3, 2-5, 1 (по Н „SO ) и 25-минутном выдерживании растворов, а твердофазный ионный ассоциат — молибдоалюминат КФ (МАК-КФ) получают при РН
1,20-1,40 (по Н БО„) добавлением (2,45-3,43) 10 М реагента-красителя, отделяют центрифурированием, растворяют в смеси 9 мл ацетона и ! мл 2 M HN03 и спектрофотометрируют полученный раствор при 595 нм.
При этом образуется соединение, содержащее девять ассоциированных катионов КФ, использование ацетоновых растворов которого обеспечивает высокую чувствительность спектрофотометрического определения алюминия:
Е=9,2.10 .л. мол х см ; С „„„
5 1.
=1,35 нг А1/мл;,С ь, „=135 нг А1/мл, Создается воэможность количественного определения в 100 раз разнящихся содержаний алюминия.
Оптическую плотность (OII) исследуемых ацетоновых растворов измеряют спектрофотометром, а равновесные значения РН соответствующих водных растворов — стеклянным электродом, Осадки соединения MAK-КФ отделяют двухминутным центрифугированием при
3000 об/мин.
Как видно из фиг. 1 (табл. 1), для получения MAK онтимальной является кислотность среды в интервале
РН 3 2 5,1 (по Н ЯО,,), т,е, выход соединения MAK-КФ, выделенного на основе МАК, полученной в указанном интервале РН„, максимален и ацетоновые растворы характеризуются постоянным значением коэффициента молярного погашения (Е=9,2:105), При РН „ ч (3,2 резко падает выход МАК, а значит и соединения MAK-КФ, поэтому использование указанных, значений РН при определении алюминия приводит к заниженным результатам, При РН„ „ о 5,1 укаэанные соединения (NAK и MAK-КФ) вновь количественно не образуются, что при определении алюминия также приводит к неправильным (заниженным) результатам.
20 Согласно данным фиг. 2 (табл. 1) количественное образование соедине ния МАК-КФ наблюдается при кислотности в процессе его образования, равной РН 1,20-1,40 (по H
РН 1,20 резко падает выход соедине30 ния . 1АК-КФ и поэтому использование указанных значений РН при опредеkoH ленни алюминия приводит к заниженным результатам, При РН „ э 1,40 резко возрастает сигнал ОП холостых опытов, и в результате конкурентной реакции выход соединения NAK-КФ падает, что при определении алюминия также приводит к заниженным результатам, I
Использование для создания среды азотной и соляной кислот нецелесообразно, поскольку при этом .значения сигналов холостых опытов резко возрастают, Согласно данным фиг. 3 и табл. 1 для количественного образования
MAK-КФ оптимальной является концентрация КФ в интервале (2,45-3,43 )х г
<10 М, При этом выход и соединения МАК-КФ постоянны, а сигналы холостых опытов очень малы. При С „,<
< 2,45 10 M соединение МАК-КФ количественно пе образуется, что при определении алюминия приводит к заниженным результатам, При С „ф> 3 ° 43х
«l0 1 резко возрастают сигналы как холостых растворов, так и соединения .1АК-КФ (т.е. на фоне соединения MAKЭ 308
Результаты определения алюминия при С = 5 10 лМ (1) 35 мкг Al/IO мл))
См>о =3 84 10 1, = 595 нм, 1
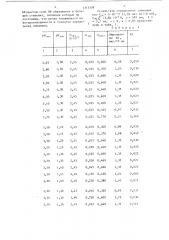
О, 1 см, n = 9, р = 0,95 представлены в табл. 1, Т а б л и ц а 1
Определены Al мкг/1О мл иссл
Aх, рН„„
Ск )
M 10 рН, „
1,30 2,45 0,025 0,200
0,59
2,65
1, 30 2145
1,03
0,025 0,350
2,80
1,30 2,45 0)025 0 1460
I 35
3,20
1,30 2,45
1) 30 2,45
0,025 0,460
0,25 0)460
1,35
3 50
I 35
3,75
1,30 2,45 0,025 0,460
4,50
1,35
1,30 2) 45
0,025 0,460
I 35
5,10
1, 30,2, 45 О, 025 О, 325
1,30 2,45 0,025 0,170
0,97
5,50
0,51
5) 75
1,10
0,89
0,010 О) 300
0,010 0,370
0 015 0,460
0,020 0,460
0,025 0,460
0,030 0)460
0,045 0,460
0,150 0,420
0,270 0,380
2,45
3,50
1,15
2)45
1,08
3 50
1,20
2,45
3,50
I 35
1,25
2,45
3,50
I 35
1130
2,45
3,50
l 35
2,45
1,35
1,35
3,50
2,45
l 40
3 50
1, 35
2,45
1,45
3 50
1,24
2,45
1 50
3,50
1, 10
3 50
0)0I0 0,320
0,020 0,400
0,025 0,460
l,47
1, 30
0,95
0,035
1,.30 1, 96
1, 30 2,45
3,50
0,030
0,023
1, 19
3,50
1,35 з
134
КФ простые соли КФ образуются в большей степени), значения которых не ,постоянны, что резко сказывается на воспроизводимости и точности определения алюминия, 0,050
0,030
0,020
0,021
0,020
0,023
0,021
0,035
0,060
0,050
0,040
0,030
0,020
0,022
0,021
0,025
0,040
0,075
1 343308
Продолжение табл.1 (t
0>025 0,460
1,35
0,020
0,021
0,022
0,025
0 040
0,070
3,50 1,30 2,94 0,035 0,460
3,50 I 30 3,18 0,040 0,460
1,35
1,35
0 050 0 460
О, 110 0,490
1,35
1,60
3,50 I 30 3)92 0)170 0,525
I,90
3,50 >30 2,70
3 50 1,30 3 43
3 50 1,30 3) 68
При построении кривой на фиг. 4 для каждой концентрации алюминия проведены 16-18 параллельных определений. Согласно приведенным результатам использование предлагаемого способа позволяет определять от 1,35 нг 25
Аl/мл (Sr = 0,29) до 135 нг Аl/мл (Sr = 0,020), При содержании Al
)35 нг Аl/мл значения Е соответствующих ацетоновых растворов снижаются вследствие неполного образования 30 соединения MAK-КФ, что при определении алюминия приводит к заниженным результатам. При 4 1,35 нг Аl/мл воспроизводимость результатов заметно падает вследствие затруднения процесса агрегации соединения МАК-КФ, Пример 1, 1 мл слабокислого раствора, содержащий 13 5 нг Al, помещают в центрифужную пробирку, добавляют 0,8 мл 0,0048 М раствора
Na>Mo04, создают рН 3,2 введением
0,4 мл 0,01 М раствора H>S04, перемешивают и выдерживают 25 мин для количественного образования MAK 3aтем прибавляют 1,! мл 0,5 M раствора
Н S04, 1 мл О, 1Х-ного (в конечном объеме С,ф = 2,45 .-10 М) раствора
-4
КФ, доводят объем дистиллированной водой до 10 мл (в полученном растворе рН 1, 20), перемешивают в течение
2 мин, Осадок соединения MAK-КФ отделяют двухминутным центрифугированием, раствор декантируют, осадок в той же пробирке растворяют в смеси 9 мл ацетона с 1 мл 2 М HNO> и полученный раствор спектрофотометрируют при 1= 595 нм и 1 = 1,0 -см.
Одновременно в тех же концентрационных условиях проводят холостой" опыт (A„., = 0,150). Оптическая плотность полученного раствора соединения MAK-КФ (d А) равна 0,050.
Пример 2. 1 мл слабокислого раствора, содержащий 0,27 мкг Al, помещают ц нтрифужную пробирку, добавляют 0,8 мл О, M раствора
Г1а„ Мо04, создают рН 4,25 введением
0,2 мл 0,0! М раствора Н 804, перемешивают и выдерживают 25 мин для количественого образования МАК. Затем прибавляют 0,9 мл 0,5 М раствора
Н. 804, 1,1 мл 0,17.-ного раствора
-4
КФ (в конечном объеме С„ = 2,7;10 М), доводят объем водой до 10 мл (в полученном растворе рН 1, 30), пер "мешивают в течение 2 мин, Осадок соединения МАК-КФ отделяют двухминутным центрифугированием, раствор декантируют, осадок в той же пробирке растворяют в смеси 9 мл ацетона с 1 мл
2 М HNO и полученный раствор спектрофотометрируют при ) =595 нм и
1 = 0,3 см, Одновременно в тех же концентрационных условиях проводят
"холостой" опыт (А „,Ä =0,075), Оптическая плотность полученного раствора МАК-K<9 (dA) равна
0,275, Пример 3. 1 мл слабокислого раствора, содержащий 1, 35 мкг Аl, помещают Ei цен трифужную пробирку, добавляют 0,8 мл 0,0048 М раствор-i
Na< Чо04, создают рН 5, I введением
0Ä3 мл !О M раствора Н S0„, перемешивают и выдерживают 25 мин для количес твенного образования MAK. Затем прибавляют 0,6 мл 0,5 М раствора
H,SG, 1,4 мл 0>!7-ного раствора КФ (в конечном объеме С,,>=-1,43.10 M), 08
Таблица 2 20
Определено Sr
Аl, мкг
При- Взято Al, мер мкг
0,29
0,014
1 0,0135
2 0,27
3 1,35
0 035
О, 021 ЗО
0,27
1,35
Яхf0 5
6,0 Р." ач
5,0
Ю0 40
Фиг. f
3,0,0
1З43З доводят объем водой до10 мл (B полученном растворе рН 1,40), перемешивают в течение 2 мин ° Осадок соединения МАК-КФ отделяют двухминутным
5 центрифугироЬанием, раствор декантируют, осадок в той же пробирке растворяют в смеси 9 мл ацетона с 1 мл
2 M HNO и полученный раствор спектрофотометрируют при 1 =595 нм и 1
= 0,1 см. Одновременно в тех же концентрационных условиях проводят холостой" опыт (A„,„= 0,050). Оптическая плотность полученного раствора соединения MAK-КФ (аА) равна
0,460, Результаты определения алюминия (п=16) в соответствии с примерами сведены в табл ° 2.
Таким образом, предлагаемый способ по чувствительности превышает из в е стные спе ктрофо томе триче ски е способы определения алюминия и применим для количественного определения в
100 раз разнящихся его содержаний.
Формула изобретения
1. Способ спектрофотометрического определения алюминия, включающий перевод его в окрашенное комплексное соединение и измерение оптической плотности, отличающийся тем, что, с целью повышения чувствительности определения содержаний алюминия от 1,35 нг/мл до 135 нг/мл алюминий переводят в молибдоалюминиевую гетерополикислоту при рН сре-, ды 3,2-5,1 по Н Я04 изменяют рН среды до 1,2-1,4 по Н ЯО, добавляют (2,45-3,43)r10 M кристаллического фиолетового, отделяют образующийся осадок, растворяют в подкисленном ацетоне и измеряют оптическую плотность при 595 нм.
2 ° Способ по и, 1, о т л и ч а— ю шийся тем, что, с целью повышения зкспрессности анализа, осадок отделяют центрифугированием.
1 343308 «
1,5 Р
Фиг. г
Е « 0 5
Z0 Я,О q0 50 С„@ Ю4м юг. 0 г,0 о,г
И Ф0 60 Ю f00 f70 140 0ле нГ) п
Д. ff
Составитель О. Бадтиева
Редактор Н, Егорова Техред Л. Сердюкова
Корректор 3, Пожо
Заказ 4816/44 Тираж 776
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб, „д, 4/5
Подписное
Производственно-полиграфическое предприятие, г. Ужгород, ул, Проектная, 4