Электрод для электролиза водных растворов хлоридов щелочных металлов
Иллюстрации
Показать всеРеферат
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК
А3 (19) (11) 111 4 С 25 В 11/lî
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н ASTOPCHOMV СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И OTHPblTPM (21) 3298834/23"26 (22) 03.06.81 (46) 07,06.88. Бюл. и 21 (72) В.Б.Буссе-Мачукас, Ф.И.Львович., Е.К.Спасская, В.Л,Кубасов, А.Ф.Мазанко, Э.А.Дружинин, А.Н.Мартынов и Л.H.Íåëèïà, (53) 621.3.035.2(088.8) (56) 1. Патент США У 3948751, кл. 204-290 F, 1976 °
2. Авторское свидетельство СССР
В 369923, кл. С 25 В ll/00, 1968. (54)(57) 1. ЭЛЕКТРОД ДЛЯ ЭЛЕКТРОЛИЗА
ВОДНЫХ РАСТВОРОВ ХЛОРИДОВ ЩЕЛОЧНЫХ
МЕТАЛЛОВ, содерлуицал основу из вентильного металла с нанесенным на нее покрытием из смеси окислов титана,. иридия и рутения, причем содержание окиси титана в смеси составляет более 50 мол.Х, о т л и ч а ю щ и й— с.я тем, что, с целью повьппения стойкости электрода, покрытие содержит окислы иридия и рутения при моль ном соотношении 0,75-.3:1.
2. Электрод по п.l, о т л ич а ю шийся тем, что покрытие содержит окислы титана в количестве
50-75 мол.X.
1401072
Изобретение относится к области электрохимических производств, конкретно к электродам для электролиза водных растворов хлоридов щелочных металлов с получением хлора и каусти" ческой соды, хлоратов, гипохлоритов, Известен электрод для электрохимических процессов, содержащий электропроводную основу, например из тита- 10 на, на которую нанесено активное покрытие из смеси окислов титана, иридия и рутения, причем содержание окислов титана в покрытии является значительным и составляет более l5 75 мол. . Например, в известном элект; роде покрытие имеет следуюший состав,, мол. : Ir O 3,91; КиО., 7,43 и
TiO 88,66 (образец В и образец Д) и ТгО 7,25; RuO 13,8 и Т10д 78,95 20 (образец С).
Таким образом, в известном электроде ингредиенты взяты в следуюшдх соотношениях, мол.%: Ti0 :(IrO +
+ RuO<) = 3,8 — 7,8:1 и ХгО :КиОд= 25
= О,5:1. Я
Недостатком указанного электрода является неустойчивость анодного по" тенциала при электролизе, низкий выход по току, недостаточная стойкость 30 электрода, Кроме того, недостатком электрода является неполное срабатывание активной массы - потенциал электрода резко возрастает при надиии еще досгаточного, количества масы активного покрытия.
Так,при испытаниях образцов В, и Д в насыщенном растворе NaCI ри плотности тока 1 А/см и 65 С нодный потенциал образца В изменялся в пределах 1,53-1,62 В за время электролиза 2000 ч (-83 сут), образца С вЂ” в пределах 1,35-1,38 В за
Время электролиза 2300 ч (96 сут) и образца Д вЂ” в пределах 1,44-1,50 В.45 за время электролиза 8)6 ч (34 сут).
Наиболее близким к изобретению по технической сущности и достигаемому результату является электрод для
Электролиза водных растворов хлоридов щелочных металлов, содержащий основу из вентильного металла с нане". и сенным на нее покрытием из смеси окислов вентильных металлов, например титана, и окислов металлов групПы платины, например иридия и рутения, причем содержание окисла вен-. тильного металла в смеси составляет более 50 мол.X. В известном электроде покрытие может содержать как смесь окислов титана и одного металла группы платины, например рутения, так и смесь окислов титана и нескольких металлов группы платины, например иридия и рутения (2) .
Недостатком известного электрода является невысокая стойкость.
Цель изобретения — повышение стойкости электрода.
Поставленная цель достигается тем, что в электроде для электролиза водных растворов хлорида щелочных металлов, содержащем основу иэ вентильного металла с нанесенным на нее покрытием из смеси окислов титана, иридия и рутения, причем содержание окиси титана в смеси составляет более
50 мол. ., покрытие содержит окислы иридия и рутения при мольном соотношении 0,75-3:l.
Кроме того, в предлагаемом электроде покрытие содержит окислы титана в количестве 50-75 мол.X.
Пример. На титановую основу электрода, предварительно прошедшую пескоструйную обработку, обезжиривание и травление, наносят покровный раствор — смешанный водный раствор
Т С 4 H OHC
Покровный раствор готовят из исходных растворов и компонентов: раствора гидрооксихлорида рутения (RuOICCl>) в воде с концентрацией
1501-5 г/л; раствора четыреххлористого титана (TiC1<) в воде с концентрацией 220+5 г/л (в пересчете на Т О ) ; соль треххлористого иридия (IrC1>) добавляют в смешанный раствор RuOHClTiCQ ) В Виде KpHcTcUIJIoB ° з
Активное покрытие электрода изготовляют многослойным, Каждый слой наносят по следующей технологии: расход смешанного .раствора на l --й спой—
25 мл/м, что соответствует заклада ке активной массы 1-2 г/м ; после нанесения каждого слоя электрод сна-. ,чала сушат при 150 С, затем обжигают о при 350 С в течение 20 мин первые
2"3 слоя, последующие слои прокаливают при 450-500 С в течение 2040 мнн.
Всего было изготовлено 9 электродов. Образцы 1,2,3 и 8 соответствуют по составу известному электроду. образцы 4-7 -,по составу предлагаемому электроду. Образец 9 иллюстрирует электрод с покрытием из смеси окис1401072 лов титана, иридия и рутения, причем содержание окиси титана в смеси составляет менее 50 мол. ..
Образец 1 соответствует общепринятому s промышленности окисному рутениево-титановому аноду.
Измерения потенциала анода проводят в условиях хлорного электролиза; концентрация раствора хлорида натрия
280 г/л, температура 90 С, рН = 3;03,5, плотность тока 1000, 2000,4000, 6000 и 10000 A/M, и в условиях хлоратного электролиза: 400 г/л NaC10>
100 г/л NaC1 рН = 7, плотность тока
1000-3000 А/м ; температура 80 С, Стойкость электродов оценивают по нескольким ускоренным методикам изучения износостойкости электродов: по методу переменной полярности и амаль.— гамации, при электролизе в растворе
Na0H, так и в условиях длительного электролиза, Сущность метода переменной полярности и амальгамации заключается в следующем: испытуемый образец при о плотности тока 1 А/см, 60 С в растворе хлорида натрия с концентрацией
300 г/л подвергают переменной анодной и катодной поляризации в течение
40 мин. Затем электрод опускают на
30 с в амальгаму натрия с концентрацией 0,2 мас. . После этих испытаний электрод промывают в дистиллирован,ной воде, сушат и определяют потерю веса.
Иэносостойкость электродов при электролизе растворов NaÎH изучают в следующих условиях: 200 г/л раствора о
Na0H, температура 90 С, плотность тока 2 A/ñì, и определяют потерю веса образца и время до запирания анода.
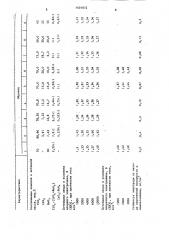
Результаты испытаний приведены в таблице.
Как видно из результатов, приве денных в таблице, предлагаемый электрод (образцы 4-7) не уступает известному электроду (образцы l и 8) по величине анодного потенциала в условиях хлорного и хлоратного элект.ролиза, Во всем заявленном интервале моль- ного соотношения окислов иридия и рутения в покрытии, а именно 0,753:1, стойкость предлагаемого электрода, оцениваемая по потере активной массы, как при испытаниях IIQ методу переменной полярности и амальгамации, так в зависимости от продолжительности электролиза в жестких условиях (200 г/л NaOH), является значительно более высокой, чем известного электрода, примерно в 1,5-2 раза.
2б При содержании окиси титана в покрытии более 75 мол. . и при мольном соотношении окислов иридия и рутения вне заявленного интервала стойкость известного электрода ниже, чем у предлагаемого (образцы 2 и 3). При содержании окиси титана в покрытии менее 50 мол, даже в пределах заявленного интервала мольного соотношения окислов иридия и рутения стой35 кость электрода является неудовлетворительной (образец 9).
Экономический эффект от использования изобретения составит 182 тыс.
4б рублей из расчета на производство
130 тыс.т хлора в год, 1401072
° ° ° л ф 0 сч сЪ сч с ъ О О со .с
РЪ РЪ M л а л сч с Ъ РЪ л а сЪ а о
1 I
1
1 CO о о и о о а ° о о с ъ сч
СЧ С Ъ ССЪ О
РЪ РЪ сЧ с Ъ с Ъ сЪ а
a. a а л л
О г» сЪ а л л е сСЪ ÑO Ф ° ° ° л м СсЪ 4"Ъ
СЧ 3 сСЪ О с ) с Ъ с Ъ с ) со о а о л! л. л. л ° е. л
В °
1
1 м
° е о о о гъ а е. л С Ъ о о о - * сч сч сч
О с Ъ .Э с \ с 3 с ъ б ) с ъ д о ссЪ ь а
Ю О1 !
1
1 л а л. a a м ° с м м а е. м м о о о а а а С ) ч
О сЪ сЪ -* м с сЧ мс ма с Ъ л ° а. л
° ю лъ
О а
C) а л a ° a a м а с м
° Ф °
О сЧ ссЪ а
Се! Ъ Ъ СсЪ С Ъ л. л . a., a ° а
I со а а. а о ev a с ъ м 1-ч
Ф Ъ л л л о
0Ъ
1 л ь
СЧ 0 Ф СО ОЪ с "! с"Ъ с Ъ с"!
° е ссЪ с.!
Щ л л сЪ О ссЪ сЪ
Ch с со
a a л
00 л с Ъ л Ч с Ъ л ь с Ъ I л, а л. л л м мс СО
° а с с °
CO сб1 л л
О сЪ О сЧ сЪ сЪ О О О ч ссЪ со ОЪ 1 а л е
00 РЪ со а ь а а е а м м
° %
° а
Р Ъ с Ъ о о
1 cv I с Ъ ссЪ С-- О с Ъ < Ъ с"Ъ ссЪ а. е л е а
1 I м м 1
О с Ъ Оъ 3 1 а л а м «е сч л
C) Х !
0 aS
Х И
m0CS O о
5 Ф Ж ь al E
В о
СОЦО о ж фг as Р & о < I o и с0 О н ж г о о о о
Ф O О О О О жм -e о о о
eS Р СсЪ с4 СсС ъО
& o & Е
1 4
1 с6
1 Е 1 5
ЬФ
° )
gI о
Е
-о
Ф ° ã4
v H
О с6
Ф ж
1 Ж
l Ф
8 о
-4
1ч о о
I O
I
1 l и I
0I 1
as 1
1о!
l 1
1 &
I Х
1 О
1 01
I 1 ! g
1 al
I О ! aI
l
1
I г" с в о
+ с! о
Н сс с и о о м О °
Н 0С сС о
° л
1-
0О Ф
Х М
С0 лО
О са 1.
52ж в Ц f о v
С0 О О
О5 Х аФО
os:g
Ж О) С о ж
О 5ОО о х ж о о
О Ы! - О О о ж Ф о о
Ф С4 Pl с с сЧ
I-Og Z!
»1 4
l о
Ж
Ф
X Х о и
О О (Ч
n x
gs0V о ц п О 4
Е !
Ф Ф
s".о х
6) Ж Х ж
А Ф е» Е Е
Ь VCSaS о on,r.
ОМФ0 с Ъ ig g о
I» ° Е о
140I 072 е и — л с л л а л a a a a a a Щ л о о о с ъ сс в л л
a a л a a о о о,1 !
1 3
ul Ch Сь1 ьО с ь
a a л. л л л сЧ ° сЧ с сс! Ч сЧ
a a . a о о о Г1 Ch а л л о о сЧ
О л л и
1 I
1 l !
I ! сО
I е4 Сл! Ф О 00
a a . л а л
О О О О О со СЧ O л л . а
СЧ Сс) Ф н сл! л л а! 1...! а —
tot i
О О О с! л л. а. л си с1 л л о0 л л сЛ а л е»
a a
О в сь ) Ф о а
° ь сЧ ес СЧ а л о о
О О л л с 1 3" ьО л a: a о о о ф Ch
° ь. о о л а сЧ
I 1 с 1 сО 00 а о о сЧ Ю О л л сьев 1
l I I 1 л л с сЧ
Ch л о сО л л о о
° ь
CV л л
° °
I I 1 1
«t
r I
Ch а Эь о о л л л
° ° сЧ
° ь ь
1 I 1 1 I I I!
» о ф ф
X х ьХ о о а х
1=3 !" и о ю о
О О о о а о о
° СЧ СЧ СьЪ
I Ж ! о
hC c6
Ф !Б с ф с
Х ь»
Р
c;о
Ю
td CV с о е
Рь Qr
1 о ! с ф
Ф Е
r. u ф ф
С4
А
f» I!I о с о э ьх х о с:
1- о о а
° Ф л о
О ф ф 0l х х с: к о
О О, х !» я !с х Ф
Ц
М A ф х х х
Оь 0l
4J X !
» Э о а, И Р3 оо а сЧ
a a a о сч с Е ! 1 м х
6 о с
lO Cf. о о .Ое Х И ф
3a f» сс! v с/ и со л
3/
00 л и с/ л сЛ сО л и
hC с ф
С.ь с»
Е ф л х 3 ьс! U