Способ определения концентрации гемоглобина в фекалиях
Иллюстрации
Показать всеРеферат
Изобретение относится к области медицины, в частности, к способам определения концетрации гемоглобина в фекалиях. Цель - повышение точности и ускорение способа. Цель достигается за счет превращения гемоглобина в порфирин при нагревании в присутствии щавелевой кислоты и оксалата железа полученный порфирин определяют флуоресцентным анализом в экстракте при λ возбуждения 408-410 нм и испускания 660 нм. При этом учитывают величину неспецифической флуоресценации, определяя ее в отдельном образце, где лимонная кислота или другое аналогичное нереагирующее соединение заменяет систему щавелевая кислота-оксалат железа.3 з.п.ф-лы,5 ил.
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИК (5ц 4 С 01 N 33/72
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТНРЫТИЯМ
ПРИ УНТ СССР (21) 3458455/28-14 (86) РСТ/US 81/0126 (21:09 ° 81) (22) 21.05.82 (31) 190.399 (32) 24.09.80 (33) (46) 23.04.89. Бюл. Р 15 (71) Риджентс оф Дзе Юниверсити оф Миннесота (US) (72) Самюель Швартц (US) (53) 612 ° 015(088.8) (56) Analytical Chemi, 1965, v. 37, р. 1124-1126. (54) СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ
ITМОГЛОБИНА В ФЕКАЛИЯХ (57) Изобретение относится к области медицины, в частности к способам on1
Изобретение относится к медицине, а именно к способам определения концентрации гемоглобина в фекалиях.
Цель изобретения — повышение точности и ускорения способа.
Цель достигается за счет превращения нефлуоресцирующего гемоглобина в порфирии при нагревании в присутствии щавелевой кислоты и оксалата
° железа, полученный порфирин определя ют флуоресцентным анализом в экстракте при длине волны возбуждения 408410 нм и испускания 660 нм, при этом учитывают величину неспецифической флуоресценции определяя в отдельном образце, в котором лимонная кислота или другое аналогичное нереагирующее соединение заменяет систему щавеле„„SU„„1475493 А3 ределения концентрации гемоглобина в фекалиях. Цель — повышение точности и ускорение способа. Цель достигает= ся за счет превращения гемоглобина в порфирии при нагревании в присутствии щавелевой кислоты и оксалата железа полученный порфирин определяют флуоресцентным анализом в экстракте при возбуждения 408-410 нм и испускания 660 нм. При этом учитывают величину неспецифической флуоресценции,. определяя ее в отдельном образце, где лимонная кислота или другое аналогичное нереагирующее соединение заменяет систему щавелевая кислота — оксалат железа. 3 э, и. ф-лы, 5 ил.
Ми4 вая кислота — оксалат железа. Вычитая величину флуоресценции, полученную в лимонной кислоте из величины, найденной для анализируемого образца, Ql получают величину флуоресценции, ко- фЬ торая связана с порфирином, получен- {;© ным из гемоглобина. СМ
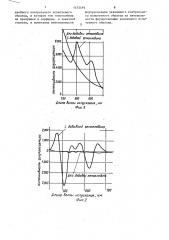
На фиг.1 изображен спектр флуоресценции гелеобраэной реакционной смеси (щавелевая кислота: окса ат железа) с добавлением гемоглобина и без не.— го; на фиг,2 — вторая производная от спектра флуоресценции;- на фиг.3 график сравнения спектров флуоресценции гемоглобина в растворе щавелевая кислота — оксалат железа и гемоглобина в растворе лимонной кислоты (по вертикали — уровни флуоресценции, 1475493 по горизонтали — длины волн испускания), на фиг.4 — график сравнения спектра флуоресценции образца фекалий в растворе щавелевая кислота — окса5 лат железа со спектром того же самого образца в растворе лимонной кислоты на фиг.5 — линейная зависимость между уровнем гемоглобина и флуоресценцией в растворе щаведевая кислота — оксалат железа, в который добавлено железо в виде FeSO< (по оси абс-, цисс — концентрация гемоглобина, по оси ординат — уровень флуоресценции). 15
Способ осуществляется следующим образом.
Определение слагается иэ трех стадий. Первая включает приготовление тестового образца фекалий, вторая— количественное превращение гемоглобина образца во флуоресцирующий порфирии, третья — измерение флуоресценции порфирина в тестовом образце и в . бланковом образце (в котором используют вместо смеси щавелевая кислота оксалат железа, лимонную кислоту) и сравнение разности во. флуоресценции с контрольным стандартом известной концентрации гемоглобина. Вначале отбирают и взвешивают тестовое количество образца фекалий— ,0,5 r. В образец добавляют 20-40 мл
0,85 - ного хлористого натрия, смесь гомогенизируют до равномерной дисперсии фекалий. Полученный тестовый об35 разец хранят в замороженном состоянии при температуре от (-15) до (-30 С) до востребования. Концентрация материала 2,5 .
Затем тестовый образец смешивают с реакционной смесью, содержащей 0,3З сульфата двухвалентного железа или
1 оксалата двухвалентного железа в
2М щавелевой кислоте при объемном. соотношении гомогенизированный материал: реакционная смесь,1:20. Полученную смесь нагревают до растворения ингредиентов (120 С в течение 90 мин), Добавление оксалата или сульфата железа, которые действуют как дополнительные, восстанавливающие агенты (наряду со щавелевой кислотой), обеспечивает полные превращения гема геМоглобина в порфирин и это обеспечивает прямолинейный график флуоресценции в интервале концентраций гемоглобина, достаточном для всех возможных уровней его в фекалиях (фиг.5);
На фиг.5 концентрации обработанного в автоклаве гемоглобина отложены в зависимости от интенсивности флуоресценции для концентрации сульфата железа: 0,0 ; 0,1% 1,0Х и 3 OX.
Как видно кривая 1, подученная без
FeS0< нелинейна при больших концентрациях гемоглобина, а кривая 2 в присутствии FeS04 — линейна. На фиг.5 1 возб. = 410 нм, а h исп. = 660 нм.
Образцы перед флуоресцентным анализом разбавляют до исчезновения окраски.
После превращения гема в протопорфирин смесь оставляют остывать. 3атем к ней добавляют в соотношении
4: 1 раствор, содержащий этилацетат и ледяную уксусную кислоту, взятые в соотношении 1:12. Полученную смесь центрифугируют. Для флуоресцентного анализа используют супернатант, ко.— торый благодаря добавлению этилацетата и ледяной уксусной кислоты получается прозрачным.
Спектрофлуориметрирование .проводят на приборах фирм Аминко Боуман или
Перхин Элмер (например, Перхин Элмер модель MPF-44Â) °
В качестве бланкового раствора, для учета присутствия в образце других флуоресцирующих веществ, используют тестовый образец, в котором щавелевую кислоту и оксалат, сульфат
Fe + заменяют на 1,5 М лимонную кислоту, остальные процедуры идентичны описанным, для анализируемого тестобразца, так как в присутствии лимонной кислоты не происходит превращения заметного количества гема (менее
0,2 ) < в порфирии, получаемый бланковый тест-образец позволяет оценить базовыи уровень порфиринов в фека" лиях.
На фиг.3 и 4 изображены спектры флуоресценции как смеси с лимонной кислотой, так и смеси щавелевая кислота — оксалат Fe 2 .
На фиг.3 показан спектр флуоресценции добавленного гемоглобина в системе щавелевая кислота — оксалат
Fe + — кривая 1 и спектр флуоресценции (кривая 2) добавленного гемоглобина в системе лимонной кислоты.
На фиг.4 изображен спектр флуоресценции (1) образца фекалий с гемогцобином в системе щавелевая кислотаоксалат Fe и спектр флуоресценции
5493
5 t47 (2) того же образца в бланковой системе лимонной кислоты.
Таким образом, разность флуоресценции между спектрами 1 и 2 отражает количество превращенного порфирина в исследуемом образце фекалий.
Пример 1. Приготавливают
2,5Х-ный фекальныи гомогенат в 0,85Хном растворе NaC1, Затем приготавливают 100 r реакционной смеси, объединяя 255,2 r щавелевой кислоты, 1,0 r порошка Fe04 или оксалата Fe+ в
73,8 мл воды. Эти ингредиенты нагревают в кипящей водяной бане до растворения (100-.120 С). Реакционную смесь заливают в трубочки или ампулы, которые запаивают и хранят при -30 С до употребления. Приготавливают также
100 r контрольной бланковой смеси, объединяя 28,8 r лимонной кислоты и
71,9 мл воды. Далее 50 мл 2,5Х-ного гомогената добавляют в каждую из трубочек, в которой проводится анализ. Туда же добавляют 1,0 мл либо подогретой смеси щавелевая кислота — оксалат Fe+, либо бланковой смеси. Содержимое трубок перемешивают на центрифуге, покрытой сорановой пленкой с отверстиями на верху. Затем трубки нагревают в автоклаве 90 мин при о
120 С оставляют остывать, проводят экстрагирование этилацетатом как описано ранее и измеряют флуоресценцию, так как протопорфирин составляет около 3,37Х молекулярного веса гемоглобина, величины, полученные для порфирина умножают на 100/3 37 или на
29,67 для получения соответствующего значения гемоглобина. Затем определяют величину гемоглобина в миллиграммах на грамм фекалий, умножая на соответствующие коэффициенты разбавления.
Пример 2. Для сохранения ре-. акционной смеси в нее дополнительно вводят полиэтиленгликоль при следующем соотношении компонентов: 73,8 r полиэтиленгликоля; 25,2 г щавелевой кислоты, 1,0 г порошка оксалата Fe или 1,0 г сульфата Fe+ .
В бланковую смесь дополнительно вводят 71,2 r полиэтиленгликолей и
28,8 г лимонной кислоты, Вышеуказанные смеси дают концентрации 4 М щавелевой кислоты и 1,5 М лимонной кислоты соответственно.
Для получения ожидаемого результата могут быть использованы 70Х-ный или 75Х-ный полиэтиленоксид.
При анализе спектров гелеобразной реакционной смеси применение вторых производных спектров флуоресценции может дать существенные преимущества (фиг.1 и 2).
Формула изобретения
1. Способ определения концентрации гемоглобина в фекалиях путем по- лучения суспензии исследуемого материала, превращением гема гемоглобина в порфирии в присутствии щавелевой кислоты и восстанавливающей соли с последующим измерением флуоресценции полученного образца, о т л и ч а ю— шийся тем, что, с целью повышения точности и ускорения сrrocoáh суспензию получают гомогенизацией в растворе 0,85Х-ного хлорида натрия при концентрации материала 2,5Х, .затем вводят гомогенизированный материал в реакционную смесь, содержащую
0,3-3Х сульфата двухвалентного железа или 1Х. оксалата двухвалентного железа в 2 М щавелевой кислоте при объемном соотношении гомогенезированный материал: реакционная смесь 1:20, полученную смесь нагревают до растворения ингредиентов и добавляют к ней в соотношении 4: 1 раствор, содержащий этилацетат и ледяную уксусную кислоту, взятые в соотношении 1:12, и в верхнем слое смеси измеряют флуоресценцию при 660 нм и длине возбуждающего света 408 †4 нм, 2. Способ по п.1, о т л и ч а ю— шийся тем, что,превращение гема гемоглобина испытуемого образца в порфирин проводят в реакционной смеси, содержащей полиэтиленгликоль или полиэтиленоксид . в концентрации
70-75Х.
3. Способ по п.1 или 2, о т л и ч а ю шийся тем, что испытуемый образец соединяют со щавелевой кислотой, или оксалатом, или сульфатом двухвалентного железа при 100-120 С.
4. Способ по пп.1-3, о т л и ч аю шийся тем, что стадия измерения флуоресценции превращенного парфирина включает в себя измерение флуоресценции испытуемого образца, в котором гем гемоглобина превращен в порфирин, измерение флуоресценции
1475493
8000
550 о00 б50Длина палны испускания, нм
ФУ8. f.
gg00 б00 HO
Клина палны испускания, нм
ФИГ Я двойного контрольного испытуемого образца, в котором гем гемоглобина не превращен в порфирии в заметной степени, и вычитание интенсивности
Ъ В.00
В
Ь.ОOО
М
Ъ2,00 ф ф
0 флуоресценции указанного контрольного испытуемого образца-из интенсивности флуоресценции указанного испы5 туемого образца.
1475493
600 б50
Алина Йлиы исгусканиц нм
4lи8.5
KDíöèíïÐàùè гекоалсйна, ике мл расп 3ора
Фие. 5
Редактор Г.Волкова
Заказ 1916/59 Тираж 788 Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат "Патент", r. Ужгород, ул. Гагарина, 101
Ю
30 zo
Ъ И,ОО
Ядопп
Q. ии
5 ю
А и
600 ОО
Алина 8олны испускания, нм
4 иа - Ф
Составитель А.Агуреев
Техред М.Дидык Корректор JI,Ïèëèïåíêî