Способ получения 3-феноксибензилового эфира @ цис, транс-2, 2-диметил-3-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты
Иллюстрации
Показать всеРеферат
Изобретение касается эфиров цикпошмфатических кислот, в чааноаи получения 3-феноксибензилового эфира (Ca(OH)J цис, транс-22- димепт-3-{22- дихпореинилЬ циклолроланкарбоновой кислотыь используемого для уничтожения вредных насекомых Г оцесс ведут омылением метилового эфира перметриновой кислоты Са(ОН) в среде растворителя с последующей обработкой полученной соли 3-феиоксибензилхлоридом в среде рааворителя в присутствии катализатора - тетрабутиламмониевой соли (±) цис транс-22-диметип-3-(2 -ДИХЛОрвинипН(иклолропановой кислоты или триэт««1бензипаммониевой соли указанной кислоты, взятые в количестве 1-5 моп% от количества 3-феноксибеизилхлорида Эти условия сокращают длит&ыюсть процесса до 3 ч и увеличивают до 99jB8% выход целевого продукта при улучшении его качества 1 табп
ОЮ) SU (Ill 152244М АЗ (51) 74
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ РЕСПУВЛЯК
ГОСУДАРСТВЕННОЕ IIATKHTIIOK
ВЕДОМСТВО СССР (I OCIIATEHT СССРНГ,Фл
„„),„„ амр
К ПАТЕНТУ (21) 4212281/04 (22) 18.0387 (46) 30.1193 Бка No 43-44 (71) Всесоюзный научно-исспедовате ыкий актитут химических средств защиты растений с опытl%N заводом (72) Костенко Н.И. Акшенцев ВВ; Костенко С.В„.
Верпеская ПА; Промоненков ВК (73) Всесоюзний научно-исследоватепьсюе юститут химических средств защиты растений (54) СПОСО6 ПОЛУЧЕНИЯ 3-ФЕНОКСИЬЕНЗИЛОВОГО ЭФИРА (+ ) ЦЯС TPAHC-2,2-ДИМЕТИЛ-3- (2,2-ДИХЛОРВИНИЛ)- ЦИКЛОПРОПАНКАРБОНОВОЙ КИСЛОТЫ (57) Изобретение касается эфиров циклоалифатических кислот, в частности получювтя 3-феноксибенмювого эфира (Са(ОН) ) цис, транс-2,2- диметиМ3-(2,2- дихлорвинип)- цицюпропанкарбоновой кислоты искктьзуемого для уничтожемя вредных насековмс Процесс ведут омыпением метилового эфтра перметриновой кислоты Са(ОН) в среде растворителя с тюспедующей обработкон г полученной сопи 3-феноксибензипхлоридом в среде растворителя в присутстее кататмзатора — тетВ Й () -22 тип-3-Ю-дихлорвинил)-циклопропановой киспор Ч вюють взятые в котмчестве 1 - 5 моп% от количества а Эти условия соNpBI43oT длительность процесса Qo 3 ч N )$8%5oвеют до 9988% выход целевого продукта при улучшена его качества 1 таба
1524439
Изобретение относится к органической химии и касается, в частности, способа получения 3-феноксибенэилового эфира (ч ) цис, транс-2,2-диметил-3--(2,2-дихлорвинил)циклопропанкарбоновой кислоты (перметрина), и рименяемого в качества инсектицида для борьбы с вредными насекомыми.
Цель изобретения — повышение выхода целевого продукта и сокращение времени реакции, Пример 1. В колбу загружают 0,88 моль КОН, 0,8 моль метилового эфира перметриновой кислоты, 300 мл толуола, нагревают до температуры кипения смеси, одновременно отгоняя образующийся спирт, и выдерживают до исчезновения метилового эфира перметриновой кислоты и
0,8 моль 3-феноксибензилхлорида (3-ФОБХ) в 300 мл толуола перемешивают в присутствии 0,004 моль (0,5 моль. ) тетрабутилперметрината (ТБА ПК) при 75ОC в течение 3 ч.
Образовавшийся хлорид калия отфильтровывают, фильтрат промывают 300 мл воды, толуол отгоняют под вакуумом. Кубовый остаток представляет собой технический перметрин с содержанием основного вещества
42,0ф„выход 39,0%.
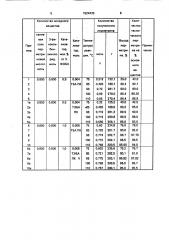
Примеры 2-26 и 1а — 26а проводят аналогично примеру 1, Условия проведения процесса и выход целевого продукта представлены в таблице.
Анализ технического продукта проводят методом газожидкостной хроматографии на колонке длиной 2 м с 5% ХЕ-60 на хроматоне N=AWDMCS с внутренним стандартом, При проведении анализа по нормализации: температура испарителя 240 С, nporpaMMa: температура колонки 100235 С, начальная скорость 8 град./мин, скорость ленты 600 мм/ч, объем вкола 0,2 мкм без растворителя.
Пример 136 (сравнительный, см. таблицу). Полученную в примере 8 калиевую соль перметриновой кислоты и 0,8 моль 3феноксибензилхлорида в присутствии 0,024
M (3 мол. (,) триэтилбензиламмонийхлорида перемешивают в 300 мл толуола при 96 С в течение 3 ч. Реакционную массу обрабатывают по примеру 8.
В результате получают технический перметрин (0,68 моль - 266,1 г) с выходом
85 и качеством 86 основного вещества.
Максимальный выход(90 ) перметрина достигается эа время реакции не менее 8 ч, Получение катализатора,1 моль калиевой соли перметриновой кислоты
35 ао
50 и 1 моль триэтилбенэиламмонийхлорида (тетрабутиламмонийбромида) перемешивают в течение 2 ч в иэопропиловом спирте при комнатной температуре. Затем образовавшийся в результате взаимодействия хлорид калия отфильтровывают от реакционной массы, а изопропиловый спирт упаривают. Остаток — триэтилбензиламмонийпе рметринат (тетрабутиламмонийперметринат) — в качестве катализатора поступает на стадию синтеза перметрина.
Регенерация и рецикл катализатора.
Пример 13 (см. таблицу). 0,8 моль
3-феноксибензилхлорида в 300 мл толуола и полученную по примеру 8 калиевую соль перметриновой кислоты в присутствии
0 024 моль (3 моль.7ь) триэтилбенэиламмониевой соли перметриновой кислоты при
96"С перемешивают в течение 3 ч. Образовавшийся осадок хлорида калия отфильтровывают, фильтрат промывают водой три раза. После расслаивания органический слой подвергают отгонке толуола под вакуумом и получают 0,778 моль (304,4 г) перметрина с выходом 97,25ф».
Водные слои — раствор катализатора— обьединяют, упаривают и возвращают в синтез (пример 26). Выход регенерированного катализатора 98,07; (0,0235 моль, 9,4 г).
Пример 26 (с применением регенерированного катализатора).
0,790 моль З-.феноксибензилхлорида и
0,790 моль калиевой соли перметриновой кислоты в 300 мл толуола перемешивают в присутствии 0,0235 моль триэтиламмонийперметрината, регенерированного из реакционнойй масс ы перметрина (и ример 13), в течение 3 ч при 96 С. Затем реакционную массу обрабатывают, как описано в примере 13, и в результате получают 0,768 моль (300,5 г) перметрина с выходом 97,2, содержание основного вещества 97.5 .
С применением регенерированного катализатора процесс не ухудшается, Таким образом, получение перметрина по предлагаемому способу позволяет повысить выход целевого продукта до 95 — 987 (по сравнению с 82 — 90 ) и сократить продолжительность процесса в 1,7 раза. (56) Патент СССР № 516911, кл. С 07 С 69/74, 1977, Патент СССР ¹ 627749, кл. С 07 С
69/74, 1978, Патент СССР N 725553, кл. С 07 С
69/74, 1980.
1524439
Количество пол pl6 н ного пе мет ина
Количество исходного вещества калиеКатализавая
8ыход
Температура персоль
Приперперметрина, $ реак«и, С мер моль рид основФОБХ моль ного щества
42,0
0,004
ТБА ПК
0,800
0.5
0,800
869
0,5
0,800
0,800
2а
За
88,0
83,0
4а
5а
78,0
1,0
0,008
ТБА ПК
0,800
0,800
76.7
0,602
1,0
0.800
0,800
6а
7а
8а
9а
1Оа
2
7
9
10 метриновой кислот, моль ноксибензилхлотор ° мол. от 3Катализатор, моль
0,004
ТЭБА
flK
0,008
ТЭБА
IlK Ч
96
110
А5
96
110
96
110
96
110
0,312
0,483
0,72.
0,69
069
0,32
0,482
0,719
0,719
0 680
0,60
0,720
0,774
0,772
0,768
0,721
0,775
0,768
0,767
122,1
189.1
281,7
270,0
270 4
125.2
188,5
281,3
280,8
266 1
234,8
281,7
302,7
302,1
300 5
235,6
282,0
303,1
300,5
300,1
39,0
60,4
90,0
86,4
864
40,0
60,2
89,9
89,9
85,0
75,0
90.0
96,7
96.5
95 99
75,2
90,1
96,82
96,0
95,9. Количество технического метри- Примена на чание
62,7
89,0
86.35
42,5
65,0
90,0
92,0
97,79
96,5
940
91,9
97,82
96,7
95,5
1524439
0,024
ТБА ПК
0,614
240,4
291,0
76.8
92,95
97,25
76.0
12
0,744
93,98
97,75
0,778
304.4
0,0235 м (выход
98 ) регенерированногока- . талиэатора намеру
97,0. 100
110
0,775
0,767
303,3
300,2
96,9
95,9
93.0
0,024
ТЭБА
ПК
0,611
11а
239,2
76,4
0.0235 м (вы77,3
12а
0,752
294,2
94,0
94.5
13а
0,781
305,6
97,35
97,68 ход
97,8 ) регенерированный катализатор направляют в опыт по примеру
26а
0,800 0,800
0.800 0,800
Продолжение таблицы правляют в опыт по при10
1524439
Продолжение таблицы
86
Сравнитель0.68 266.1
85$
13б
0.800
0,024
ТЭ БАХ ный пример: макси мал ьный выход
8ч
0,778 304.8
0,768 300,5
97.3
97,5
110
14а
15а
96,0
945
0,040
ТБА llK
0,800
79,3
0,800
16а
17а
96,3
98,2
18а
98,0
96,0
19а
20а
0,08
ТБА flK
0,800
0,08
81,9
80,0
0,800
21а
98,5
98.2
ТЭБА
ПК
22а
23а
97,0
0,778
0,760
24а
93,0
25а
16
17
18
19
21
22
23
24
0,800 3
0,800 5
0.800 5
0.800 10
0,800 10
0,040
ТЭБА
flK
96
110
96
110
96
110
96
110
0,632
0,764
0,784
0,782
0 768
0.631
0,767
0,784
0,783
0,769
0,640
0.767
0,788
О,778
0,768
0.640
0,768
0,784
247,3
299,0
306,8
306,2
300 5
247,0
300,2
306,7
306,4
300 8
250,4
300,2
306,4
304,6
300 6
250,4
300,5
306,4
304,6
297 5
29,0
95,5
98,0
97,8
96 05
78,9
95.9
97,99
97,9
96 09
80,0
95,9
97,88
97,3
96,05
96,0
98,0
97,3
95,03
79,3
96,3
98.1
97,9
969
82,0
96,2
97.95
97,3
94,7 достигается эа время неменее
1524439
10
297,8
0,761
0,0235
ТБА ПК
97,2
97.5 меру
0,762
298.0
0,0235
ТЭБА
97,5
97.25
26а ра, меру
13а
68,87
88 (н а
МЭПК) 23,2
КатализаНе укаП ример 1
Вщ)иэнт А зано тор мин. дии омыления
0,783 0,783
0,783 0,783
0,2 0,2375
МЭПК
Продолжение таблицы
0,058 Известный моль способ 100 С
10 г 0,176
Время 5 ч
Катализатор регенерированный иэ опыта по приС испол ьзованием катализаторегенерированного из опыта по припентаметилдиэтилентриаПредположительно выход на ста1524439
Продолжение таблицы
1524439
Продолжение таблицы
TSA ПК - тетрабутиламмомиевая соль перметриновой кислоты;
ТЭЬА ПК вЂ” триэтилбензиламмомиевав соль перметримовой кислоты;
ТЬАХ вЂ” триэтилбемзиламмомийхлорид;
МЭПК - метиловый эфир перметриновой кислоты;
ЭЭГИ(- этиловый эфир перметримовой кислоты;
Составитель P.Марголина
Техред М,Моргентал Корректор E. Папп
Редактор M.Ëåíèíà
Заказ 3336
Тираж Подписное
НПО "Поиск" Роспатента
113035, Москва, Ж-35, Раушская наб„4/5
Производстеенно-издательский комбинат "Патент", г, Ужгород, ул.Гагарина. 101
Формула изобретения
СЙОСОБ ПОЛУЧЕНИЯ Э-Ф НОКСИ ЬЕНЗИЛОВОГО ЭФИРА () ЦИС, ТРАНС-2,2-ДИМЕТИЛ-З {2,2-ДИХЛОРВИ
НИЛ)-ЦИКЛОПРООАНКАРБОНОВОЙ КИС
ЛОТЫ, включаюафФ омыление метилового ðÎ перметриновою кислоты гидроокисью калил в растворителе с последующим взаимодействием образовавшейся сане с 3-феноксибензилхаоридом в растворителе в присутствии МТ3пН33Тор8, отличаюшрайсл тем, что, с целью повышения выхода целевого продукта и сокращения времени реакции, в качестве катализатора используют тетрабутиламмониевую соль () цис. транс-2,2-диметил-3-(2,2-дихлорвинил)-циклопропанкарбоновой кислоты или триэтилбензиламмониевую соль () цис, транс-2,2-диметил-З(2,2-дихлорвинил)-цик лопропамовой кислоты, взятые в количестве 1 - 5 мол. Я, от количества 3-феноксибензилхло рида.