Способ определения этилендиаминтетраацетата в воде
Иллюстрации
Показать всеРеферат
Изобретение касается аналитической химии, в частности определения этилендиаминтетраацетата в воде, и может быть использовано для анализа сточных вод в этом производстве. Анализ ведут добавлением в пробу 5-12 об.% ацетона и NCL до рН 1,5-2 с последующей обработкой избытком нитрата висмута в присутствии индикатора ди-(п-сульфофенил)-тиокарбогидразида и титрованием полученной смеси раствором этилендиаминтетраацетата натрия. Эти условия повышают чувствительность с 3,4 до 0,168 мг/л и избирательность определения, которому не мешают присутствие PB, MN, CU, ZN, CD, AL, щелочно-земельных металлов, лактаноидов. Относительная ошибка до 2,98%. 3 табл.
СОЮЗ СОВЕТСКИХ социАлистичесжих
РЕСПУБЛИК (51)4 С 01 N 31 16
ОНАЯ
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К А ВТОРСНОМУ СВИДЕТЕЛЬСТВУ
ГОсУДАРстВенный KOMMTET
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР
1 (21) 4376647/31-04 (22) 05.02.88 (46) 30.11.89. Бюл. Н 44 (71) Институт коллоидной химии и химии воды им. А.В.Думанского (72) А.Т Пилипенко, Л.Н.Демуцкая, Н.В.Онопа, Н.Ф.Фалендьаи и Е.Н.Арендарюк (53) 543,24.087(088.8) (56) Лурье N.I0. Аналитическая химия промышленных сточных вод. М.: Химия, 1984, с.396-399, 447. (54) СПОСОБ ОПРЕДЕЛЕНИЯ ЭТИЛЕНДИАИИНТЕТРААЦЕТАТА В ВОДЕ (57) Изобретение касается аналитической химии, в частности определения этнлендиаминтетраацетата в воде, Изобретение относится к аналитической химии органических соединений, а именно к титриметрическнм методам определения этнлендиамннтетраацетата (ЭДТА), и мокет быть использовано заводскими и научно-исследовательскими лабораториями для определения содеркания ЭДТА в производственных растворах, природных и сточных водах.
Цель изобретения — повышение чувствительности и избирательности определения.
Методика определения.
К анализируемой пробе прибавляют ацетон в количестве 5-12 об,Х, соляную кислоту до рН 1,5-3,0, 0,02Хный раствор ди-(п-сульфофенил)-тиокарбогидразида до появления синей окраски раствора, а затем прибавля„„SU„„525574 А 1
2 и мокет быть использовано для анализа сточных вод в этом производстве.
Анализ ведут добавлением в пробу
5-12 об.Х ацетона и HCl до рН 1,5-2 с последующей обработкой избытком нитрата висмута в присутствии индикатора ди-(п-сульфофенил)-тиокарбогидразида и титрованием полученной смеси раствором этилендиамннтетравцетата натрия. Эти условия повышают чувствительность с 3,4 до
О, 168 мг/л и избирательность определения, которому не мешают присутствие РЬ, Ип, Cu, Zn, d, А1, щелочно-земельных металлов, лантаноидов.
Относительная ошибка до 2,98Х.
3 табл. ют стандартный раствор нитрата висмута до перехода синей окраски раствора в розовую. Избыток висмута оттитровывают стандартным раствором
ЭДТА до перехода розовой окраски в синюю. Садеркание ЭДТА в анализируемой пробе (Х), мг/л, вычисляют по формуле aK> - Ъ.К.1 -Т -1000
V где а - объем прибавленного раствора нитрата, висмута,мп;
К, - поправочный коэффициент для приведения концентрации раствора нитрата висмута к гочно 5-10-> моль/л (или 5 .1О моль/л);
Ъ - объем ЭДТА, израсходованного на обратное титрование, мп;
1525574
К вЂ” поправочный коэффициент для приведения концентрации раствора ЭДТА к точно
5 1О моль/л (или 5 х х 10 4 моль/л)
Т вЂ” число миллиграммов ЭДТА, отвечающее 1 мл титранта (равно 0,0 168 при титровании 5 .10 -г моль/л растворами или 0,168 при титровании 5 10 моль/л растворами);
V — объем анализируемой пробы, мл.
Пример 1. В колбу для титрования вводят 1,5 мл 5 10 моль/л раствора ЭДТА, 20 мп дистиллированной воды, 5,5 мл ацетона (1О об.Х), 5 мл О, 1 моль/л соляной кислоты для создания рН 2, 0,7 мл 0,02Х-ного раствора ди-(и-сульфофенил)-тиокарбогидразида. Затем объем раствора доводят до 50 мп дистиллированной водой. Прибавляют 5 -10 моль/л ра-5 створа азотнокислого висмута до перехода синей окраски раствора в розовую. Избыток висмута оттитровывают 5 -10 моль/л раствором ЭДТА до перехода окраски индикатора из розовой в синюю. Объем прибавленного раствора нитрата висмута 2,0 мл; объем ЭДТА, израсходованного на обратное титрование,0,5 мл. Среднее значение содержания ЭДТА при шести параллельных определениях равно
0,506+0,007 мг/л. Относительная ошибка определения 0,39Х.
Пример 2. Определение ЭДТА в растворах моющего средства Вертолин", в состав которого входит
3 мас.Х ЭДТА.
Отбирают в колбу для титрования
50 мл анализируемой пробы, содержащей 0,270 мг/л ЭДТА, прибавляют бмп ацетона (10 об.Х), соляную кислоту до рН 2, 0,7 мп 0,02Х-ного раствора ди-(и-сульфофенил)-тиокарбогидразида и титруют 5 10 > моль/л раствором азотнокислого висмута до гурехода окраски раствора из синей в розовую. Затем избыток висмута оттитровывают 5 .10 моль/л раствором
ЭДТА до перехода окраски раствора иэ розовой в синюю. Объем прибавленного раствора нитрата висмута 1,5 мл; объем ЭДТА, израсходованного на титрование избытка висмута, 0,7 мп.
Среднее значение содержания ЭДТА при
1О
15 шести параллельных определениях равно 0,27?+0,005 мг/л. Относительная ошибка определения 0,74X..
Установлено, что высокие чувствительность и избирательность определения ЭДТА обеспечивает использование ди-(п-сульфофенил)-тиокарбогидразида только в водно-ацетоновой среде при содержании ацетона 5-12 об.X и рН среды 1,5-3,0. Зависимость чувствительности и точности определения
ЭДТА от условий проведения реакции представлена в табл.1.
Из приведенных в табл.1 данных видно, что заявляемые параметры— содержание ацетона и кислотность раствора - выбраны из условий, обеспечивающих максимальную чувствительность (О, 168 мг/л) и высокую точность определения ЭДТА в широком диапазоне его концентраций (примеры
1-16) .
Запредельное снижение концентрации ацетона при оптимальной кислотности среды приводит к резкому увеличению (7-8X) оавебкн определения ЭДТА (табл.1, примеры 17, 18, 23) вследствие нечеткого перехода окраски индикатора в точке эквивалентности.
Запредельное поввапение концентрации ацетона при оптимальном рН раствора приводит к получению завышенных результатов определения ЭДТА. Относительная ошибка определения при этом зависит от концентрации ацетона и возрастает от 7, 14 (13X по объему ацетона) до 70Х при содержании ЗОХ ацетона в растворе (табл. 1, примеры
19-22, 24 и 25).
Проведение определения в более кислых растворах при рН (1,5, где устойчивость комплекса висмута с с
ЭДТА падает и наблюдается переход окраски индикатора при добавлении количеств ЭДТА, не эквивалентных содержанию висмута в растворах, вызывает увеличение ошибки определения
ЭДТА до 5,95-9,52Х (табл.1, примеры
26, 27 и 30). В растворах с рН ) 3,0 устойчивость комплекса висмута с дн-(и-сульфофенил)-тиокарбогидразидом увеличивается в такой степени, что отсутствует переход окраски индикатора при титровании избытка висму55 та стандартным раствором ЭДТА, что не позволяет определять ЭДТА в этих условиях (табл.1, примеры 28, 29, 31 и 32).
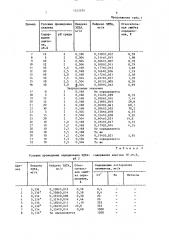
1«25574
Таблица 1
Относительная ошибка
Найдено ЭДТА, мг/л
Введено
ЭДТА, мг/л определения, Х
РН среды
Содержание ацетона, об. способ
О, 173+0,015
О, 170i0, 008
О, 16510 013
0, 164+0,014
0,342+0 020
О, 33510, 009
Пр едла r аемый
О, 168
О, 168
О, 168
О, 168
0,336
0,336
2,98
1, 19
1,78
2,38
1,79
0,30
8
12
1
3
5
Проведение определения ЭДТА в заявляемых условиях обеспечивает высокую избирательность. Зависимость чувствительности и точности определения ЭДТА от присутствия в раст5 воре различных количеств посторонних ионов представлена в табл.2. Иэ приведенных в ней данных видно, что хлорид-ионы (7000-кратные по массе количества) (пример 7) и железо (300-кратные по массе количества) (пример 13), которые наиболее часто сопутствуют ЭДТА в природных и сточных водах, не мешают определению.
Определению ЭДТА ие мешают также свинец, марганец, кобальт, медь, цинк, кадмий, алю;-ь-.иии, щелочно-земельные металлы, лаитаноиды.
Применение предлагаемого инди- 20 катора в отсутствие ацетона не позволяет вести определение ЗДТА в растворах, содержащих хлорид-ионы и ионы железа даже в небольших количествах (примеры 4, 12 и 14). В от- 25 сутствии ацетона ошибка определения
ЗДТА в растворах, содержащих 60кратные количества хлорид-ионов (табл.2, пример 4), увеличивается до
4,5Х. В растворах, содержащих 1000кратные количества хлорид-ионов (табл.2, пример 6), ошибка определения возрастает до 21 „ а еще пгн более значительном содержании хлорид-ионов определение 0,336 мг/л
ЭДТА становится невозможным (пример 8). На точность определения ЭДТА в отсутствие ацетона влияют ионы железа. Так, в присутствии 300-кратПример Условия проведения анализа ных количеств железа относительная ошибка определения ЭДТА составляет 9,8Х (табл.2, пример 14), а при совместном присутствии в растворе х.,орид-ионов (1000-кратных количеств) и ионов железа (3-кратных количеств) определение ЭДТА в отсутствпе ацетона становится невозможны. (табл.2, пример 12).
В табл.3 приведены данные, полученные по предлагаемому и известному способам.
Данный способ по сравнению с известным и >эволяет понизить нижнюю границу определяемых содержаний с
3,40 до О, 168 мг/л, т.е. в 20 раз, н повысить чэбирательность определения .
Формула изобретения
Способ определения этилендиаминтетраацетата в воде путем добавления к анализируемой пробе избытка нитрата висмута в присутствии нидикатора в кислой среде с последующим титрованнем полученной смеси раствором этилендиаминтетраацетата натрия, о т л и ч а ю, и и с я тем, чт:, с целью повышень., чу ствительиости и избирательности определения, в анализируемую пробу предварительно добавляют ацетон в количестве 5
12 об.Х, соляную кислоту до рН 1,53,0 н в качестве индикатора используют ди-(п-сульфофенил)-тиокарбогидраэид.
1525574
Продолжение табл.1
Найдено ЭДТА, мг/л
Относительная ошибка
Условия проведения анализа
Введено
ЭДТА, мг/л
Пример определения, Х
Содержание рН среды ацетона, об. Х
0,336
0,504
0,504
0,504
О, 168
О, 168
О, 168
0,504
0,504 ф,504
0,59
1,98
0,39
0,79
1,68
1,19
2,38
1,39
0,59
0,99
2
2
1,5
2,5
3,0
1,5
2,5
3,0
12
12
7
9
11
12
13
14
Запредельные
8,33
7,14
29,8
60,1
70,2
6,75
9,92
19,8
9,52
6,55
5,95
Таблица 2
Условия проведения определения ЭДТА: содержание ацетона 10 об.Х, рН 2
Найдено ЭДТА мг /л
Введено
ЭДТА, мг/л
Содержание посторонних элементов, мг/л тноПример снтельная ошибС1 Fe
Металлы ка определения, Х
0,4
0,4
1200
0,338i0,012
О, 338i0, 014
0,335+0,009
О, 32110,016
0,340 0,011
0 266+0 023
0,334Т0,014
0,59
0 59
0,30
4,46
1,19
20,8
0,60
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
Не определяется
17
18
19
21
22
23
24
26
27
28
29
31
О
13
2
2
2
2
2
1,0
1,2
3,3
3,5
1,2
3,3
3,5
О, 168
О, 168
О, 168
О, 168
О, 168
О, 168
0,504
О, 504
0,504
О, 168
0,168
О, 168
О, 168
0,504
0 504
0,504
0 338 0 012
О, 514+0,015
О, 506 О, 007
0,500+0,011
О, 171i0,О13
О, 166t0,О16
О, 172+0,021
0,49710,017
0,507+0,005
0,509+0,012 эначения
Не определяется
О, 154 0,039
О, 180t0,О14
0,218 0,015
0,269+0,041
0,286+0,052
0,538 0 019
0,554+0,018
0,604+0,031
О, 184+0,017
О, 179+0,014
Не определяется
То же
0 534 0 021
Не определяется
То же
1525574
Пр одогме ние та бл . 2
Содержание посторонних лементов, мг/л
ОтноНайдено ЭДТЛ, мг /л
Введено
ЭДТА, мг/л
Пример сительная ошибFe
Металлы ка определения, 0,340+0,021
0,339+0,019
0,341tO t015
Не определя
0,338+0,016
0,369+0,027
0,399+0,О31
0,504 0,039
0,339Ы,О!3
0 334 0,014
0,339 0,012
0 33440 О11
0 339 0,013
0,34110,014
0t339iOt011
0,335i0,015
0,337+0,012
О, 34 0+0, 011
0,339 0,009
2400
1, !9
0,89
1,49 ется
0,60
9,82
18,S
0,90
0,60
О,89
0,60
0,89
1,49
0,89
0,30
0,30
1,19
0,89
0,5
1,0
1,0
160
355
" В отсутствие ацетона.
Таблица 3
Пример
Введено
ЭДТА, мг/л
Предлагаемый способ
Иэвестный способ
Найдено
ЭДТА,мг/л
ОтносиОтносительная ошибка тельная опыбка определения, определения, Не определяется
0,079+0,009
О, 121+0,012
О, 170t0t 008
0,335+0,009
0,506+0,O07
0,839+0,004
1 69 0,01
2„340,02
Зэ35 0102
5,02+0,03
16,80+0,06
84,02+0,09
Не определяется
То ае
II
It
1, 77+0,23
342003
5,09+0,03
16,7640,11
84,01+0,09
24,6
1,79
0,99
0,30
0,05
11
12
13
14
16
17
18
19
21
22
23
24
26
1
3
5
7
9
11
12
0,336
0,336
0,336
0,336
0,336
0,336
0t336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,336
0,067
О, 101
О, 134
О, 168
0,336
0,504
0,840
1,68
2,35
3,36
5,04
16,81
84,05
21,8
9,7
1,19
0,30
0,39
О,!2
0,59
0,43
0,30
0,40
0,0
0,04
355
400 Си
400 Cd
400 Al
400 Zn
400 Pb
400 Со
400 Мп
400 РЗЭ
400 Са
400 Mg
400 Na