Электрохимический способ определения металлов в растворе
Иллюстрации
Показать всеРеферат
Изобретение относится к области аналитической химии и может быть использовано для определения металлов в объектах окружающей среды и в сточных водах. Цель изобретения - повышение чувствительности и селективности определения. Цель достигается тем, что используют дополнительный электрод, идентичный индикаторному, который помещают в анализируемый раствор. В период осаждения на дополнительном электроде задают потенциал на 0,1±0,05 В меньше, чем потенциал, при котором начинает выделяться анализируемый металл на индикаторном электроде. После осаждения электрод выдерживают 2 - 3 с в отсутствие поляризации. Растворение металла с индикаторного электрода осуществляют путем замыкания электродов через гальванометр. О концентрации металла судят по максимальному значению тока в момент замыкания электродов. 1 ил., 1 табл.
СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСНИХ
РЕСПУБЛИК
А1 (19) (11) (),р ц(р
6ГГГЛЗМ6
ПМ 11 И ч11ь 61
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
И ABTOPCHOMV СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТНРЫТИЯМ
ПРИ ГКНТ СССР
1 (21) 4321662/31-25 (22) 28.10.87 (46) 30.01.90. Бюл. Ф 4 (71) Специальное конструкторско-технологическое бюро по конструированию оборудования и приборов дпя очистки промышленных сточных вод "Казмеханобр" (72) В.В. Гадицкий (53) 543.253(088.8) (56) Ашкинази В.Е. и др. Упрощенный вариант инверсионнохронопотенциометрического анализа. — Зав. лабор., 1984, .1Il 66, с. 14-15.
Бонд A.M. Полярограпические методы в аналитической химии. М.: Химия, 1983, с. 111 †1. (54) ЭЛЕКТРОХИИИЧЕСКИ11 СПОСОБ ОПРЕДЕЛЕНИЯ MI."TAJIJIOB В РАСТВОРЕ (57) Изобретение относится к области аналитической химии и может быть исИзобретение относится к аналитической химии, а именно к способам количественного анализа металлов в растворах, и может быть использовано для определения металлов в объектах окружающей среды и в сточных водах.
Целью изобретения является повышение селективности и чувствительности определения.
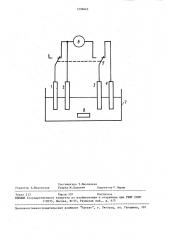
На чертеже приведена схема применяемой установки для определения кадмия .
Установка состоит из цинкового электрода 1, стеклоуглеродных электродов 2,3, кадмиевого электрода 4, двухполюсного переключателя 5 с нейтральпользовано для определения металлов в объектах окружающей среды и в сточных водах. Цель изобретения — повышение чувствительности и селективности определения. Цель достигается тем, что используют дополнительньш электрод, идентичный индикаторному, который помещают в анализируемый раствор .
В период осаждения на дополнительном электроде задают потенциал на 0,1+ 0,05 В меньше, чем потенциал, при котором начинает выделяться анализируемый металл на индикаторном электроде.
После осаждения электрод выдерживают
2-3 с в отсутствие поляризации. Растворение металла с индикаторного электрода осуществляют путем замыкания электродов через гальванометр. О концентрации металла судят по максимальному значению тока в момент замыкания электродов. 1 ил., 1 табл. ным положением микроамперметра 6 с различными пределами измерения, стака— на 7, магнитной мешалки 8.
Установка работает следующим образом.
Переключатель 5 переводится в крайнее правое положение, проводится электроосаждение кадмия и всех электроположительных металлов на электроде 2.
На электроде 3 кадмий не вьделяется, но выделяются все более электроположительные металлы. По истечении времени осаждения (время задается по секундомеру) переключатель 5 переводят на 2-8 с в нейтральное, а затем в крайнее левое положение. При этом за1539645 мечают, на какую максимальную величину отклоняется стрелка микроамперметра б. Эта величина является аналитическим сигналом.. Перед следующим измерением электроды протирают фильтровальной бумагой. Для контроля других .металлов необходимо подобрать материал электродов 1,4.
Предлагаемый способ реализуется следующим образом..
В анализируемый раствор погружают два идентичньгх индикаторных электрода (например, стеклоуглеродных) и поляризуют их в течение некоторого заранее заданного времени с использованием потенциостата или внутреннего электролиза. При этом задают потенгиал, при котором на одном электроде анализируемый металл выделяется, а на другом нет, но выделяются все мешающие электроположительные металлы. Затем электроды в течение
2-3 с выдерживают без тока поляриза.цки, Это время необходимо для того, чтобы электроды приняли потенциалы, близкие к соответствующей равновесной системе. За это время происходит перезарядка двойного электрического слоя, а также значительно снижается 30 фарадеевская составляющая фонового тока. По истечении этого времени вы— делившийся на индикаторном электроде металл начинает взаимодействовать с окислителями, присутствующими в раст- 35 воре, например растворенным кислородом или ртутью (II), если ее вводили в раствор, и часть аналитического сигнала теряется. Поскольку на индикаторном электроде анализируемый ме- 40 талл содержится, а на дополнительном электроде нет, то между ними за
2-3 с устанавливается какая-то разность потенциалов, определяемая различными факторами: наличием электро- 45 положительных металлов, составом фона, количеством выделившегося на индикаторном электроде металла и т.д.
За счет этой разницы при замыкании электродов через гальванометр потечет 50 .ток, максимальная величина которого характеризует количество анализируемого металла в растворе. Поскольку мешающие металлы выделяются как на индикаторном, так и на дополнительном электродах, то их наличие не оказывает влияния на анализ. Таким образом достигается селективность определения.
За счет того, что вводится бестоковая выдержка (при этом часть фонового тока компенсируется), потенциалы электродов отличаются, как правило, на
0,2-0,4 В, причем в момент замыкания каждый электрод поляризуется только на половину этой величины, поскольку в этом случае индикаторный электрод является анодом, а дополнительный— катодом, и устанавливается какой-то смешанный потенциал. Если анализируемый металл в анализируемом растворе
I отсутствует, то после 2-3 с выдержки электроды принимают одинаковый потенциал и фоновый ток не регистрируется, что повышает чувствительность анализа.
Пример 1. Готовят несколько модельных растворов, содержащих на фоне 1 М НС1 различные .концентрации кадмия, свинца, меди, которые заливают в ячейку объемом 100 мл. В ячейке размещена магнитная мешалка (скорость вращения 600 об/мин) °
Используют два одинаковых индика-. торных электрода из стеклоуглерода
СУ-2000 (диаметром 11 мм), а также металлические цилиндрические электроды из цинка, кадмия, свинца и меди диаметром 75 мм, погруженные на 25 мм в анализируемый раствор.
В качестве гальванометра используют вопьтамперметр Ц вЂ 43 или осциллограф, параллельно входу которого подключают сопротивление. 1 кОм, на которое соответственно рассчитывают ток.
Время осаждения для 1-7 опытов составляет 30 с.
Опыт 1. Определяют содержание кадмия 1,0 мг/л. На 30 с один стеклографитовый электрод соединяют с цинковым, а другой — с кадмиевым электродами (устанавливают потенциал, при котором кадмий не выделяется) . Затем стеклографитовые электроды отключают от металлических электродов и выдерживают без тока 2 с, после чего стеклографитовые электроды подключают к ,вольтамперметру Ц-4313. Фиксируют максимальный бросок стрелки 3,5 мА.
Концентрацию кадмия определяют по градуировочному графику — 1,0 мг/л.
Опыт 2. Проводят определение аналогично опыту 1, но в раствор дополнительно вводят 1,0 мг/л меди (II) °
Опыт 3. Проводят определение аналогично опыту 1, отмечая возможность анализа как по способу-прототипу, 1 так и по предлагаемому способу.
5 15396
Опыты 4,5. Проводят определение аналогично опыту 1 (в опыте 5 для регистрации тока растворения используют осциллограф). Отмечено что чувстви- Ф о Р У л а и з о б Р
1 .5 тельность определения предлагаемого способа в 1000 раз выше> чем способапрототипа. !
Введено, мг/л
Способ опыта Cd
Предлагаемый
Си
Прототип
Pb айдено, Максимальный Найдено, мг/л . ток, мкА мг/л ремя аство ения, 1,0
1,0
0,095
0,009
0,0001
1,0
1,0
31
0,29
1700
1,0
1,0
1,0
0,1
0,01
0,0001
2
4
5 .6
1,0
0,1
0,15
0,4
0,25
1,0
1,0
1,0
1,0
Опыт 6. Проводят определение свинца (ZI) аналогично опыту 1, но используют кадмиевый и свинцовый металлические электроды, Опыт 7. Проводят определение аналогично опыту 1, но используют кадмие-15 вый и медный металлические электроды.
Опыты 6 и 7 иллюстрируют возможность анализа различных металлов. Результаты опытов 1-7 сведены в таблицу.
Способ позволяет повысить селектив— ность определения в 10-20 раз, проводить анали з, если содержа ни е мешающих электроположительных металлов составляет 100-200Х от содержания анализируемого металла, повысить чувствительность в 1000 раз (см. опыты 4,5,8); упростить метод анализа: для анализа необходимы только секундомер, переключатель, мешалка, набор электродов, 30 что позволяет проводить анализ в по45 6 левых условиях; ис ключить не обходи— мость применения токсичной ртути (ZZ) Электрохимический способ определения металлов в растворе, включающий их предварительное электрохимичес кое осаждение в виде металла на индикаторном электроде и последующее электрохимическое растворение, о т л ич а ю шийся тем, что, с целью повышения селективности и чувствительности определения, дополнительный электрод, идентичный индикаторному, помещают в анализируемый раствор и в период осаждения задают на нем потен- циал на (0,1+0,05) В меньше, чем потенциал, при котором начинает выделяться анализируемый металл на индикаторном электроде, после осаждения электроды в течение 2-3 с выдерживают в отсутствие тока поляризации, затем растворение металла в индикаторного электрода осуществляют путем замыкания электродов через гальванометр между собой, а о концентрации металла судят по максимальному значению тока в момент замыкания электродов.
1539645
Составитель Т.Николаева
Техред M.Õoäàíè÷ Корректор С. Черни
Редактор А.Маковская
Заказ 213 Тираж 501 Подписное
ВНИИПИ Государственного комитета по изобретениям и открьггиям при ГКНТ СССР
113035, Москва, R-35, Раушская наб., д. 4/5
Производственно-издательский комбинат "Патент", r, Ужгород, ул. Гагарина, 101