Способ определения железа
Иллюстрации
Показать всеРеферат
Изобретение относится к химическому анализу и может быть использовано для определения железа в промышленных водах, содержащих примеси металлов, и чистых реактивах, в которых железо находится в качестве примеси. Целью изобретения является расширение интервала определяемых концентраций при повышении селективности и точности определения. Анализируемый раствор, содержащий железо, смешивают с нитратом 9-циано-10-метилакридиния. Добавляют смесь перекиси водорода, о-фенантролина и ацетатного буфера с PH 5,0-5,3, взятых в оптимальных соотношениях, и при получении светящейся смеси измеряют сумму хемилюмиесцентного свечения за 60 с. 2 табл., 3 ил.
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК
„„SU„„1567939
А1 (51)5 С 01 !х! 21 76
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
2 (54) СПО(.ОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (57) Изобретение относи»ся к химическому анализу» может быть использовано для определения железа в промышленных водах. содержащих примеси металов. и чистых реактивах, в которых железо находится в качеств» примеси. Целью изобретения является расширение интервала определяемых концентраций при повышении селективности и точности определения. Анализируемый раствор, содержащий железо, смешивают нитратом 9-циано-10-метилакридиния.
Добавляют смесь перекиси водорода, о-фенантролина и ацетатного буфера с рН 5,0—
5,3, взятых в оптимальных соотношениях, и при по:»учении светящейся смеси измеряют сумму хемилюминесцентного свечения за 60 с. 2 табл., 3 ил.
1,. б . ° » . I!, i 1..o 1»ус гим«o сo, ;ер—
)"Х»»»»»Е . «3»» .»
Привнес ь
>) (1 !) (та) i,0
2,0
1, !) р
»!) и»
0! )
Г т ! !!
I Т l, . (1., Cт -т) (. ) 3,()
1,5 ъ 3
5,()
1,0
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
flO ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР (21) 4467276/31-25 (22) 26.07.88 (46) 30.05.90. Бюл. № 20 (71) Львовский государственный университет им. Ив. Франко (72) А. М. Гута, С. В. Мидяный, В. А. Яртысь.
Р. Д. Мыцук и И. !О. Завалий (53) 543.42(088.8) (56) Долманова И. Ф., Рычкова В. И. и
Пешкова В. М. Определение микроколичеств железа с использованием каталитической реакции окисления и-фенетидина периодатом калия. — ЖАХ, т. 28, вып. 9, 1973, с. 17631767.
Калиниченко И. E. и Грищенко И. M Активирование солей железа диэтилентриамином при окислении люминола перекисью водорода. — Украинский химический журнал, т. 36, 1970, № 6, с. 6! 0- — -613.
Изобретение относится к химическому анализу и может быть использовано для ог:— ределения железа в промышленных водах. содержа щих п римеси металлов. и чистых реактивах. в которых железо находится в качестве примеси.
Цель изобретения — расширение интервала определяемых концентраций при повышении селективности и точности определения.
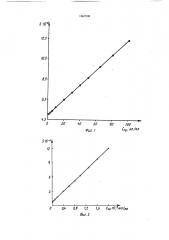
На фиг. 1 изображен рабочий калибровочный график для определения железа в пределах его содержаний 2,5 — 100 нг в 1 мл раствора; на фиг. 2 — то же, в пределах его содержаний 100 — 1700 нг в 1 мл раствора; на фиг. 3 — то же, в пределах его содержаний 1700 — 10000 нг в мл раствора.
Допустимые содержания примесей в анализируемом растворе, не мешающие определению железа, приведены в табл. l.
ХРОМ (3 ! (оба»; ьт х!ар г:» пои
".(<-. )», (» » !
1и», с 3»». (fir»i»», (!
Рту»» »? . ».Г»»»»М»; И И и (! .. 33» . !!» »
Ос .-»»» 3 » .!. i:3ò,»»»;»
l I r1. » 3»:; . r r!!»
Впнаии»»
Т»»т»» : (1.Г 3
10)
1 ()
1 (3
») 3
I !
)и
1C)
1 О) ,0
1, 5
1 Г) ) 56)7<)39
В табл. 2 приведены максимальные знач(ння отп<н и гельllhlx ошн(н)к определения железа длн разли Illblx его концентрационных интервалс)в. 1 б л и и а 2
11птep»;I. (олержпний Г1а коим()льная отжелез», нг./мл носительная ошибка определения, 7.
2, >-15
1 5-40
40-1 00
100-300
300-900
900-1700
1700-".ООО
5000-10000
2,0
1,6
1,4
1,2
0,9
0,7
О 8
1,2
Концентрации нитрата 9-пиано-10-метила криди пня, перекиси вод< рода, о-фенантролина и рН ацетатного буфера выбраны оптимальными для хемилюминесценции, т. е. для ))ол уче»а нбол bllle и разности м(жду ны ходом сB(òB в смеси, содержащей железо
25 и без него, что обуславливает чувствительносtt и точность определения железа.
Выбор оптимальных концентраций реагентов: (3,0 8,0) .10 моль/л — для нитрата
9-ци Illo-10-мет ил акрнднния; ),3 — — 1,7 моль/
/л -- для пс рекиси водорода; (4-- зр
6) 10 моль/л - д ч)) о-фенантро зина и оптим:)льlloro рН (5.0--5,3) ацетагного буфера, сделан и;) основании результа и в эксперимента. УOTBíoBëåío, IT<) независимо ()T
<.оогношеннн содержаний других компоненТ<>В оптил(>)явные концентрации нитрата
9-цнано-1О-метила <ридиния, перекиси водоро да. о-фе)(антролина и оптимального рН зцетатного буф< ра соответствуK)T указанным.
У
Количества реагентов, а также значения рН BI
Выбор оптимальной концентрации ацетатно го буфер; ) сделан и а основании топ>, что концентрация ацетатного буфера 0,17 моль/л
<)озполнст обеспечить необходимук> буферную емкость. I lðH кон<(с нтрациях ацетатпого буфера меньших, чем 0,17 моль/л, вслед- 5р ствие низкой буферной емкости, рН конечной смес н не соответствует рН буфера; количе< тва ацетатного буфера, превышающие 0,17 моль/л, заметно тушат свечение.
Замена ацетатного буфера на универсальцый фталатный или фосфатный приводит 55 к уменьlll< ник) раз)п>сти светосумм в присугсгнии желе)a и без него. Так, при применс сии <1)ос<1)атного буфера разность свечепия уменьнгалась приблизительно в 3 раза, IT() lip H B<)äèò к сни же ни ю ч увстви тельное>ии и точности.
В <)IITHMaльных условиях значение светосуммы за 60 с достигает максимального значении при содержании железа 10 мкг/мл, затем уменьшается при дальнейшем увеличении содержания железа.
Лин(.иная )B BHcHMo(Tb cB< тосум мы oT содержа (ия железа наблюдается в интервале еп> содержаний от 2,5 нг/мл до 1,7 мкг/мл.
Н редел обнаружения рассчитан по Зп-крите.г)ию и c<>CIBBëÿåò 2,5 нг железа в 1 мл растнора. (!ример. Лнализируемый раствор. содержащий железо в пределах от 2,5 до
l0() нг/мл, смешивают с нитратом 9-циано-! ()-метилакридиния и вносят в кювету хемнлк>мнн(сцентного фотометра. Затем в Kloш <у прибавляют смесь перекиси водорода, ацетатного буфера с рН 5,0 и о-фенантролина. Концентрации реагентов в расчете на конечный объем смеси должны составлять: для нитрата 9-циано-10-метилакридиния
:1,0 lÎ моль/л, для перекиси водорода—
1,3 моль/л, для о-фена нтролина
4,().! О моль/л и для ацетатного буфера с р11 5,0 -0,17 моль/л. (. помощью хемилюминесцентного фотометра измеряют сумму выделившегося света за 60 с н ее значение в дальнейшем используют для определения концентрации железа с помоп<ью калибровочного графика (фиг. 1) . Относительная ошибка определения не превышает 1.7%.
Использование предлагаемого способа да T возможность опрс деления келеза в ширс>ком концентрационном интервале от нг/мл до 10 мкг/мл и обеспечиваег высокую точность и селеKTHBHocTb опр..деления.
Формула изобретения с пособ определения железа, включаю<ций взаимодействие железа с органическим со< динениеM B присутствии перекиси водорода и регистра пик) хемилюминесценгного свечения образующейся смеси, IIo светосумме к<>горого о>)ределяют количество железа, г)тличающийсн тем, ITo с целью расширения интервала определяемых концентраций при увеличении селектнвности и точности определения в; нализируемый раствор, содеркагц>)й 2,5 нг/мл -- 10 мкг/мл железа вводят (3,0 — 8,0) ° 10 моль/л нитрата 9-пиано- 10-метилакридиния, добавляют смесь, состоящую l(B 1,3 — 1,7 моль/л перекиси водорода, (4,0--6,0) 10 моль/л о-феньнтроли<(а и 0,17 моль/л ацетатного буфера с рН 5,0 --5,3, и регистрируют в течсние не
М< нее 60 с светосумму хемилюминесценгного cвечения.
1567939 б0
f00
Ci, иг/ги
Рыг. 1
0,4 О,д 1,2 fp 0 Ске Ю-гмкГlмл
Фиг. г!
567939
$10
2,2
z,à
1,2
lд
i & уmrW
Составитель О. Бадтиева
Редактор М. Келемеш Техред И. Верес Корректор А. Обручар
Заказ 13!8 Тираж 5! 2 Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж вЂ” 35, Раушская наб., д. 4!5
Производственно-издательский комбинат «Патент», г. Ужгород, ул. Гагарина, 101