Способ определения карбоангидразы
Иллюстрации
Показать всеРеферат
Изобретение относится к биохимии и касается исследований в энзимологии. Цель - повышение точности и воспроизводимости анализа. Способ основан на реакции дегидратации бикарбоната с удалением образующейся в результате дегидратации двуокиси углерода при интенсивном барботировании реакционной среды освобожденным от CO 2 воздухом и одновременной регистрацией скорости изменения PH. Активность карбоангидразы определяют по изменению начального значения PH 8,2 - 8,7. Коэффициент вариации способа в серии из 5 определений равен 2,55%. 2 ил., 1 табл.
союз советских соОиАлистичесних
РЕСПУБЛИК (51) 5 С 12
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К А BTOPCHOIVIY СВИДЕТЕЛЬСТВУ
ГОСУДАРСТВЕННЫЙ КОМИТЕТ по изоБ етекиям и откРытиям
ПРИ ГКНТ СССР (21) 4410233/31-13 (22) 23.02.88 (46) 15.08.90, Бюл. № 30 (71) Институт физиологии и биофизики растений АН ТаджССР (72) В,В,Аракелян, В.Л.Калер и Г.Б.Ибрагимова (53) 577.15.08(088.8) (56) Gibbona В.Н., Edsall Е.Т
Kinetic Studies of Human Carbonic
Anhydràsås Bande. — J. Biol. Chem,.
1964, v. 239, ¹ 8, р,,2539-2544.
Devoe Н., Kistiakowsky G.Â.
The Enzymic Kinetics of Carbonic
Anhydrase from Bovine and Human, Erythrocytes. — J. Amer. Chem, $ос., 1961, v. 83, № 2, р. 274-280.
Изобретение относится к биохимии и касается исследований в энзимологии.
Цель изобретения — повышение точности и воспроизводимости анализа.
Способ определения активности карбоангидразы основан на реакции дегидратации бикарбоната: НСО, ОН + з
+ СО Фс удалением образующейся в ре1 акции дегидратации двуокиси углерода при интенсивном барботировании реакционной среды освобожденным от
СО воздухом и одновременной регистрации скорости изменения рН.
На фиг. 1 изображена схема установки для удаления СО иэ реакционной среды.
Воздух подается в реакционную среду, находящуюся в реакционном со-.
09) (11) . i
2 (54) СПОСОБ ОПРЕДЕЛЕНИЯ КАРБОАНГИДРАЗЫ (57) Изобретение относится к биохимии и касается исследований в знэимологии. Цель — повышение точности и воспроизводимости анализа. Способ основан на реакции дегидратации бикарбоната с удалением образующейся в результате дегидратации двуокиси углероца при интенсивном барботировании реакционной среды освобожденным от СО воздухом и одновременной регистрацией скорости изменения рН, Активность карбоангидразы определяют по изменению начального значения рН 8,2 — 8,7. Коэффициент вариации ф способа в серии иэ 5 определений равен 2,557.. 2 ил, 1 табл. суде 1, через обратный фильтр 2 (диаметр пор 14,4 мкм), подключенный через резиновую трубку 3 с краником 4 к склянке 5 Дрекслера с раствором щелочи и к системе сжатого воздуха либо к микрокомпрессору. Для измерения рН реакционной среды используют электроды 6, Реакцию запускают барботированием реакционной среды, воздухом, освобожденньм от СО . Активность карбоангидразы определяют по изменению начального значения рН от 8,2 до 8,7 в реакции дегидратации COz. Электро" метрически измеряют скорость накопления гидроксильных ионов с использованием чувствительного рН-метра (рН 121) с самописцем (КСП-4) по
1 585334 сдвигу рН от 8,2 до 8,7, как функции от времени на линейном участке.
Способ иллюстрируется примером.
Пример I. .Контрольное определение.
В опытный сосудик помещают 9,5мл
0,1 М раствора NaHC0> (рН 8,2) и
0,5 мл среды, которую используют для получения исследуемого препарата фер- 10 мента (без фермента).
Опытное определение осуществляют так же, как и контрольное, но в со. судик помещают 0,5 мл опытного образца (исследуемый препарат фермента).
Перед опытом проверяют значение рН исследуемого образца, чтобы оно было равно начальному значению рН 8,2 раствора NaHCO>.
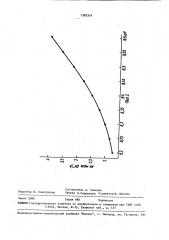
Расчет активности производят по графику зависимости концентрации гидроксильных ионов от рН, построенному на основании ионного произведения воды (фиг. 2).
В присутствии ферментного препара- 25 та накапливается 0,035 мкмоль ОН /мин, а без фермента (контроль) — 0,019мкмопь
ОН /мин. По разности опытного и контрольного вариантов (0,035 — 0,019
= 0,016) находят .количество мкмоль
0Н /мин, образовавшееся в про цессе.ферментативной реакции. В реакционную среду было внесено 1 00 мкг . белка. В пересчете на 1 мг белка активность фермента составляет 0,16 мкмоль ОН мг мин
Анализ точности и воспроизводимости результатов при определении активности карбоангидразы по реакции дегидратации НСО по величине довериЭ тельного интервала (S > t О, ц (4)
0,004) и коэффициенте вариации (Ч = 2,55X) следующий.
Пример Активность карбоангидразы по дегидратации НСО мкмоль ОН мг мин—
0,155
0,150
0,158
0,153
О, 160
Формула изобретения . Способ определения карбоангидразы, включающий смешивание раствора субстрата, в качестве которого исполь эуют бикарбонат натрия, с анализируемым образцом фермента и инструментальную регистрацию изменений рН реакционной смеси, вызываемых катализируемой ферментом реакции дегидратации бикарбоната до углекислого газа, отличающийся тем, что, с целью повышения .точности и воспроизводимости анализа, изменения рН реакционной смеси регистрируют электрохимическим способом, причем в процессе регистрациичерез реакционную смесь барботируют воздух, очищенный от углекислого газа.!
585334
u/ù тонхи
Составитель А. Семенов
Текред Л.Сердюкова Корректор М, Шарони
Редактор Н. Киштулинец
Заказ 2304 Тираж 486 Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат "Патент", г. ужгород, ул. Гагарина, 101