Способ определения пероксидазной активности крови
Иллюстрации
Показать всеРеферат
Изобретение относится к биологии и медицине и может быть использовано в диагностике состояния перекисных процессов в организме Цель изобретения - повышение точности способа о Способ заключается в том, что при 25°С инкубируют опытную пробу , содержащую ацетатный буфер, индигокармин в концентрации 4-10 М, перекись водорода и гемолизат крови, разведенный в 3000 раз, а также контрольную пробу, не содержащую крови. Измеряют кинетику изменения оптической плотности опытной и контрольной проб, . продолжают инкубацию опытной пробы до прекращения изменения оптической плотности, а активность пероксидазы рассчитывают по Лормуле 2 табл.Q
СОЮЗ СОЕЕТСНИК
И
РЕСПУБЛИК
„„SU„„1644035 (gg)g О 01 N 33/52 33/68
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
И А ВТОРСНОМ У СВИДЕТЕЛЬСТВУ
1п(у) п (Л
0,056 и где А
D о
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
flO ИЗОБРЕТЕНИЯМ И OTHPbITHAM
ПРИ 1ННТ СССР (21) 4351815/14 (22) 28.12.87 (46) 23.04.91. Бюл. Р 15 (7 1) Ялтинский научно-исследовательский институт физических методов лечения и медицинской климатологии им. И.И.Сеченова (72) В.Л.Семенов и И.Ф.Шинкарчук (53) 612.015(088.8) (56) Попов 7., Нейковска Л. Гигиена и санитария, 1971, Р 10, с. 85-91. (54) СПОСОБ ОПРЕДЕЛЕНИЯ ПЕРОКСИ АЗНОЙ
АКТИВНОСТИ КРОВИ (57) Изобретение относится к биологии и медицине и может быть использовано в диагностике состояния переИзобретение относится к биологии и медицине, точнее к лабораторным исследованиям,.и может быть использовано для диагностики перекись-разрушающих систем организма.
Цель изобретения - повышение точности способа.
Способ осуществляется следующим образом.
Пробу крови разводят в 3000 раз.
Инкубируют опытную пробу, содержащую ацетатный буфер индигокармин концентрации 4 10 М, перекись водорода
Д и гемолизат крови, а также контрольную пробу, содержащую предварительно нагретые до 250 С ацетатный буфер, индигокармин и перекись водорода.
Инкубацию проводят при 25 С. Измеряют в течение 2 мин кинетику изменения оптической плотности опытной и контрольной проб при 25 С, затем продол2 кисных процессов в организме. Цель изобретения — повышение точности способа. Способ заключается в том, что при 25 С инкубируют опытную пробу, содержащую ацетатный буйер, индигокармин в концентрации 4 10 М, перекись водорода и гемолизат крови, разведенный в 3000 раз, а также контрольную пробу, не содержащую крови.
Измеряют кинетику изменения оптической плотности опытной и контрольной проб, продолжают инкубацию опьггной пробы до прекращения изменения оптической плотности, а активность пероксидазы рассчитывают по формуле.
2 табл, жают инкубацию опытной пробы до прекращения изменения ее оптической плотности, активность пробы до прекраще.ния изменения ее оптической плотности, а активность пероксидазы рассчитывают по формуле активность пероксидаэы крови, л мл мин момент времени измерений, мин; значение оптической плотности опытной пробы до начала инкубации (С=О); значение оптической плотности после прекращения ее изменения при инкубации в опытной пробе;
1644035
Э - значения оптической плотности к соответственно в опытной и контрольной пробах в момент времени .
Пример 1. У донора П-ва взяли
0,02 мл крови из пальца,и развели его дистиллированной водой в соотношении
1:3000. Все используемые в работе растворы перед измерением 10 мин выдер- 10 живали в термостате при 25 С. В терь мостатированной при 25 С кювете фотометра ЛМФ-72 смешали 1 мл 0,2 И ацетатного .буфера, рН 4,9, 0,5 мл 4х10 54 индигокармина, 0,5 мл 0,03 N раствора перекиси водорода и измеряли оптическую плотность (Э реакционной смеси опытной пробы в процессе инкубации при длине волны 610 нм через каждые 15 с в течение 2 мин. Реакционную смесь сливали в пробирку и инкубировали в термостате в течение
1-1,5 ч, до тех пор, пока ее оптическая плотность практически не изменилась во времени, т,е, получали значе- 25 ние оптической плотности реакционной смеси, в которой индигокармин был полностью окислен (Э„). Ее величина может быть использована для серии измерений при условии использования этих же реактивов.
Контрольную пробу, отличающуюся от опытной тем, что вместо 0,5 мл образца крови смешивали 0 5 мл воды, инкубировали аналогично опытной и измеряли таким же образом ее оптичес35 кую плотность.
Расчет константы первого порядка скОрОсти Окисления индигОкарм™на В 40 опытной и контрольной пробах осуществляли аналитически по формуле:
К(пп g) (1п(Эр Эао) / (Эф «Do+)g / Су где Ф вЂ” время, мин;
Эр,М,Эа, — оптическая плотность реакционной смеси соответственно в начальный момент реакции, к моменту времени и после окончания реакций.
Графический расчет, константы скорости в Опытной и контрольной пробах имеют преимущества перед аналитичес- . кими, так как для его определения отсутствует необходимость определения величины Do. Графический расчет вы55 полняется путем построения графика в координатах 1n(O„"D ) . Тангенс угла наклона прямой к оси дает численное значение величины константы скорости.
Данные измерения кинетики окисления индигокармина в опытной и контрольной пробах и аналитический расчет константы скорости представлены в табл. 1.
График в коорпинатах Dq-D, © опытной и контрольной проб имеет вид экспоненты. Зависимость 1п(Э -Э ) от имеет линейный характер. Эти графики указывают на первый порядок реакции в опыте и контроле. Тангенсы углов наклона прямых к оси 6 дают (1. значения констант скоростей в опыте и контроле соответственно. 0,24 и
-(0,03 мин, что хорошо согласуется с аналитическим расчетом. Используя значения констант скоростей в опытной и контрольной пробах, полученные аналитическим или графическим расчетом вычисляем пероксидаэную активВ ность крови (ПАК) по формуле ПАК=
=(Коп-Kg)g) /B, rpe Kon H Ккон константы первого порядка скорости окисления индигокармина соответственно в опыте и контроле,. В=0,056 — концентрация крови в реакционнбй смеси (мл/л):
PAK- †- -3 96 мин мл л ° (О 26-0 04) 1 (0,056
ПАК= — =3 78 мин мл л. (О 24-0 03) r 4
0,056
Различие результатов пероксидазной активности крови между графическим и аналитическим расчетом не превьппает
57.
Пример 2. У группы лиц (2 донора и 4 пациентов с воспалительными заболеваниями органов дыхания) взяли по 0,02 мл крови из пальца, которую развели дистиллированной водой 1:1000 (эти образцы использовались для определения пероксидазной активности по прототипу) и 1:3000 (для оценки пероксидазной активности по предлагаемому способу).
Данные измерения предс гавлены в табл. 2, Анализ табл, 2 показывает, что пероксидазная активность крови, определенная по известному способу, у пациентов с воспалительными заболеваниями легких находится в пределах величины, измеренных у доноров. Принимая во
1644035 внимание, что контрольная проба в иэвестном способе не позволяет определить скорость окисления индигокармина перекисью водорода (без пероксида5 зы), была поставлена проба, содержащая эквивалентные концентрации перекиси водорода, индигокармина, буферного раствора, но без образца крови и проведена инкубация ее согласно грототипу. Ее экстинция эа
2 мин инкубации составила 0,25. Но при такой экстинции контрольной пробы у
3 из 5 обследуемых лиц разница экстинций между опытом и контролем (дЕ) оказывается отрицательной величиной, что вряд ли соответствует действительности. Эти результаты указывают на недостаточную точность известного способа определения перокси- 20 даэной активности крови, возможные причины которой изложены вышее.
Изменение пероксидазной активности крови по предлагаемому способу показывает, что ее величина у пациентов 25 вышее, чем у доноров. Эта оценка учитывает именно пероксидазную активность крови (т.е. с учетом неферментативного окисления индигокармина), находится в соответствии с кинетическими закономерностями реакции, и адекватно соответствует измеряемому показателю.
Таким образом, предлагаемый способ позволяет повысить точность определе- 35 ния пероксидазной активности крови за счет использования технологии проведения реакции, учитывающей неферментативное окисление индигокармина перекисью водорода, использование адек- 40 ватного кинетике реакции констант первого порядка скоростей окисления индигокармина в суммарной (неферментативной + ферментативной) и неферментативной реакциях, разность констант 45 которой, отнесенных к концентрации крови в реакционной смеси, прямо пропорциональна пероксидазной активности крови. Точность и простота способа позволяет использовать его в любых лечебно-профилактических учреждениях, не требует по сравнению с известным способом дополнительного оборудования, реактивов и других средств на внедрение.
Формула изобретения
Способ определения пероксидазной активности крови путем забора крови, ее разведения, инкубации опытной пробы, содержащей ацетатный буфер, нндигокармин, перекись водорода и гемолиэат крови, и контрольной пробы, содержащей ацетатный буфер и индигокармин, с последующим измерением оптической плотности опытной и контрольной проб, отличающийся тем, что, с целью повышения точности способа, используют кровь, разведенную в
3000 раз, индигокармин в концентрации
4 ° 10 5моль, в контрольную пробу дополнительно вносят перекись водоро-. о да, инкубацию проводят при 25 С, измеряют кинетику изменения оптической плотности опытной и контрольной проб, продолжают инкубацию опытной пробы до прекращения изменения оптической плотности, а активность пероксидазы рассчитывают по формуле
A=(ln (D -D )/(В „DQ)-In ((По DP/
) („=a„)g 1 У0,056 с, где А — активность пероксидазы, л мл мин ;
+c — момент времени измерения, мин;
П, — значение оптической плот, ности опытной пробы после прекращения ее изменения;
D B — значения оптической плотности соответственно в опытной и контрольной пробах в мол. мент времени ь;
9 — значение оптической плотности опытной пробы.до начала инкубации при 6=0.
1644035
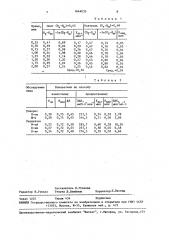
Таблица 1
Р -Р
Контроль (Р -Р, )=0,48
Опыт (Р -Р )=0,45
Время, мин
Дп(Р D ) К (D D ) Ы(Р D ) К ,мин
0,25 0,41
0,50 0,39
0,75 0,37
1,00 0,34
1,25 0,32
1,50 0,30
1,75 0,29
2,00 0,27
Таблица 2
Обследуемые лица
Показатели по способу известному предлагаемому
Екон Е
1 Кол ° КМон
Mia мин мин мин мин.мп л
0,30 0,75 0,45 257,1 0,24 0,03 3,78
0,20 0,75 0,55 314,3 0,21 0,04 3,06
0,60 0,03 10,26
0,38 0,02 6,48
0,39 0,02 б,бб
0,22 0,72 0,50 285,7
0,27 0,72 0 45 257,1
0,24 0,72 0,48 274,3
Составитель Н.Гуляева
Редактор Н.Гунько Техред Л.Олийнык
Корректор Л. Бескид
Заказ 1237 Тираж 434 Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат "Патент", r.Ужгород, ул. Гагарина,101,0оноры:
П-ов
Ш-к
Пациенты:
М-ой
К-ин
П-ак
0,89
0,94
0,99
1,08
1,14
1,20
1,24
1,31.
0,17
0,29
0 ° 26
0,28
0,28
0,27
0,26
0 25
Сред.=0,26
0,47
0,47
0,47
0,46
0,46
0,45
0,45
0,44
0,74 0,05
0,76 0,05
0,76 0,04
0,78 0,04
0,78 0,03
0,80 0,04
0,80 0,03
0,82 0,03
Сред.=0,04