Способ получения производных 2-аминоизохинолина
Иллюстрации
Показать всеРеферат
СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСН ИХ
РЕСПУВЛИН
ПРИ ГННТ СССР
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н llATEHTV
ГОСУДАРСТВЕННЫЙ НОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТНРЫТИЯМ (21) 4613229/04 (22) 30.12.88 (31) 6132/87 (32) 30. 12.87 (33) HU (46) 07. 09. 91. Бюл. N 33 (71) Хиноин Дьедьсер еш Ведьесети
Термекек Дьяра PT (HU) (72) Эндре Палоши, Дже Корбонитш, Эржебет Молнар, Ида Свобода, Ласло Харшинг, Дьердь Шимон, Вера Гергели, Петер Кермеци, Шандор Вираг и Каталин Мармароши (HU) (53) 547.781.785.07(088.8) (56) Бюлер К„, Пиосон А. Органические синтезы. Ч. I Мир, 19/3, с. 504. (54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
2-AMHHOH30XHHOJlHHA (51) Изобретение относится к гетероциклическим соединениям, в частности
Изобретение относится к способу получения новых производных 2-амино-1,2,3,4-тетрагидроизохинолииа, которые могут найти применение в качестве мочегонных и салуретических средств.
Цель изобретения — синтез новых соединений в ряду тетрагидроизохинолинов, обладающих более высокой активностью, чем гипотиазид, применяемый для тех же целей.
Б р и м е р 1. 43,3 r 2-амино-1,2,3 4-тетрагидроизохинолин-гидро хлорида и 24,5 r карбоната кальция. Ж 1676444 А3
Щ) С 07 0 217/08// А 61 К 31/47
2 к получению производных 2-аминоизохинолина ф-лы
R В 5
О
R ЬН 3Н- СО О С1
R3 .>02 Н2 ". где R< и R< — H или метоксигрупла;
Н3 u R g — Н или группа СН, Rg — Н или С1, которые могут найти применение в качестве мочегонных и салуретических средств, Бель — разработка способа получения более активных соединений. Получение ведут реакцией производного 2-аминоизохинолина с производным карбоновой кислоты.
1 табл. перемешивают в течение 30 мин в
400 мл приготовленной в отношении
2:1 смеси из диоксана и воды. К суспензии при перемешивании при комнатной температуре добавляют небольшими частями 59,5 r 4-хлор-3-сульфамил-бензоилхлорида. Через 2 ч разбавляют реакционную смесь 300 мл воды.
Осаждающиеся кристаллы отсасывают, промывают водой, затем 0 5 н. соляной кислотой и снова водой. В форме белых кристаллов получают /1,9 г (847) 2 — (3 -сульфамид-4 -хлорбензоил)-амнно (-1,2,3,4-тетрагидроизохинолина, который после переосажде16/6444
2» ния в основной среде имеет т, пл.
225 228о C.
Вычислено, : С 52,53; Н 4,41;:
N 11,49; cl 969; s 8, //.
С l6H16 ClNgO gs
Найдено, .: С 52,26; Н 4,41;
N 11,32,:Cl 9186; S 8ю90
Пример 2. Исходят из 28,2 r
1-метил-2-амино-1,2,3,4-тетрагидроиэохинолина, 1 /,5 г карбоната кальция, 43,2 r 4-хлор-3-сульфамил-бензоилхлорида и 350 мл упомянутой смеси диоксана и воды и аналогично примеру 1 получают 48,3 г (14,8 )
1-метил- - 3 -сульфамил-4 -хлорбенГ 1 I зоил)-амино)-1,2,3,4-тетрагидроизохинолина, который после переосаждения в основной среде разлагается при
22/-229 С. 20
Вычислено,, .: C 53, /5; H 4, /8;
N 11,06; С1 9 33 S 8,44.
С !-/ H16 ClN 0 s, Найдено, :;С 53,86; Н 4,66;
N 11,1/; cl 9,41; s 8,48., Получение исходных веществ. а) Раствор 21,5 г 1-метил-1,2,3,4- тетрагидроиэохинолин-гидрохлорида в 50 мл воды при /5 С в течение 1 ч смешивают по каплям с раст- 30 вором 8,22 r нитрата натрия в 25 мл воды. Реакционную смесь перемешивают при 15 С 2 ч, затем охлаждают и экстрагируют 6х30 мл хлороформа. Органическую фазу промывают 50 мл воды, сушат и выпаривают в вакууме. Полу3» чают в форме коричневого масла
19,2 г (93X) 1-метил-2-нитрозо-1,2,3,4-тетрагидроизохинолина, который без дальнейшей очистки примейяют в следующей стадии. б) Полученное в стадии а нитрозосоединение растворяют в 32 мл ледяной уксусной кислоты и при охлаждении ледяной водой и перемешивании до- 4» бавляют по каплям в суспензию 31,9 г цинковой пыли в 30 мл воды. Реакционную смесь перемешивают 1 ч при охлаждении ледяной водой и 2 ч без охлаждения, затем нагревают до 85 С и фильтруют. Оставшийся на фильтре цинк промывают 3х20 мл кипящего водного раствора 5 .-ной соляной кислоты.
Фильтрат доводят до щелочного состояния при помощи 40Х-ного натрового щелока н затем экстрагируют 4х100 мл хлороформа. Органическую фазу промывают водой, сушат и выпаривают в вакууме. В качестве коричневого масла получают 18 г (! OOX-ного) 1-метил-2-амино-1,2 3,4-тетрагидроизохинолина, который беэ очистки применяют дальше.
Пример 3. Исходят из 28,1 г
1-метил-2-амино-6,/-диметокси-1,2,3,4-тетрагидроиэохинолина, $ г карбоната кальция, 32, 1 r 4-хлор-3-сульфамил-бенэоилхлорида и 20 мл (2:1) смеси диоксана и воды и аналогично примеру 1 получают 50 г (90X) 1-метил-2- ((3 -сульфамил-4 -хлорбенэоил)-амино1-6,/-диметокси-1,2,3,4-тетрагидроизохонолин-моногидрата который о имеет т.пл. 230-233 С.
Вычислено, %: С 49,83: Н 5,28;
N 9,18; CL 7 74: S 7 00. (.i Н22С1NgО S Hg®
Найдено, %: С 49,58; Н 5,00
N 8,84; С1 /,50; S 6,81.
Пример 4. Работают аналогично примеру 1 с тем отличием, что реакцию осуществляют в 400 мл приготовленной в отношении 2:1 смеси иэ изопвопанола и воды. Получают 70,1 г (82%) 2- ((3 -сульфамил-4 -хлор-бензоил) — амино -1,2,3,4-тетрагидроизохинолина, который после переосаждения в основной среде имеет т. пл.
226-228 С.
Пример 5. В раствор 22,6 г
2-амино-1,2,3,4-тетрагидроизохинолина в 400 мл диоксана добавляют раствор 12,/ г безводного карбоната натрия в 200 мл воды. При охлаждении холодной водой и при перемешивании реакционную смесь смешивают по каплям с раствором 68 г 4-хлор-3-(И-(диметиламинометилен)-сульфамил)-бензоилхлорида в 400 мл диоксана, причем температуру поддерживают 15-20 С.
По окончании добавки смесь перемешио вают при 20 С еще 2 ч и затем фильтруют. Фильтрат разбавляют 2 л воды, осажденные кристаллы отсасывают, промывают водой и сушат при 80 С. Сырой продукт 63 г перемешивают в 430 мл
2 н. натрового щелока при 50 С в течение 8 ч. Раствор осветляют активным углем, фильтруют и устанавливают величину рН фильтрата при охлаждении и перемешивают с помощью 2 н. соляной кислоты до 6. Осажденный осадок отсасывают, промывают водой и сушат при 80 С. Получают 43,9 r (60 )
2- )i,3 -сульфамил-4 -хлорбензоил)1 I
-амино -1, 2, 3, 4-тетрагидроизохинолина, который имеет т. пл. 225-22/ С.
Способ получения производных
45 2-аминоизохинолина общей формулы
R Rg 5
О р N-кн- сО О с1
50 . R3 502ИН2 где R< и R2
3 и 4
55 отлича производное щей формулы
5 1b/
Пример 6. К суспензии 14,5 г е-хлор-3- f(N-диметиламинометилиден)-сульфамил|-бенэойной кислоты в
50 мл хлористого тионила добавляют две капли диметилформамида. Реакционную смесь кипятят прн перемешивании
2 ч, затем фильтруют, и фильтрат выпаривают в вакууме. В форме снежнобелых кристаллов получают 12,7 г (82X) 4-хлор-3- P(N-диметиламинометилен)-сульфамил1-беиэоилхлорида, который имеет т.пл. 140 t . После перео кристаллизации иэ бенэола т.пл. 154155 С.
Вычисленор Х: С 38,84; Н 3,26;
Н 9 06þ ;Cl 22р93; $ 10р37 °
C lo Н ho ClzNzO>S
Найдено, X: С 38,28; H 3,0/;
N 8,94;е Cl 23,14; S 10,58.
Пример /. К суспензии 8,2/ г
2-амино-1,2,3,4-тетрагидроизохинолина в 25 мл пиридина добавляют 17,25 r
4-хлор-3- f(N-диметиламинометилиден)-сульфамил)-бензоилхлорида. Реакционную смесь нагревают приблизительно о до 60-/О С, причем образуется желтый раствор, который оставляют на ночь.
На другой день раствор смешивают с
200 мл воды. Осаждается желтая смола, которая через несколько минут перемешивания разлагается до порошка песочного цвета. Продукт отсасывают, промывают водой и затем сушат. Сырой продукт подвергают гидролизу описанным в примере 5 способом, с 143 мл
2 н. натрового щелока. Получают
15,4 r (/5X) 2- ((3 -сульфамил-4-хлорбенеоил)-анино) -1,2, 3,4-тетрагидроизохинолина, который имеет т.пл.
225-22/ С.
Пример 8. Работают аналогично примеру 4, но превращение производят в 350 мл приготовленной в отношении 2:1 смеси иэ этанола и воды.
Исследование салуретического действия на крысах.
Для Screen — исследования применяют крыс мужского пола штамма
LATI СГУ со средним весом 240 г. Животные получают стандартный корм для крыс. 3а 16 ч до начала опыта кормление прекращают, однако не ограничивают прием жидкости. Для подтверждения мочегонного действия используют известный метод. Животных помещают в клетки для исследования обмена веществ. Мочу собирают от 0 до 6 и от
О до 24 ч. Контрольные животные по6444 лучают через желудочный зонд 25 мл/кг физиологического раствора хлористого натрия, Исследуемые соединения вв<)дят
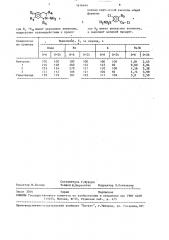
5 в таком же количестве физнологического раствора хлористого натрия и при дозе 5 мг/кг. Через 6 ч животные получают через желудочный зонд такое же количество физиологического раствора хлористого натрия, как количество выделенной в первые 6 ч мочи. Определяк)т вьщеленное за 0-6 и за 0-24 ч количество мочи, концентрацию Na и К в моче и отношение Na/К вьщеленной за соответствующий период мочи. Кроме обработанной физиологическим раствором хлористого натрия контрольной группы имеют также группу для сравнения, обработанную гипотиазидом, 20 Действие полученных соединений, назначенных при однократной дозе
5 мг/кг, на вьщеление воды, Na и К у крыс в периоды 0-6 и 0-24 ч в процентах по отношению к необработан2.) ным контрольным животным и íà Na/К— отношение продемонстрировано в таблице.
На основании проведенных на крысах исследований можно установить, 30 что соединения имеют отличную сапуретическую активность. Действие наступает через 1-2 ч после приема, достигает своего максимума между 3 и
5 ч и держится в течение 24 ч. В результате этого обеспечивается мягкий и длительный диуреэ. Особенно выгоди пчи являются благоприятное Na/К отношение и небольшая токсичность. Последняя при оральном назначении у мы4р шей составляет ЛД ) 3000 мг/кг.
Формула изобретения — водород или метоксигруппа;; — водород или группа метила;
" водород или хлор, ю шийся тем, что
2-аминоизохинолина об1676444 водным карболовой кислоты общей й, 4 2 где R имеет указа ное значение ° и выделяют целевой продукт. где R -Ry имеют указанное значение, 1 подвергают взаимодействию с произВыделение, Й, за период, ч
Соединение по примеру
Na/К
Вода
0-6 0-24
0-6 0-24, 0- 0-24
0-6 0-24
Составитель Г Жукова
Текред М.Моргентал Корректор Э.Лончакова е.
Редактор М.Бланар
Заказ 3016 Тираж Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям прн ГКНТ СССР.
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат "Патент", r.Óèrîðîä, ул. Гагарина, 101
Контроль
2
Гипотиазид
100 100
216 148
233 154
147 112
159 119 формулы
С1
Н2ИО2S СО-С1
Na б
100 100
260 152
279 151
186 121
187 123
100 100
145 82
170 100
104 84
117 109
1,81 2,45
9,09 5,94
7,56 5,38
4,74 3,99
3,9 3,50