Способ кристаллизации госсипола
Иллюстрации
Показать всеРеферат
Изобретение относится к ароматическим альдегидам, в частности к кристаллизации госсипола. Цель изобретения улучшение качества разделения. Кристаллизацию из бинарных органических растворителей , содержащих эфир, ведут растворением госсипола в эфире до концентрации 0,04-0,1 г/м с последующим добавлением гексана, нагретого до 30-32°С в количестве 0.5-2,8 от объема эфира. Затем проводят осаждение различных кристаллических форм госсипола в зависимости от температуры, выбранной в интервале 10- 27°С. Способ обеспечивает улучшение качества разделения образцов продукта, что позволяет использовать их как стандартные образцы для контроля качества выпускаемого фармакопейного гиссигюла. 2 табл 6 ил.
союз соВетских
СОЦИАЛИСТИ -ГЕСКИХ
РЕСПУБЛИК (м)5 С 07 С 47/57, 45/78
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
1 4
О (гд
0 (лЭ
ОО
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (21) 4144748/04 (22) 18.07.86 (46) 07.01.92, Бюл. М 1 (71) Институт биоорганической химии
АН УЗССР (72) Б.Т.Ибрагимов, С.А.Талипов, P.Ã,Màðданов и Т.Ф.Арипов (53) 547.44(088.8) (56) Авторское свидетельство СССР
М 212245, кл. С 07 С 91/28, 1965. (54) СПОСОБ КРИСТАЛЛИЗАЦИИ ГОССИПОЛА (57) Иаобрвтенив относится к ароматическим ельдегидам, в частности к кристалливвции госсипола. Цель изобретения—
Изобретение относится к получению госсипола путем его кристаллизации из растворителей.
Целью изобретения является улучшение качества разделения, в результате чего получают отдельные кристаллические образцы госсипола для контроля качества фармаколейного госсипола.
Поставленная цель достигается путем растворения госсипола в эфире до концентрации 0,04-0,1 мг/мл, со следующим добавлением в раствор гексана в количестве
0,5-2,8 от объема эфира, нагретого до 3032 С, и дальнейшим осаждением в диапазоне температур 10-27 С для различных кристаллических форм с последующим осуществлением контроля путем сравнения дифрактограмм.
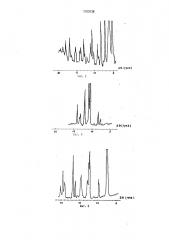
На фиг.1-5 приведены дифрактограммы контроля качества фармакопейного госсипола, который проводят обычным путем сравнения дифрактограммы образца с диф„„5U„„1703б38А1 улучшение качества разделения. Кристаллизацию из бинарных органических растворителей, содержащих эфир, ведут растворением госсипола в эфире до концентрации 0,04-0,1 г/м с последующим добавлением гвксана, нагретого до 30 — 32 С в количестве 0,5-2,8 от объема эфира. Затем проводят осаждение различных кристаллических форм госсипола в зависимости оТ температуры, выбранной в интервале 1027 С. Способ обеспечивает улучшение качества разделения образцов продукта, что позволяет испрльзовать их как стандартные образцы для контроля качества выпускаемого фармакопейного гиссиг ола. 2 табл.
6 ил. рактограммами пяти таким способом пол ученных индивидуальных кристаллических форм.
Пример 1. Госсипол в количестве 1 г отвечающий требованиям временной фармакопейной статьи ВФС-42-366-74 (ВФС), растворяют в 10 мл серного эфира, предварительно очищенного от перекиси, но не от влаги, и добавляют 20 мл гексана, нагретого до 30-32 С, оставляют в холодильнике или термостате при 10 — 12 С на 24 ч, Выпавший осадок отфильтровывают, сушат под вакуумом при 50-60 С в течение 5 ч, При этом выход продукта, имеющего кристаллическую форму t, составляет 820 мг (82%). Дифрактограмма этой формы приведена на фиг.1.
Госсипол в этой кристаллической модификации плавится из-за разложения в широком диапазоне температур (177-184 С), Результаты термогравиметрического анализа и ЯМР-исследования наряду с фактом
1703638
30
40 госсипола в этой кристаллической модифи- 45 кации III неустойчивы, при стоянии начина50
55 получения кристаллов госсипо а в этой форме из-за смесей эфир-ксилол и хлористый метилен-гексан свидетельствуют о несольватном характере этой кристаллической модификации госсипола. Продукт в этой полиморфной модификации является наиболее растворимым. Фармакопейный госсипол имеет именно эту кристаллическую форму.
Пример 2. Берут 1 г фармакопейного госсипола, растворяют в 25 мл эфира, очищенного как в примере 1, добавляют 65-70 мл нагретого до 30-32 Ñ гексана, оставляют при 26-27 С в термостате до образования достаточного количества монокристаллов пластинчатого габитуса, отделяют их фильтрацией, слегка сушат на воздухе, растирают в порошок и снимают дифрактограмму, которая приведена на фиг,2.
Госсипол, кристаллизующийся в этой полиморфной модификации И, плавится при
214 С. Согласно результатам рентгеноструктурного анализа монокристаллов госсипол этой модификации не содержит молекул растворителя в кристаллической решетке. Посредством иежмолекулярных водородных связей молекулы госсипола упакованы наиболее плотно по сравнению с другими кристаллическими формами. Кристаллические образцы формы И имеют наименьшую растворимость как в полярных, так и в слабополярных растворителях.
Пример 3. 1 г госсипола растворяют в 20 мл эфира, добавляют 10 мл гексана, имеющего температуру 30-32 С, оставляют до образования монокристаллов игольчатого габитуса, отделяют их фильтрацией, не производя сушки растирают в порошок и сразу же снимают дифрактограмму, которая представлена на фиг.3.
Согласно исследованиям структуры этих кристаллов методом рентгеноструктурного анализа, в их решетку входит эфир в соотношении госсипол: эфир 1:1. Кристаллы ют терять молекулы растворителя. Однако скорость десольватации сильно зависит от размеров кристаллов, практически доходя до нуля для достаточно крупных (0,02 х 0,1 х
0,4 MM ) монокристаллов.
Пример 4. Берут монокристаллы формы И(, тщательно растирают в порошок и сушат под вакуумом в течение 2-4 ч при постоянном перемешивании, контролируя исчезновение на дм фрактограмме пика формы III при угле 7,22 (фиг.4) . Необходимость контроля диктуется тем, что время, требуемое для завершения перехода формы (И в
20 форму IV, зависит от степени измельчения и совершенства кристаллов формы (II.
Данные рентгеноструктурных исследований монокристаллов этой формы свидетельствуют о том, что и эта кристаллическая модификация госсипола является кристаллосольватом, однако, с содержанием эфира в кристаллической решетке вдвое меньше.
Образец в этой кристаллической форме также является неустойчивым и медленно переходит в результате десольватации к очередной форме Ч, уже не содержащей эфир.
Пример 5. Берут образец, полученный в примере 4, или тщательно измельченные монокристаллы формы (И подвергают сушке под вакуумом при 80 — 100 С и постоянном перемешивании в течение 10-12 ч, снова контролируя с помощью дифрактограммы исчезновение характеристического пика формы (Ч при угле 7,78О. Полученный таким образом продукт не содержит растворителя.
Однако не всегда удается добиться осуществления полного фазового перехода, так как из-зв рваного качества (дефектности) кристаллов исходной формы Ш десольватация происходит при разных режимах температуры и времени. 8 таких случаях получают монокристаллы формы Ill более дефектными эа счет более интенсивного испарения растворителя, твк квк дальнейшее увеличение температуры сушки нежелательно в связи с тем, что при этом госсипол может частично окиеляться, Дифрактограмма формы Ч приведена на фиг.5.
П р и ц е р 6. Этот пример иллюстрирует контроль качества фармакопейного госсипола. Нв фиг.6 показана дифрактограмма одной из партий фармакопейного госсипола, Данный продукт представляет собой смесь форм НЧ. Наличие в образце форм Ш и IV свидетельствует î его относительно низкой чистоте. Поскольку максимальное содержание госсипола в кристаллической форме III составляет 88, а в форме IV—
947, чистота данного образца не отвечает требованиям ВФС. Измеренная температура плавления образца 179-183 С отвечает этим требованиям, хотя налицо неоднофазность продукта. Измерение коэффициента при тщательной сушке в связи с мелкодисперсностью и качеством микрокристалликов форм III u IV свидетельствует о соответствии значению, приведенному в
ВФС. Поэтому, на основе измерения значений этих параметров данную партию госсипола принимают за фармакопейную.
Зависимость фазового состава госсипола от параметров и условий кристаллизации
1703638 образцы для контроля качества выпускаемого фармакопейного госсипола.
Формула изобретения
Способ кристаллизации госсипола иэ
5 бинарных органических растворителей, содержащих эфир, отличающийся тем, что, с целью улучшения качества разделения, госсипол растворяют в эфире до концентрации 0,04--0,1 г/мл с последующим
10 добавлением гексанв, нагретого до 30-32ОС в количестве 0,5 2.8 от объема эфира и дальнейшим осаждением различных кристаллических форм госсипола в зависимости от температуры, выбранной в интервале 1015 27 С. представлены в табл,1; фармакологические свойства различных кристаллических форм — в табл,2.
Из данных этой таблицы видно, что по биологическому действию образцы госсипола не идентичны, Токсичность кристаллических модификаций меняется в очень широких пределах, причем изменение доходит до того, что форма ll оказывается нетоксичной.
Таким образом. предлагаемый способ кристаллизации госсипола дает воэможность улучшить качество разделения кристаллических образцов продукта, что позволяет их использовать как стандартные
Таблица 1
Концентра- Обьем гексация госсипо- нв ла а эфире, г/мл
Опыт
Температура осаждения, С
Кристаллическая форма
Температура гексвна. С
Таблица 2
ЛД о, мг/кг
КристалличесКВА о ма
Клиника отравления
640 (450-768) Малоподвижность, кратковременное возбуждение сменяется угнетением, судороги, боковое пбложение.
Гибель в течение суток
Угнетение, малоподвижность, которая проходит через 5 ч.
Малоподвижность, расслабление задних конечностей, умывание.
Гибель в течение 3 с
1500*
750 (646 — 870) + Если у препарата ЛД5о.1500 мг/кг, он считается нетоксичным, 1
3
5
7
9
0,10
0,04
0,05
0,03
0,11
0,08
0,08
0,10
0.08
0,10
0,08
2,0
2,5
0,5
2,5
1,0
3,5
0,2
2.0
1,5
2.5
1,5
30-32
30-32
30-32
30-32
30-32
30-32
30-32
20-22
30-32
20-22
34-35
10-12
26 27
20-22
25-26
22-23
25-26
10-12
5-6
30-32
10-12
25- 26, 1
III
1+И
I+II!+IV+V
I+ аморф.
1+ИН11г
l+ вморф.!
+И
I+ аморф.
НИ
45 гО
Фиг. 3 ао
1703638
1703638 гв траян со
Фиг. 5 гв (rpah) (о
Ъ
Фиг. 6
Составитель Т. Фомичева
Тенред M. Моргентал Корректор М. Максимишинец.
Редактор H. Гунько
Заказ 38 Тираж Подписное
ВНИИПИ Государственного комитета по иэобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб„4/5
Производственно-иэдательский комбинат "Патент", г, Ужгород, ул.Гагарина, 101