Способ определения токсичности отработанных вод после отбелки целлюлозы
Иллюстрации
Показать всеРеферат
Использование: оценка токсического действия продуктов, образовавшихся после отбелки целлюлозы, критерий для выбора схем отбелки целлюлозы. Сущность изобретения: токсичность определяют по результатам воздействия отработанных растворов на плазму крови, а именно по изменению общей протеолитической активности (ОПА) плазмы крови ОПА выражают в микромолях аргинина, отщепленного от протаминсульфата 1 л плазмы крови за 1 мин по формуле, 1 ил., 3 табл.
СОЮЗ СОВГТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК оп 5 G 01й 33/555, 33/18
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (21)4779070/13 (22) 05.01.90 (46) 23.08.92. Бюл. М 31 (71) Всесоюзное научно-производственное обьединение целлюлозно-бумажной промышленности (72) Г.М,Боголюбова, В.M.Âàñèëüåâ и
И.Г.Щербак (56) Лесников Л.А. Методика оценки влияния воды из природных водоемов на
Paphnta Manga S traus. — Методики биологических исследований по водной токсикологии. M. Наука, 1971, с. 157-166.
Изобретение относится к оценке суммарного токсического действия групп химических веществ, образующихся и переходящих в раствор при выделении природных полимеров, в том числе целлюлозы, полученной из различных видов растительного сырья с использованием в процессе ее отбелки различных реагентов: хлора; гидроокисей Са +, Mg, Na; кислорода; пероксида водорода, а также их соединений — диоксида хлора, гипохлоритов и соединений серы — сульфитов, бисульфитов.
Изобретение может быть использовано для оценки токсического действия продуктов, образовавшихся после отбелки целлюлозы с применением различных химических веществ, и служить одним иэ критерием для выбора имеющихся схем отбелки целлюлозы и создания новых, Цель изобретения. — повышение точности и ускорение способа проведения анали.!Ы 1/56824 А1 (54) СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ОТРАБОТАННЫХ ВОД ПОСЛЕ ОТБЕЛКИ ЦЕЛЛЮЛОЗЫ (57) Использование: оценка токсического действия продуктов, образовавшихся после отбелки целлюлозы, критерий для выбора схем отбелки целлюлозы, Сущность изобретения: токсичность определяют по результатам воздействия отработанных растворов на плазму крови, а ийбнно по изменению общей протеолитической активности (ОПА) плазмы крови ОПА выражают в микромолях аргинина, отщепленного от протаминсульфата 1 л плазмы крови за 1 мин по формуле, 1 ил„З табл. за, позволяющего определить токсичность исследуемых растворов.
Поставленная цель достигается тем; что в качестве биологического объекта используют плазму крови человека, определяют ее протеолитическую активность до и после инкубирования, а токсичность оценивают по изменению общей протеолитической активности (ОПА).
ОПА плазмы определяют до и после воздействия указанных растворов. Увеличение или снижение активности исследуемого показателя служит оценкой повреждающего действия. ОПА является суммарным показателем состояния важнейших протеолитических систем крови: фибринолитической, калликреин-кининовой, системы свертывания крови и системы комплемента. Активация или угн тение этих систем может стать причиной развития различных паталогических состояний. Систел.а протеолитических
1756824 ферментов является весьма чувствительной и быстро реагирует на различные воздействия.
Способ осуществляется следующим образом.
В процессе многоступенчатой отбелки целлюлозы отбирают пробы образовавшейся сточной воды (фильтрата). Затем проводят оценку токсичности этих вод, определял
ОПА плазмы до и после воздействия фильтратов. В качестве субстрата используют протаминсульфат (ПС). Схема опыта." к 0,1 мл плазмы крови добавляют 0,5 мл 0,05 M мединалового буфера (рН 7,6) и 0,2 мл 1%ного раствора ПС. Пробуинкубируют15мин при 37 С, после чего реакцию останавливают, добавляя ОЯ мл 20%-ного раствора трихлоруксусной кислоты (TXJ), Нерасщепившийся ПС осаждавши центрифугованием в течение 30 мин при 8000 об,/мин. В прозрачном центрифуга е определяют содержание аргинйна методом Сакагуши в модификации В.А.Храмова. Для этого к 1 мп центрифугата добавляют при-перемешивании по 1 мл энтеросептола, 7.,5% NaOH u
NsBrO; Интенсивность окрашенного растйора измеряют с помощью фотозлектраколориметра ФЭК-56 М со светофильтром М
5 в кювете 10 мм, сравнивая опытную пробу с контрольной, Контрсльйая проба отличается от опытной тем, что ПС добавляется в пробу-после ТХУ. Количество аргинина в пробе служит мерой протеолитической активности плазмы крови.
ОПА выражают в микромолях аргинина в пробе, что служит мерой протеолитической активности плазмы крови.
ОПА выражают в микромолях аргинина, отщепленного от протаминсульфата 1 л плазмы крови эа 1 мин, по формуле
1,6 1000
ОПА — -6,1 мкМ арг/л мин
0,1 15 174 2 где 1,6- объем инкубационной смеси;
1000 — пересчет на 1 л плазмы;
0,1 — количество плазмы в опыте;
15 — время инкубации;
174,2 — мол,масса аргинина, Если исходную величину ОПА принять эа 100, активности,то ОПА, полученная после 15-мййутной инкубации плазмы с отработанным раствором (величина Х) будет составлять Y% от исходной.
Пример расчета:
ОПА=22,2 мкМ арг/л мин — 100%
X=4,8 мкМ арг/л мин — Y%
4.8 100 21 6 о
22,2
100% — 21 6%78 4% угнетения.
Пример 1. Исследуют токсичность отработанных растворов после отбелки целлюлозы по схеме: хлорирование (Х) — щелочение (Щ) — обработка гипохлоритом в две
5 ступени (Г1-Г2), т.е. X-Щ-Г1-Г2.
Пробы фильтратов отбирают после ступеней хлорирования, щепочения, полной схемы отбелкЫи определяют токсичность по предлагаемому способу.
10 Влияние отработанных растворов после отбелки целлюлозы по схеме X-Ù-Г1-Г2 на общую протеолитическую активность плазмы крови человека представлено в табл.1.
15 Отклонение протеолитической активности плазмы крови (ОПА) в сторону ее уменьшения (угнетения) или увеличения (активации) от исходного (нормального) уровня является характеристикой токсично20 сти исследуемых растворов и может быть сопоставимой с характеристикой токсичности этих же растворов, полученной класси- ческим методом контроля по выживаемости определенных тест-организмов при раэлич25 ных разбавленных исходных отработанных растворов эа определенный период (3-10 сут).
Пример 2. Исследуют токсичность отработайных растворов после перекисной
30 делигнификации (Пд) и последующей добелки по схеме; диоксидом хлора в 2 ступени с промежуточной перекисной обработкой, полная схема Пд-Д1-П-Р2.
Пробы отработанных растворов отбира35 ют после перекисной делигнификации (Пд), отбелки двуокисью хлора (Д1) и после полной схемы отбелки, Определяют токсичность по предлагаемому и известному способам.
40 Влияние отработанных растворов после отбелки целлюлозы по схеме Пд-Д)-П Д2 на об цую протеолитическую активность плазмы крови представлено в табл. 2.
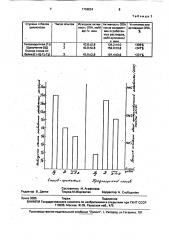
Расхождение данных наблюдается в ре45 эупьтатах определения токсичности отоаботанных растворов от делигнификации небеленой целлюлозы перекисью водорода только на начальной стадии схемы отбелки (см. чертеж). Расхождения вызваны тем, 50 чтьо на этой стадии в раствор переходит значительное количество органических веществ целлюлозного и пигнинного характера. Эти вещества большей частью являются опигосоединениями и представляют собой в
55 растворе коллоидную систему, которая "забивает" дыхательные органы дафний, что отмечается 9 качестве основной причины их гибели при определении токсичности по известному способу. В то же время сама по себе тсксичность отработанных растворов
i766824
Угнетение или активация ОПЛ, %
Активность ОПА после воздействия отработайных растворов, мкМ аргинина/ л мин
Число опытов
Исходная активность ОПА, мкМ арг/л. мин
Ступени отбелки целлюлозы.. -35%
+i 35%
52,4+.3,6
52,4+3,6
Хлорорование(Х)
Щелочение (Щ)
Полная схема отбелки X- -Г1-Г2
34,2 ;8 23,2 3,4 . +63 4
85,4 2,6
52 4н-3 6
Таблица 2
Активность
ОП А после воздействия отработанных растворов, мкМ аргинина/ л мин
Ступени отбелки:целл юлоэы
Число опытоь
Исходная активность ОПА, мкМ арг/л мин
Угнетение или активация
ОПА, %
Перекисная делигнификация (Пд) Отбелка двуокисью хлора (Д1) Полная схема отбелки (Д-П-Д) 63,7 4,8
89,8+4,0
„. 46,7+4,2
166, l 6,9
46 4,2
133,4+6,0
+195 от стадии Пд по-видимому невысокая, на что отработанных растворов после отбелки целуказывают результаты, полученные в при- люлозы является достаточно чувствительмере 2 при определении токсичности по . ным, так как в качестве исследуемой предлагаЕМОМу МетоДу. :: . вЕличины выбран суммарный пОказатель акПример-3, Исследуют токсичность 5 тивности многих фермЬнтных систем плазотработанных раствороs от отбелки целлю-: - мы крови. Активация или угнетение одной лозы по схеме: обработка гипохлоритом (Г1) из них отражается на величине общей про— щелочение (Щ) — обработка гипохлоритом теолитической активности (ОПА) плазмы в две ступени (Г1-.Гз), т,е. Г1-Щ-Г2-Гэ. крови.
Пробы фильтратов отбирают после пер- 10 При использовании преДлагаемого спо- вой ступейи мпохлоритной " обработки (Г1);:: соба оценка токсичности отработанных расщелочения и смесь фильтратов от полной творов от отбелки целлюлозы, получвйнйх с схемы отбелки (Г1-Щ-Г2-Гз), Определяют применением разлйчййотбелйвающих ре-: токсичность по предлагаемому способу. агентов, может быть проведена достаточно
Влияние отработанных растворов по- 15 быстро и по четким количественным критесле отбелки целлюлозы по схеме Г1-Щ-Г2-Гэ риям. на ойцую протеолитическую активность Ф о р м у л а и з о б р е т е н и я плазмы крови человека представлено в Способ определения токсичности оттабл,3, работаннь:х вод после отбелки целлюлозы
Представленные данные показывают, 20 путем инкубирования исследуемого матечто плазма крови, в частности ее протеоли- . риала с биологическим обьектом с последутическая актйвность, является чувствитель- ющей оценкой полученных *результатов, о тным объектом для выявления токсичности лича ю шийся тем, что, с целью повышеотработанных растворов от отбелки целлю- ния точности и ускорения способа, в качестлоэы. 25 ве биологического объекта используют, Предлагаемый метод, таким образом,: плазму крови человека, опредеЛяют ее про-: позволяет точнее, оценивать абсолютную теолитическую активность до и после инку- токсичность отработанных растворов. Ис- . бирования, а токсичность" оценивают по, пользование общей протеолитической ак- изменению общей протеолитическойактив- тивности для определения токсичности 30 ности.
Таблица 1
1256824
Таблица 3
Ь а
Ъ а-и-д
CnoroХ- яро о vn
Л сул г.р гм с саос 3
Составитель И. Агафонова
Техред М.Моргентал Корректор Н, СлободянЬк
Редактор В. Данко
Производственно-издательский комбинат "Патент", r. Ужгород, ул.Гагарина, 101
Заказ 3085 Тираж Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., 4/5