Способ получения с @ -углеводородов
Иллюстрации
Показать всеРеферат
Сущность изобретения: окислительную димеризацию метана на окисном катализаторе в присутствии кислорода проводят, подавая в импульсном режиме пероксид водорода в количестве 0,04-0,8 об.%. 2 табл.
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК
ОПИСАНИЕ ИЗОБРЕТЕН
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (21) 4854846/04 (22) 25.07.90 (46) 15.10.92. Бюл, № 38 (71) Институт химической физики АН
АрмССР (72) Л.А.Вартикян, В,Т.Минасян и Т.А,Гарибян (56) Otsuka К., Lin Q., Hatano M., Morikawa А., Chem. Lett., 1986, р. 467, Moriyama T., Takasaki N„Ewamatsu Е., Aika K„Chem. Lett., 1986, р, 467, Но T„Waning 1,-Х., Lin С.— Н., Lunsfond
I,H „J.Am. Chem. Soc., 1985, ¹ 107, р.5062.
Патент США № 4567307, кл. С 07 С 2/02, 1985.
Заявка Японии в- м е «. и . ь. Мт — —— о
Q0 (Л с с ) ГОСУДАРСТВЕННЫЙ КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР
Изобретение относится к области органической химии, в частности получения низших олефинов и может быть использовано в химической промышленности, Известен способ получения С2-углеводородов при окислительной димеризации метана на оксидных катализаторах, промотированных щелочными добавками. Наибольшая активность катализатора ZnO наблюдается при увеличении доли Li— - Na в катализаторе до 12,5 моль.%.
Для катализатора MgO оптимальный состав: 15 моль.% Na/MgO при 800 С и объемном соотношении СН4:воздух: Не
=1:2,5:33,3.
Во многих случаях используемые в процессе превращения метана катализаторы дезактивируются по мере прохождения процесса, Одной из основных причин является отложение на поверхности катализатора продуктов уплотнения. Так, для Li/MgO найдено, что в течение 16 часов реакции при
7000С конверсия метана уменьшается от.Я2 1768569А1 (я)5 С 07 С 2/84, 9/06, 11/04 (54) СПОСОБ ПОЛУЧЕНИЯ С2-УГЛЕВОДОРОДОВ (57) Сущность изобретения: окислительную димеризацию метана на окисном катализаторе в присутствии кислорода проводят, подавая в импульсном режиме пероксид водорода в количестве 0,04 — 0,8 об,%. 2 табл.
27 до 20 $, площадь поверхности от 8,9 до
2м /r, Для регенерации исходного катализатора его обрабатывают кислородсодержащим газом при высокой температуре — 1200 С в течение нескольких часов.
Известен способ получения Сг-углеводородов контактированием СН4 при 750800 С с катализатором в присутствии Oz. В качестве катализатора использовались оксиды или карбонаты щелочных металлов (Li, Na, К) ил и щелочно-земель н ых металлов (Mg, Са, Ва), либо соединения этих металлов, нанесенные на MgO, ZnO, AtzOs.
Лучшие результаты получены на каталитической системе Ме20/MgO (Ме = Li, К, Na) и Ме О/MgO (Me = Sr, Ва). Содержание активного компонента 0,2 — 15%. Максимальный выход не превышает 20 об.%.
Необходимость восстановления активности катализатора снижает производительность процесса и ведет к его усложнению, так как подразумевает допол1768569 выход Cz-углеводородсв со временем падает, что, как было установлено, связано с 35 нительную стадию регенерации при высоких температурах, Целью изобретения является упрощение процесса и повышение его производительности путем активации используемого катализатора, Поставленная цель достигается тем, что процесс окислительной димерий)ции метана протекает при атмосферном давлении s температу 1Ьом интервале 740 — 800 С в присутствии парЪгв пероксида водорода, подаваемого в импульсном режиме E количестве (0,04-0,8) об,%, Импульсный режим подачи Hz02 подразумевает попеременное введение в реактор смеси СН +О и смеси, обогащенной парами HzOz Т.е. через Определенный промежуток времени подачи реакционной смеси в реактор (несколько минут) из смеси реагентов исключалась HzOz (смесь реагентов поступает в реактор, минуя ампулу с HzOz), Затем ре>ким подачи (импульс) возобновлялся и повторялся с заданной периодичностью в течение всего опыта.
Прсдол>кительность импульса зависит от условий проведения эксперимента — скорости струи, длины коммуникаций (путь от ловушки до реактора). Чем выше скорость струи и короче коммуникации, тем короче продолжительность импульса, При постоянной подаче паров Н О (не импjnüñíûé режим) суммарный высокий влиянием воды, как продукта распада НгО .
Показано, что ниже 0,04 об,% эффект активации катализатора почти не ощутим, Подача паров HzOz больше 0,8% объем. нежелательна, так как растут и количества продуктов распада Н О, что сказывается на выходе Cz-углеводородов и как следствие — производительности процесса.
Выбранный состав смеси СНг+02 определяется тем, что как предварительно установлено, в обозначенном интервале температур увеличение доли О приводит к росту выхода продуктов глубокого окисления — CO, COz, HzO и снижению селективности процесса.
Проведение процесса при температуре выше 800 С приводит к снижению селективности по С>-углеводородам, за счет роста выхода побочных продуктов, Проведение процесса при температурах ниже 740 С не обеспечивает существенного выхода С>-углеводородов.
Пример, В обогреваемый реактор и >сточного типа помещают слой катализа3" з тора (диаметр гранул 1 — 2 мм, объем 0,5 см ), 5
4 (50
55 расположенный над насадкой, в виде кварцевого боя.
Катализатор — 10% NazO/MgO готовят пропиткой порошка Mg0 раствором МаМОз, концентрацию которого подбирают так, чтобы вес Ма О составлял 10% от общего веса навески. Далее катализатор подвергают термообработке при 750 С в токе кислорода, таблетируют и измельчают на куски нужных размеров.
Смесь реагентов (CH4+Oz). перемешанную при комнатной температуре в соотношении 9;1, пропускают через ампулу с раствором Н Ог. Обогащаясь парами НгОг (ампула с HzOz находится при комнатной температуре, концентрация Н202 — 0,15 об,%) смесь поступает в реактор, Через определенный промежуток времени (несколько минут) ампула с HzOz изолируется и в реактор подается смесь СН4+02 (несколько минут), Затем периодичность повторяется.
Для !,êopoñòè струи 6 см /мин период (импульс, подразумевал 2 минуты ввода паров HOz + (CH4+Oz) и 3 мин ввода чистой смеси СH4+Oz, Температура реактора 740 С. Анализ продуктов осуществлялся методом газовой хроматографии. В ыход С2-углеводородов (СрНв+С Н ) — 1,22 об,%.
Пример 2. В условиях примера 1 процесс проводят при t = 800 С. Выход Сгуглеводородов 1,4 об,; .
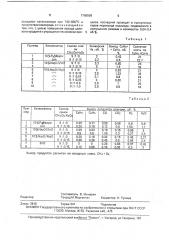
В табл,1 приведены результаты опытов при t = 740 С как без, так и при наличии в реакционной смеси паров Н20>,концентрация которого варьировалась в пределах
0,04-0,8 об, % для катализаторов 10%,.
PbO/àýðoñèë, 10% На О/ZnO, 10%. йа;О/MgO, используемых в процессе окислительной димеризации метана.
Катализатор10% РЬО/аэросил готовился поопиткой порошка аэросил-200 раствором РЬ(МОз)2, катализатор 10% Na20/ZnO— пропиткой порошка ZnO раствором КагСОз по описанной методике, В табл,2 приведен полный состав продуктов для всех рассмотренных катализаторов, Выход продуктов рассчитан на исход- . ую смесь CH4+Oz.
Таким образом, заявляемое техническое решение по сравнению с прототипом обеспечивает упрощение процесса и повышение его производительности за счет активации катализатора, что выражается в росте суммарного выхода Cz-углеводородов и селективности процесса, Формула изобретения
Способ получения С -углеводородов путем окислительной димеризации метана на
1768569
Таблица 1
Таблица 2
Выход продуктов расчитан на исходную смесь CH4+02.
Составитель В, Минасян
Техред М.Моргентэл Корректор Н. Тупица
Редактор
Заказ 3618 Тираж 341 Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., 4/5
Производственно-издательский комбинат "Патент", г, Ужгород, ул.Гагарина, 101 оксидном катализаторе при 740 †800 в присутствии кислорода, отличающийся тем, что, с целью повышения выхода целевого продукта и упрощения технологии процесса, последний проводят в присутствии паров пероксида водорода, подаваемого в импульсном режиме в количестве 0,04-0,4
5 об. О .