Вакцина для профилактики респираторных заболеваний крупного рогатого скота
Иллюстрации
Показать всеРеферат
Использование: биотехнология, ветеринарная вирусология, Сущность изобретения: вакцина включает антиген вируса инфекционного ринотрахеита из штамма ТК-А(ВИЭВ) В-2, антиген вируса диарреиболезни слизистых из штамма ВК-1(В-1) Ns 28, хламидийный антиген из штамма К 8, формалин, минеральное масло, безводный ланолин и забуференный физиологический раствор при определенном соотношении компонентов.
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК
ГОСУДАРСТВЕННОЕ ПАТЕНТНОЕ
ВЕДОМСТВО СССР (ГОСПАТЕНТ СССР) ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
1 (21) 4804352/13 (22) 09.02.90 (46) 23,01;93. Бюл. № 3 (71) Всесоюзный научно-исследовательский институт экспериментальной ветеринарии им.,Я.P. Коваленко (72) К.П. Юров, Ю.Д. Караваев, З.Ф. Зудилина, А.С. Вечеркин, Н,И. Налетов, С.А. Жидков, О.И. Сухарев, И,А, Третьякова и В.А.
Зудил ин (56) Авторское свидетельство СССР № 980307, кл. А 61 К 39/12, 1981.
Авторское свидетельство СССР
¹ 1322673, кл. С 12 N 7/00. 1987.
Изобретение относится к ветеринарной вирусологии и бактериологии, в частности к получению вакцин для специфической профилактики респираторных болезней крупного рогатого скота. а также для профилактики нарушений репродуктивной функции коров, обусловленных вирусами инфекционного ринотрахеита, вирусной диареи-болезни слизистых и хламидиями.
Эти три инфекции довольно широко распространены среди животных нашей страны и во многих других странах мира, наносят значительный экономический ущерб, складывающийся из-за недополучения приплода, низких привесов, отхода молодняка за счет гибели или выбраковки животных, низкой оплодотворяемости коров.
Цель изобретения — расширение спектра действия вакцины.
„„5U„„1789219 А1 (я)5 А 61 К 39/118, 39/12 (54) ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ РЕСПИРАТОРНЫХ БОЛЕЗНЕЙ КРУПНОГО
РОГАТОГО СКОТА (57) Использование: биотехнология, ветеринарная вирусология, Сущность изобретения: вакцина включает антиген вируса инфекционного ринотрахеита из штамма
ТК-А(ВИЭВ) В-2, антиген вируса диарреиболезни слизистых иэ штамма ВК-1(В-1) №
28, хламидийный антиген из штамма К 8, формалин, минеральное масло, безводный ланолин и эабуференный физиологический раствор при определенном соотношении компонентов.
Поставленная цель достигнута тем, что вакцина дополнительно содержит антиген вируса инфекционного ринотрахеита из штамма Herpesvirus bbvlnus 1 ТК-А (ВИЭВ)
В-2 с активностью 10 — 10 ТЦД5о/мл
5,5 7.5
0,5;ь-ом растворе гидролизата лактальбумина на растворе Хенкса и антиген вируса диареи-болезни слизистых из штамма
Кdlarroe-.,mucosal disease bovlnum ВК-1 (В-1) ¹ 28 с активностью 10 — 10
ТЦД5о/мл в 0,5, -ом растворе гидролизата лактальбумина на растворе Хенкса и забуференный физиологический раствор, Предложенную вакцину готовят следующим образом, Производственный вакцинный штамм вируса инфекционного ринотрахеита
Herpesvirus bovinus 1 ТК-А (ВИЭВ) В-2 размножают в первично трипсинизированных культурах клеток почки теленка (ПТ), или тестикулов бычков (ТБ), или их субкультурах, 1789219 можно использовать neðåâèâàåìûå клеточные линии МДВК, ЛЭК, TP. Заражение культур проводят вируссодержащей культуральной жидкостью в дозе 1 — 5 ТЦД/клетка. Зараженные культуры при стационарном или роллер- 5 ном культивировании инкубируют при
37-37,5 С в течение 24 — 72 ч, затем вируссодержащую культуральную жидкость собирают s количестве не менее 1600 — 1700 мл для изготовления 1 л вакцины, инактивируют "0 формалином в конечной концентрации
0,2 — 0,3 O в течение 46 — 48 ч при 37 — 37,5 С при периодическом перемешивании. Далее в вируссодержащую культуральную жидкость с формалином добавляют ПЭГ 60,00 15 из расчета 8 — 9 / и NBCI 2,5 — 2,8 ; Все тщательно перемешивают до полного растворения ПЭГ, оставляют при 4-8 С в течение
18 — 24 ч, далее подвергают центрифугированию при 8 — 10 тыс.об./мин, Осадок ресуспен- 20 дируют в забуференном физиологическом растворе с 0,18 — 0,2 формалина в соотношении 1;10-1:12.
Производственный штамм вируса диареи-болезни слизистых V.diàããáå-mucosai 25
disease bovinurh КВ-1 (В-1) М 28 размножают в первично трипсинизировэнной культуре клеток ПТ или ее субкультуре. Заражение проводят вируссодержащей культуральной жидкостью в дозе 5 — 10 ТЦД/клеток. Зара- 30 женные культуры при стационарном или роллерном культивировании инкубируют при 37,0 — 37,5 С в течение 72 — 120 ч. Вируссодержащую культуральную жидкость собирают в количестве не менее 1600 — 1700 мл 35 для изготовления 1 л вакцины, Далее в отношении инактивации и концентрирования антигена вируса ВД-БС поступают также, как с антигеном вируса ИРТ.
Производственный, вакцинный штамм 40
ChlamIdia abortus ov(s К-8 ВИЭВ размножают в развивающихся куриных эмбрионах 57-дневного возраста. Заражение проводят суспензией хламидий с инфекционной активностьюю 102 5-10 ЭЛД5о, 14л в дозе 0,2 мл 45 в желточный мешок, Зараженные куриные эмбрионы инкубируют при 36,0-37 С в течение 5-9 дней, после этого содержимое эмбрионов, кроме погибших зародышей, собирают не менее чем из 400 шт на 1 л 50 вакцины, добавляют эабуференный физиологический раствор рН 7,2-7,4 в соотношении 1:1 и размельчают в гомогениэаторе при
2500-3000 об./мин в течение 10- t5 мин.
Затем смесь подвергают центрифугировэ- 55 нию при 4-5 С на центрифуге марки ОТР101К при пропускной способности сопла (диаметр сопла 3 миллиметра) не более 120 л в час и давления не более 0,05 — 0,15 атм. Надосадочную жидкость собирают, осадок снимают со стенок ротора и уничтожают. Надосадочную жидкость вторично центрифугируют на центрифуге этой же марки, но при пропускной способности еопла (диаметр сопла 2 мм) не более 90 л в час и давлении не более 0,05-0,15 атм, Центрифугат удаляют, осадок хлэмидий снимают со стенок ротора центрифуги металлической лопаткой и ресуспендируют в забуференном физиологическом растворе в соотношении 1:(12-15), В суспензию хлэмидий добавляют формалин до конечной концентрации 0 38-0,42 и выдерживают в течение 96 ч при 36 — 37 С, периодически встряхивая 2 — 3 раза в сутки.
Концентрированные антигены вирусов
ИРТ, ВД-БС и хламидий берут а соотношении 1;1:1, помещают в одну емкость (реактор). Содержимое тщательно йеремешивают и охлаждают до 10 — 15 С. К смеси добавляют стерильный масляный адъювант, состоящий из 80-837ь минерального масла и 17 — 20 ланолина, предварительно охлажденный до
10-15 С. На одну часть смеси антигенов добавляют одну часть масляного адъюванта.
Смесь антигенов с масляным адъювэнтом эмульгируют, пропуская через коллоидную мельницу при зазоре 00 между трущимися поверхностями и давлением
0,4-0,6 кг/см до получения гомогенной массы, которую используют в качестве готовой вакцины.
Концентрирование антигенов указанными методами достигается в 80-100 раз.
Контроль инактивации всех антигенов проводят путем слепых пассажей (3 пассажа) в соответствующих тест-системах, разводя предварительно антигены 1:100. Если в 3-м пассаже отсутствует ЦПД или нет гибели эмбрионов, значит материал инактивирован полностю.
Конкретные примеры осуществления способа изготовления предложенной вакцины представлены в табл. 1.
Вакцина, изготовленная таким образом, обеспечивает создание иммунитета у
95 — 977 животных, Конкретные примеры на способ профилактики даны в табл. 2.
Предложенная вакцина апробирована в экспериментальных и производственных условиях в 1986-1989 гг.
Предложенная впервые поливалентнэя инактивированная вакцина обеспечивает напряженный иммунитет против трех инфекций: инфекционного ринотрахеита, вирусной диареи-болезни слизистых и хламидиоэа крупного рогатого скота. Вакцина безвредна, применение ее по сравнению с моновакцинами снижает в несколько раз число вакцинаций и связанных с ними
1789219 стрессовых явлений у животных, Путем вакцинации стельных коров достигается создание напряженного иммунитета у матерей и передача его через молозиво телятам. Применение вакцины сокращает расходы на 5 транспортировку и ее хранение.
10 лактальбумина на растворе Хенкса и эабуференный физиологический раствор при следующем соотношении компонентов, мл: антиген вируса инфекционного ринотрахеита из штамма Herpes virus bovlnus
15 1ТК-А (ВИЭВ) В-2 с активностью 10"—
5.5
10 ТЦД50/ыл 15,7 — 16,6; антиген вируса диарреи-болезни слизистых из штамма V.dlarrhoe-mucosa!
disease bovinum ВК-1 (В-1) N 28 с актив20 кОСтьЮ 10 — 10 ТЦД5О/14/I 15,7 — 16,6; антиген хламидий из штамма
Chlamidia abortus bovls К-8 ВИЭВ с активностью 10 — 10 ЭЛД5о/мл 15,7 — 1.6,6 формалин 1,9-1,17
25 минеральное масло 400- 440 безоводный Дано/}ин 90-100 эабуференный физиологический раствор до 1 л.
Таблица 1
Примеры изготовление предлагаемой вакцины
Антиген
П lgcc изготовление ввк мны flo ста гмм
Кул ьти вмрование в культуре клеток (к.к.} курннык эмбрионак1к.a.) Инвктиввцил вируснык внтигенов в конечной концентрации (об. »,Т.вре. мв) формалином
Активность
ТЦД эо/ня в
N,к.
ЭЛД звлм к.э.
Способ концентрирование антигонов
Ресуспечдированне в соотно шенин
Смешиваниее внтнгенов длл соста влепилл 1л вакцины
Инвктивацил кпамиднй фо рмвл.об.», Т. времл
Контроль пол уфабрикэтв па показателлм
Добавление масленого адъюввнтв на! л вакцины, Пример 1
0.2»,3737.5 С,46ч
ПЭГ 6000 8»
Э1аО 2.5», центрмф.В-! 0 тыс. об./мин
40 мин
Двукступенч атос цеирмфугироваиие со сменой диаметра сопла при IS тыс.об./мин
1:10
Полнота инактивации. Стерильность. безвредность. Антигенность.
157 мл
1Овв
Вирус ИРТ
Вирус ВД-6С
Хламидии к.к. ПТ
530мл
53»
1Озл ккс 11Т к.э.56 ди
1:10
157 мл
0.38».
36-37пС.
96 v
1:12
156 мл
47»
Пример 2
0.25».3737.5 С. 47 ч
Вирус ИРТ
ПЭГ 6000 8.5»
МвО 2,6». цеитрф.8-1О тыс. об./мин. 50 янгн
Аналогично примеру 1
163 мл
510 мл
51»
106 о
107 5
Вирус ВД-6С
Хлвтгидни к.к. IIT к.s.5-6 дн
1:11
1лд
163 мл
164 мл
49»
0.4»,363ТС.96ч
Вирус IfÐТ
Прммер 3
О.З».3737.5 С.48ч
10тв
c.c.МДВК.
ЛЭК.TP к.к. ПТ
ПЭГ 6000 9» г}аС! 2.7». центр.
60 мин
Аналогмчно примеру 1
012
167 мл ,165 мл
500 мл
50»
Вирус ВД.ВС
Хлагмцааи
10ь.v
107.8 к.э.5.6 дн
1:15
0.39
36-3 С, 96ч
168 мл
50»
Формула изобретения
Вакцина для профилактики респираторных заболеваний крупного рогатого скота, включающая антиген хламидий из штамма Chlamldla abortus bovls К-8 ВИЭВ с активностью 10 — 10 ЭЛД5о/мл, форма6.5 7,5 л и н, беэ водны и л а нол и н и минеральное масло, о тл и ч а ю ща я с я тем, что, с целью расширения спектра действия, вакцина дополнительно содержит антиген вируса инфекционного ринотрахеита иэ штамма
Herpes virus Ьоч!пив 1 ТК-А (ВИЭВ) В-2 с активностью 105 — 10 ТЦД5о/мл в 0,5 (ном растворе гидролизата лактальбумина на растворе Хенкса и антиген вируса диарреи — болезни слизистых из штамма
V.dlarrhoe mucosai disease bovinum ВК-1 (В-1) М 28 с активностью 10 — 10
ТЦД5О/мл В 0,5 -НОМ раСтВОрЕ ГИдрОЛИэата
Вакцина найдет применение в крупных животноводческих комплексах и фермерских хозяйствах страны, что будет способствовать повышению продуктивности поголовья и увеличению продукции отрасли.
1789219
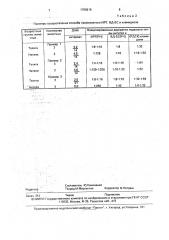
Таблица 2
Ф вЂ” Примеры осуществления способа профилактики ИРТ, ВД-БС и хламидиоза
Составитель Ю.Кононенко
Техред M,Ìîðråíòàë Корректор 8.Петраш
Редактор
Производственно-издательский комбинат "Патент", г, Ужгород, ул.Гагарина, 101
Заказ 312 Тираж Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., 4/5