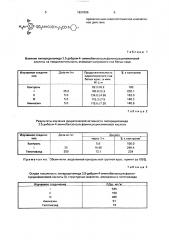
Пиперидиламид 3,5-дибром-4- аминобензолсульфонилсукцинаминовой кислоты, проявляющий нейролептическое и мочегонное действие
Иллюстрации
Показать всеРеферат
Использование изобретения: в качестве нейролептического и мочегонного вещества в медицине. Сущность изобретения: пиперидиламидЗ,5-дибром-4-аминобензолсульфонилсунцинаминовой кислоты формулы ЗЬВге- 4-NH2 C6H2-S02NHCO(CH2)2COU(CH2)4CH2. Выход 85%. БФ С15НюВг2№04, Т.пл. 192- 194°С, ЛДю 545 мг/кг. Реагент 1: М-(3,5-дибром-4-аминобензолсульфо)пирролидиндион-2,5. Реагент 2: пиперидин Условия реакции: в среде изопропилового спирта при молярном соотношении реагента 1 и реагента 2, равном 1:1,5. 3 табл. Ё
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК
ГОСУДАРСТВЕННОЕ ПАТЕНТНОЕ
ВЕДОМСТВО СССР (ГОСПАТЕНТ СССР) ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (21) 4943858/04 (22) 28.02.91 (46) 30.06.93. Бюл. N. 24 (71) Харьковский фармацевтический институт (72) В,Ф. Конев, В.А. Шаповалова. И.П, Банный, И,В. Скворцова, Л.А. Полуляхова, А.П.
Радько и О.Н. Коваль (56) Авторское свидетельство СССР
М 1178060, кл. С 07 С 143/78, 1984.
Авторское свидетельство СССР
М 1254690, кл. С 07 С 143/78, 1984.
Машковский M,Ä. Лекарственные средства: Пособие по фармакотерапии для врачей. В 24, Ч,I — Мн: Беларусь. 1988. — с.
484-490: С,35-60, Чвкман И.С. Осложнения фармакотерапии, Киев: Здоров я, 1980. с. 111 — 112; с, 35 — 38.
Западнюк В.Г., Гарбарец M,О. Фармак логия с рецептурой, 4-е изд., перераб. и доп.—
К,: Выща шк. (на укр, языке), 1989. -359 с.
Гацура B.Â. Метод первичного фармакологического исследования биологически активных веществ, — M.: Медицина, 1974, с, 21 — 26.
Изобретение относится к области синтеза биологически активных химических соединений, конкретно — к новому пиперидиламиду
3,5-дибром-4-аминобензолсульфонилсукцинаминовой кислоты формулы (1):
Br н,й 0 $0,йнсО(сн,,с0-м (и
Br,, Ы2„„1824396 А1 (я)ю С 07 D 211/06, С 07 С 311/51;
А 61 К 31/635 (54) ПИПЕРИДИЛАМИД 3,5-ДИБРОМ-4АМИНОБЕНЗОЛСУЛЬФОНИЛСУКЦИНАМИНОВОЙ КИСЛОТЫ. ПРОЯВЛЯЮЩИЙ
НЕЙРОЛЕПТИЧЕСКОЕ И МОЧЕГОННОЕ
ДЕЙСТВИЕ (57) Использование изобретения: в качестве " нейролептического и мочегонного вещества в медицине. Сущность изобретения; пиперидиламид 3,5-дибром-4- аминобензолсульфонилсунцинаминовой кислоты форм лы 3 rz4-NHz С Н2-SOz NH CO(CHz)z CON(C Hz)n Íz.
Выход 85 БФ C15H>pBrzNgOî, Т.пл. 192—
194 С, ЛД о 545 мг/кг, Реагент 1: N-(3,5-дибром-4-аминобензолсульфо)пирролидиндион-2,5. Реагент 2: пиперидин Условия реакции: в среде иэопропилового спирта при молярном соотношении реагента 1 и реагента 2, равном 1:1,5. 3 табл. который проявляет нейролептическую и диуретическую активность, Указанные свойства позволяют предполагать возможность применения его в качестве нейролептичеСкого средства с диуретическим эффектом.
Целью изобретения является создание более эффективного и менее токсичного по сравнению с приведенным аналогом препарата, обладающего комплексным фармакологическим эффектом: нейролептической и диуретической активностью. Поставленная
1824396 цель достигается новым соединением формулы (1).
Соединение формулы (1) получают в результате взаимодействия Щ3,5-дибром-4аминобенэолсульфо)пирролидиндиона-2,5 (11/) и пиперидина M в соотношении 1.1,5 в среде изопропилового спирта по схеме:
,и-.!г-ьп,н (ф
Bt o (1Ч) H (Ч)
Выход целевого продукта составляет 85 )(, Это бесцветное кристаллическое вещество, растворимое в спирте при нагревании и в других органических растворителях.
Строение соединения (!) подтверждено данными элементного анализа и ИК-спект- 20 ров.
Il р-и м е р. Пиперидиламид 3,5-дибром4- аминобенэолсульфонилсукцинаминовой кислоты (I), К взвеси 3,71 г (0,04 моль) N-(3,5дибром-4- аминобенэолсульфо)-пирроли- 25 диндиона-2,5 в изопропиловом спирте прибавляют 1 мл (0,015 моль) пиперидина, Нагревают до полного растворения осадка при постоянном помешивании. Оставляют на 24 часа. Затем разбавляют водой в соот- 30 ношении 1:3 и подкисляют хлороводородной кислотой до рН 1,0, Выпавший осадок отфильтровывают, сушат. Выход 3,49 г (857(). Кристаллиэуют из этанола. Иглы с т.пл, 192 — 4 С. Брутто-формула: С! НюВгйз04$, М.м. 496,8, Найдено, : С 36,27; Н 3,78; N 8,44;
$6,40.
Вычислено, og: С 36,23; 1-1 3,82; N 8,45;
$6,44. 40
ИК-спектры, (см ): 3085 (V N — Н); 2940—
2875 (v СН z); 1730-1615 (г с-О); 13351145 (м зо2); 680 (С вЂ” Br!.
Нейролептическую активность заявляемого соединения (1) исследовали на крысах 45 обоего пола пинии Вистар массой 150-190 г, Подопытных животных делили на 5 групп (по 7 крыс в каждой). Крысам I-й группы внутрибрюшинно вводили этаминал-натрий в дозе 30 мг/кг (контроль). Продолжитель- 50 ность наркотического сна этой группы крыс принимали за 100 .
Изучаемое соединение (i) аминазин и соединения (11) и (111) вводили внутрибрюLUItIHHo. Экспериментально было установле- 55 но, что эффективная доза для соединения (I) составляет 25 мг/кг Увеличение или уменьшение дозы приводит к понижению активности.
Эталоном сравнения служил аминазин, который вводили животным 5 группы в дозе 5 мг/кг, а спустя 30 мин этаминал-натрий в дозе 30 мг/кг.
О продолжительности действия этаминал-натриевого сна судили по времени, в течение которого животное находилось о боковом положении, т.е. с момента утраты рефлекса переворачивания.
Результаты изучения нейролептической активности представлены в табл.1. Из данных табл.1 видно, что заявляемое соединение (1) превосходит по нейролептической активности аминазин на 91,5, а структурные аналоги (11) и (Ill) на 69,1 и на 91,8 (, соответственно.
Изучение диуретической активности проводили на белых крысах-самцах линии Вистар, массой 140 — 180 г по методу
Е.Б, Берхина.
Контролем определения диуретической активности служили интактные белые крысы-самцы, которым вводили водную нагрузку в обьеме 5 массы тела, Количество выделившейся мочи данной группы животных принимали за 1007. Опытным группам вводили водную нагрузку в том же объеме вместе с заявляемым веществом. Полученные данные представлены в табл.2. Как видно из табл.2. соединение (I) по диуретической активности превосходит гипотиэзид на 647.
Следует отметить, что структурные аналоги диуретической активностью не обладают. Острую токсичность заявляемого соединения определяли на интактных серых мышах обоего пола массой 18-24 г, Все соединения (l,ll,Ill), аминазин и гипотиэзид вводили внутрибрюшинно. Результаты полученных данных обрабатывали по методу Керберэ. ЛДщ соединений указаны в табл.3.
Острая токсичность нового соединения (1) меньше, чем у аминазина и гипотиазида в
10,68 и 7,36 раэ соответственно, Заявляемое соединение (!) менее токсично своих структурных аналогов (II) и (III) в 3,63 и 1,17 раз соответственно.
Таким образом,эаявляемоесоединение(1) по фармакологической активности и бвзвредности значительно превосходит применяющиеся препараты аминазин и гипотиазид, э также соединения сравнения (II) и(П1), и может быть рекомендовано дпя создания высокоэффективного нейролептического препэрэта с диуретическим эффектом.
Формула изобретения
Пиперидиламид 3,5-дибром-4-аминобензолсульфонилсукцинаминовой кислоты формулы
1824396
Sr
HzN 0 SO>NHCO(CH2 2CO-N
Br проявляющий нейролептическое и мочегонное действие, Таблица 1
Влияние пиперидиламида 3,5-дибром-4- аминобензолсульфонилсукцинаминовой кислоты на продолжительность этаминал-натриевого сна белых крыс
Таблица 2
Результаты изучения диуретической активности пиперидиламида
3,5-дибром-4-аминобензолсульфонилсукцинаминовой кислоты
Острая токсичность пиперидиламида 3,5-дибром-4-аминобензолсульфонилсукцинаминовой кислоты (1), структурных аналогов, аминазина и гипотиаэида
Il р и м е ч а н и е: Объем мочи, выделенной контрольной группой крыс, принят эа 100-",ь.
Таблица 3