Тритерпеновые композиции и способы их применения
Иллюстрации
Показать всеИзобретение представляет собой новые сапониновые смеси для ингибирования инициации и активации эпителиальной клетки млекопитающего в предзлокачественном или злокачественном состоянии, стимулирования апоптоза злокачественной клетки млекопитающего, предотвращения аномальной пролиферации эпителиальной клетки млекопитающего, лечения воспаления и регуляции ангиогенеза у млекопитающего, которые выделены из растений вида Acacia victoriae, и способы их применения. Эти соединения могут включать тритерпеновую составляющую, такую как акациевая или олеаноловая кислоты, к которой присоединены олигосахариды и монотерпеноидные составляющие. Технический результат: смеси и соединения обладают свойствами, связанными с регуляцией апоптоза и цитотоксичности клеток, и обладают сильным противоопухолевым действием по отношению к различным опухолевым клеткам. 17 н. и 26 з.п. ф-лы, 53 табл., 50 ил.
Реферат
Предпосылки изобретения
Область техники, к которой относится изобретение
Настоящее изобретение по сути относится к области медицины. Более конкретно настоящее изобретение касается способов получения новых растительных соединений, имеющих терапевтическое применение к млекопитающим.
Состояние проблемы
Растения являются ценным источником для идентификации новых биологически активных молекул. Одним из разнообразных классов молекул, которые были идентифицированы у растений, является класс сапонинов. Сапонины представляют собой высокомолекулярные соединения, являющиеся гликозидами, у которых сахарная составляющая присоединена к тритерпеновому или стероидному агликону. В частности, тритерпеновые сапонины являются объектами более высокого интереса благодаря их биологическим свойствам.
Были исследованы фармакологические и биологические свойства тритерпеновых сапонинов, вырабатываемых различными видами растений, включая фунгицидную, противовирусную, антимутагенную, спермицидную или контрацептивную, сердечно-сосудистую и противовоспалительную активности (Hostettmann et al., 1995). Как известно, в процессе связывания с липидами крови сапонины образуют комплексы с холестерином, тем самым, изменяя динамику его метаболизма (Oakenfull et al., 1983). Тритерпеновые гликозиды, включаемые в пищу, как было показано, снижают содержание холестерина в крови и тканях экспериментальных животных (Cheeke, 1971). Было найдено, что во многих странах сапонины входят в состав лекарственных средств народной медицины и некоторых недавно разработанных фитопрепаратов.
Известно, что тритерпен, глицирретиновая кислота и некоторые его производные обладают противоязвенной, противовоспалительной, противоаллергической, противогепатитной и противовирусной активностью. Например, некоторые производные глицирретиновой кислоты могут быть средствами профилактики или лечения язвы желудка (Doll et al., 1962). Среди таких соединений известными в данной области являются карбеноксолон (патент США №3070623), производные сложного эфира глицирретиновой кислоты, замещенные по 3’-положению (патент США №3070624), аминокислотные соли глицирретиновой кислоты (публикация патента Японии А-44-32798), амидные производные глицирретиновой кислоты (патент Бельгии №753773) и амидные производные 11-дезоксиглицирретиновой кислоты (патент Великобритании №1346871). Было показано, что глицирретиновая кислота ингибирует ферменты, участвующие в биосинтезе лейкотриенов, включая 5-липоксигеназную активность, и, считается, что она ответственна за противовоспалительную активность (Inoue et al., 1986).
Сообщалось, что бетулиновая кислота, пентациклический тритерпен, является избирательным ингибитором роста меланомы человека в ксенотрансплантационных моделях бестимусных мышей, а также, как было показано, является причиной цитотоксичности вследствие индуцирования апоптоза (Pisha et al., 1995). Было продемонстрировано, что тритерпеновый сапонин, происходящий от китайского растения семейства тыквенных, обладает противоопухолевой активностью (Kong et al., 1993). Известно, что моногликозиды тритерпенов показывают сильнодействующую и избирательную цитотоксичность против клеток лейкоза человека MOLT-4 (Kasiwada et al., 1992), а некоторые тритерпеновые гликозиды растений семейства касатиковых подавляют рост опухолей и повышают продолжительность жизни мышей, которым была имплантирована асцитная карцинома Эрлиха (Nagamoto et al., 1988). Препарат сапонина, происходящего от долихоса Dolichos falcatus, относящегося к семейству бобовых, как сообщалось, эффективен в отношении клеток саркомы-37 in vitro и in vivo (Huang et al., 1982). Было показано, что сапонин сои, также представляющей семейство бобовых, эффективно действует на несколько типов опухолей (Tomas-Barbaren et al., 1988). Олеаноловая кислота и гипсогениновые гликозиды, проявляющие гемолитическую и моллюскоцидную активность, были выделены из размельченных плодов бобовых Swartzia madagascariensis (Leguminosae) (Borel & Hostettmann, 1987).
Генистеин, являющийся природным изофлавоноидом, выделенным из продуктов сои, является ингибитором тирозинкиназ, и, как было установлено, ингибирует пролиферацию эстроген-положительных и эстроген-отрицательных линий клеток карциномы молочной железы (Akiyama et al., 1987). Инозитолгексафосфат (фитиновая кислота), широко распространенный в растительном мире и являющийся естественным пищевым компонентом зерновых и бобовых продуктов, как было показано, обуславливает терминальную дифференцировку линии клеток карциномы толстой кишки. Фитиновая кислота также проявляет противоопухолевую активность в отношении экспериментального карциногенеза толстой кишки и молочной железы in vivo (Yang et al., 1995). Также было показано, что некоторые тритерпеновые агликоны обладают цитотоксической или цитостатической активностью: например, было показано, что кора ствола растения Crossopteryx febrifuga (Rubiaceae) обладает цитостатической активностью в отношении линии клеток карциномы толстой кишки человека Со-115 в диапазоне нг/мл (Tomas-Barbaren et al., 1988).
Хотя в предыдущих сообщениях были идентифицированы тритерпеновые соединения, нашедшие широкое применение, до сих пор в данной области техники имеется насущная потребность в идентификации новых биологически активных тритерпеновых соединений. Многие из этих соединений токсичны в отношении нормальных клеток млекопитающих. Кроме того, биологические активности ранее идентифицированных тритерпенов колеблются в широких пределах и многие из них, по-видимому, характеризуются ограниченной или варьирующейся степенью эффективности в лечении любого данного состояния человека или млекопитающего. Большое разнообразие различных тритерпенов, которые были идентифицированы ранее, и широкий диапазон вариабельности и непредсказуемости в проявлении биологических активностей, наблюдаемых даже у близкородственных тритерпеновых соединений, создает трудности, с которыми приходится сталкиваться при получении тритерпенов, которые представляют собой потенциальные терапевтические агенты. Решение трудной задачи идентификации новых тритерпенов с полезной биологической активностью должно открыть новые перспективы в лечении различных заболеваний человека, для которых возможности лечения в настоящее время ограничены.
Краткое содержание изобретения
Настоящее изобретение касается нового применения бобов и корней акации Виктории Acacia victoriae (Benth.) (Leguminosae) для выделения биологически полезных соединений. Семена Acacia victoriae используются в качестве пищевого продукта местными жителями Австралии в течение многих поколений (Lister et al., 1996). Однако, бобы и корни ранее отбрасывались как отходы. Следовательно, заявители настоящего изобретения продемонстрировали наличие новых противоопухолевых и других биологически полезных соединений в тех частях указанного растения, которые ранее не применялись. Например, новые биологически активные сапонины, описанные в настоящем изобретении, часто специфически цитотоксичны в отношении клеток злокачественных опухолей.
В одном из вариантов, настоящее изобретение представляет новые сапониновые соединения и их смеси, которые могут быть выделены из растения Acacia victoriae, и способы их применения. В этом отношении, один из вариантов настоящего изобретения представляет сапониновую композицию, содержащую тритерпен или другую ароматическую терпеноидную композицию. Описанные здесь сапонины также могут включать гликозидную группу.
В предпочтительных вариантах, в которых сапонин включает тритерпеновую составляющую, такая тритерпеновая составляющая обычно является акациевой кислотой или олеаноловой кислотой (карофиллином), или иной структурно сходной тритерпеновой составляющей. Тритерпеновые или тритерпенгликозидные соединения также могут, в основном, включать монотерпеновую(ые) составляющую(ие), и для специалиста в данной области техники должно быть очевидно, что описываемые здесь сапониновые соединения могут быть дополнительно замещены другими химическими функциональными группами. Таким образом, описанные здесь сапониновые соединения могут включать тритерпеновую составляющую, присоединенную, по крайней мере, к одному, предпочтительно к двум, трем и более монотерпеновым составляющим. Когда присутствует более одной монотерпеновой составляющей, то каждая из них может быть присоединена (i) непосредственно к тритерпеновой составляющей; (ii) к сахару или иной связывающей группе, которая присоединена к тритерпеновой составляющей; или (iii) к монотерпеновой составляющей, которая, в свою очередь, присоединена к тритерпеновой составляющей непосредственно или через сахар или другие связывающие группы. Связывающие группы включают сахара, ацильные, амидные, алкокси, кетильные, алкильные, алкиленовые и другие подобные химические группы, которые известны специалистам в данной области техники. Описанные здесь тритерпеновые гликозиды обычно имеют молекулярную массу в диапазоне 1800-2600 а.е.м. или от по крайней мере 1800, 1900, 2000, 2100 до примерно 2200, 2300, 2400 или 2600 а.е.м.
Важным аспектом настоящего изобретения является выделение смеси, содержащей один или большее число выделенных сапонинов или тритерпеновых гликозидов, которые могут быть охарактеризованы следующими свойствами: (а) выделяемостью из тканей Acacia victoriae: (b) наличием, по крайней мере, одного тритерпенового гликозида, имеющего молекулярную массу примерно от 1800 до 2600 а.е.м.; (с) способностью индуцировать цитотоксичность в отношении клетки Jurkat; и (d) способностью индуцировать апоптоз клетки Jurkat.
В конкретных вариантах настоящего изобретения, тритерпеновая композиция может характеризоваться следующими свойствами: способностью индуцировать цитотоксичность в отношении клетки Jurkat при IC50 от примерно 0,12 мкг/мл до примерно 0,40 мкг/мл. В других вариантах настоящего изобретения, апоптоз индуцируют путем введения в клетку Jurkat концентрации примерно от 100 до 400 нг/мл. В других вариантах настоящего изобретения апоптоз индуцируют путем введения в клетки Jurkat концентрации от примерно 200 до примерно 250, 300, 350 или 400 нг/мл или примерно от 300 до примерно 350 или 400 нг/мл.
В следующих вариантах настоящего изобретения уровень апоптоза измеряют по перестройке плазматической мембраны клетки Jurkat по связыванию аннексина. Это можно оценить с применением проточной цитометрии, и уровень индуцированного апоптоза может составлять 16-18%.
В других своих вариантах, настоящее изобретение относится к смеси, содержащей один или большее число выделенных тритерпеновых гликозидов, характеризующихся следующими свойствами: (а) выделяемостью из тканей Acacia victoriae; (b) наличием, по крайней мере, одного тритерпенового гликозида с молекулярной массой от примерно 1800 до примерно 2600 а.е.м.; и (с) способностью индуцировать высвобождение цитохрома-с из митохондрий клеток Jurkat.
В следующих вариантах настоящего изобретения представляется смесь, содержащая один или большее число выделенных тритерпеновых гликозидов, характеризующихся следующими свойствами: (а) выделяемостью из тканей Acacia victoriae; (b) наличием, по крайней мере, одного тритерпенового гликозида с молекулярной массой от примерно 1800 до примерно 2600 а.е.м.; и (с) способностью активировать каспазу-3 в клетке Jurkat, где каспазная активность составляет в пределах примерно от 0,3 до 1,6 единиц флуоресценции/мин/мг.
В других вариантах настоящего изобретения, смесь, содержащая один или большее число выделенных тритерпеновых гликозидов, может характеризоваться следующими свойствами: (а) выделяемостью из тканей Acacia victoriae; (b) наличием, по крайней мере, одного тритерпенового гликозида с молекулярной массой от примерно 1800 до примерно 2600 а.е.м.; и (с) способностью обуславливать расщепление белка PARP в клетке Jurkat.
В других вариантах настоящего изобретения смесь, содержащая один или большее число выделенных тритерпеновых гликозидов, может характеризоваться следующими свойствами: (а) выделяемостью из тканей Acacia victoriae; (b) наличием, по крайней мере, одного тритерпенового гликозида с молекулярной массой от примерно 1800 до примерно 2600 а.е.м.; и (с) способностью подавлять активность киназы PI3 в клетке Jurkat.
В других вариантах настоящего изобретения смесь, содержащая один или большее число выделенных тритерпеновых гликозидов, может характеризоваться следующими свойствами: (а) выделяемостью из тканей Acacia victoriae; и (b) способностью подавлять инициацию и активацию эпителиальных клеток млекопитающего до предопухолевого или злокачественного статуса.
В других вариантах настоящего изобретения, смесь, содержащая один или большее число выделенных тритерпеновых гликозидов, может характеризоваться следующими свойствами: (а) выделяемостью из тканей Acacia victoriae; и (b) способностью индуцировать апоптоз злокачественных клеток у млекопитающих.
В своем важном аспекте настоящее изобретение относится к натуральной фармацевтической композиции, содержащей тритерпеновый гликозид в фармацевтически приемлемой среде, такой как буфер, растворитель, разбавитель, инертный носитель, масло, крем или годный в пищу материал. В одном из вариантов настоящего изобретения нутрицевтическая композиция может содержать высушенные и измельченные корни, бобы Acacia victoriae или их сочетания в фармакологически приемлемой среде. Раскрываемые здесь нутрицевтические композиции могут иметь форму таблетки, капсулы или мази.
В другом своем аспекте, настоящее изобретение относится к способу получения композиции, содержащей смесь одного или большего числа выделенных тритерпеновых гликозидов, включающему: (а) взятие ткани растения Acacia victoriae; (b) экстракцию данной ткани растворителем с получением экстракта; и (с) получение одного или большего числа тритерпеновых гликозидов из данного экстракта. Обычно используемыми в данном способе тканями являются бобы, корни, проростки или их смеси. Растворителем, применяемым для экстракции, может быть любой органический растворитель, пригодный для экстракции, часто путем растворения, нужного сапонинового соединения. Применимыми для экстракции растворителями являются метанол, этанол, изопропиловый спирт, дихлорметан, хлороформ, этилацетат, вода, глицерин и их смеси.
Данный способ может включать дополнительные стадии.
Например, указанный способ может дополнительно включать выделение композиции из багассы фильтрованием после экстракции. В другом варианте данный способ дополнительно включает стадию обезжиривания растительной ткани с использованием органического растворителя перед проведением экстракции. Органическим растворителем может быть любой пригодный для обезжиривания растворитель, такой как гексан, дихлорметан, хлороформ, этилацетат или их смеси. В другом варианте способ выделения дополнительно включает выпаривание растворителя после проведения экстракции.
Данный способ также может включать получение смеси тритерпеновых композиций путем хроматографического выделения, по крайней мере, одного тритерпенового гликозидного соединения. Примерами методов хроматографии являются жидкостная хроматография, ЖХСД или ВЭЖХ. Хотя растворители, которые могут быть использованы для хроматографического выделения, должны быть определены специалистом в данной области техники, примерами таких растворителей являются метанол, ацетонитрил, вода и смеси.
Еще в одном своем аспекте, настоящее изобретение относится к способу получения композиции, содержащей смесь одного или большего числа выделенных тритерпеновых гликозидов, включающему: (а) получение тканевой культуры, включающей клетки растения Acacia victoriae; и (b) экстракцию тритерпеновых композиций из указанных клеток с помощью растворителя, тем самым экстрагируя, по крайней мере, первое тритерпеновое соединение из данной ткани. В одном из аспектов, данная тканевая культура включает культуру волосовидных корней. В другом аспекте настоящего изобретения, тканевую культуру приготавливают путем инфицирования клеток Acacia victoriae клетками Agrobacterium rhizogenes штамма R-1000. В близком аспекте настоящего изобретения, тканевая культура включает культуральную среду, содержащую сахарозу в количестве от примерно 3% до примерно 4% по весу. В другом аспекте настоящего изобретения используемым для экстракции композиции растворителем является метанол, этанол, изопропиловый спирт, дихлорметан, этилацетат, вода или их смеси.
Еще в одном аспекте настоящего изобретения, этот способ, кроме того, включает дополнительные стадии, такие как отфильтровывание растительной багассы из смеси тритерпенов, выделение смешанной тритерпеновой композиции методом жидкостной хроматографии и (или) выпаривание растворителя после экстракции.
В одном из аспектов описывается способ непрерывного воспроизведения тканей Acacia victoriae, из которых можно экстрагировать активные соединения по настоящему изобретению. В одном из вариантов настоящего изобретения, описывается тканевая культура волосовидных корней, включающая клетки Acacia victoriae, которые были инфицированы Agrobacterium rhizogenes R-1000 в соответствующей культуральной среде. В близком варианте эта среда для культивирования тканей содержит от примерно 3% до примерно 4% сахарозы.
В другом аспекте настоящего изобретения, описан способ непрерывного сбора ткани растения Acacia victoriae, включающий: (а) выращивание Acacia victoriae методом гидропоники; и (b) сбор ткани растения от примерно одного до примерно 4 раз в год, причем этот сбор ткани не приводит к гибели растения. В близком варианте настоящего изобретения, системой выращивания является аэропоника. В другом близком варианте настоящего изобретения, используемой для культивирования тканью Acacia victoriae является корневая ткань.
Важным аспектом настоящего изобретения является способ подавления инициации и активации эпителиальных клеток млекопитающего до предопухолевого или злокачественного статуса, включающий введение в клетку млекопитающего терапевтически эффективного количества нутрицевтической композиции, описанной выше. В одном из вариантов, такой эпителиальной клеткой является клетка кожи, клетка толстой кишки, клетка матки, клетка яичника, клетка поджелудочной железы, клетка предстательной железы, почечная клетка, клетка легкого, клетка мочевого пузыря или клетка молочной железы. В близком варианте настоящего изобретения, указанным млекопитающим является человек. Еще в одном близком варианте настоящего изобретения способом введения нутрицевтической композиции является пероральное введение. В альтернативном варианте настоящего изобретения, способом введения нутрицевтической композиции является местное введение.
Настоящее изобретение также относится к способу индукции апоптоза злокачественной клетки млекопитающего, включающему обработку этой клетки терапевтически эффективным количеством нутрицевтической композиции, описанной выше. В одном варианте, указанной клеткой является клетка кожи, клетка толстой кишки, клетка матки, клетка яичника, клетка поджелудочной железы, клетка предстательной железы, почечная клетка, клетка легкого, клетка мочевого пузыря или клетка молочной железы. В близком варианте млекопитающим является человек. Еще в одном близком варианте способом введения нутрицевтической композиции является пероральное введение. В альтернативном варианте настоящего изобретения, способом введения нутрицевтической композиции является местное введение.
Настоящее изобретение также относится к способу предотвращения аномальной пролиферации эпителиальных клеток млекопитающих in vitro или в организме млекопитающего, включающему обработку клетки млекопитающего или введение этому млекопитающему терапевтически эффективного количества нутрицевтических композиций, описанных выше. В одном из аспектов настоящего изобретения эпителиальными клетками являются клетки кишечных крипт. В другом аспекте настоящего изобретения, эпителиальными клетками являются клетки толстой кишки. В близком варианте настоящего изобретения млекопитающим является человек. Еще в одном близком варианте настоящего изобретения, способом введения нутрицевтической композиции in vivo является пероральное введение.
Настоящее изобретение также представляет способ лечения млекопитающего от воспаления, включающий введение этому млекопитающему терапевтически эффективного количества нутрицевтической композиции, описанной выше. В близком варианте настоящего изобретения, таким млекопитающим является человек.
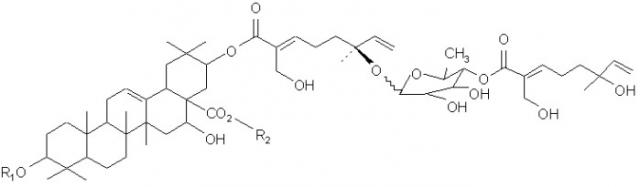
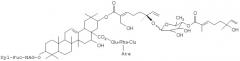
Настоящее изобретение также представляет очищенное тритерпеновое соединение, включающее тритерпеновую составляющую, соединенную с монотерпеновой составляющей следующей формулы:
или его фармацевтический препарат, где (a) R1 и R2 выбирают из группы, состоящей из водорода, C1-5-алкила или олигосахарида;
(b) R3 выбирают из группы, состоящей из водорода, гидроксила, C1-5-алкила, C1-5-алкилена, C1-5-алкилкарбонила, сахара и монотерпеновой группы; и (с) данная формула дополнительно включает R4, где R4 выбирают из группы, состоящей из водорода, гидроксила, C1-5-алкила, C1-5-алкилена, C1-5-алкилкарбонила, сахара, C1-5-алкилового сложного эфира и монотерпеновой группы, и где R4 может быть соединен с тритерпеновой составляющей или монотерпеновой составляющей. Настоящее изобретение также относится к соединению, в котором R3 представляет сахар. В близких вариантах настоящего изобретения, сахар выбирают из группы, состоящей из глюкозы, фукозы, рамнозы, арабинозы, ксилозы, хиновозы, мальтозы, глюкуроновой кислоты, рибозы, N-ацетилглюкозамина и галактозы. В других близких вариантах настоящего изобретения соединение дополнительно включает монотерпеновую составляющую, соединенную с сахаром. Настоящее изобретение представляет соединение, в котором R3 имеет формулу:
где R5 выбирают из группы, состоящей из водорода, гидроксила, C1-5-алкила, C1-5-алкилена, C1-5-алкилкарбонила, сахара, C1-5-алкилового сложного эфира и монотерпеновой группы.
В одном из вариантов настоящего изобретения, R5 представляет водород или гидроксил. В другом варианте настоящего изобретения, каждый из R1 и R2 включает олигосахарид. Еще в одном варианте настоящего изобретения, каждый из R1 и R2 включает моносахарид, дисахарид, трисахарид или тетрасахарид. В близких вариантах настоящего изобретения, каждый из R1 и R2 включает сахара, которые отдельно и независимо друг от друга выбирают из группы, состоящей из глюкозы, фукозы, рамнозы, арабинозы, ксилозы, мальтозы, хиновозы, глюкуроновой кислоты, рибозы, N-ацетилглюкозамина и галактозы. В других аспектах настоящего изобретения, по крайней мере, один из сахаров метилирован.
В одном из вариантов настоящего изобретения, R4 соединен с тритерпеновой составляющей посредством одного из углеродов метилена, соединенного с тритерпеновой составляющей. В другом варианте настоящего изобретения, тритерпеновой составляющей является олеаноловая кислота вместо акациевой кислоты.
В другом своем варианте, настоящее изобретение относится к композиции, содержащей тритерпеновый гликозид следующей формулы:
или к ее фармацевтическому препарату, где (а) R1 представляет олигосахарид, включающий N-ацетилглюкозамин, фукозу и ксилозу;
и (b) R2 представляет олигосахарид, включающий глюкозу, арабинозу и рамнозу. В своем близком варианте, настоящее изобретение относится к соединению формулы:
или его фармацевтическому препарату.
В другом своем аспекте, настоящее изобретение относится к очистке композиции, содержащей тритерпеновый гликозид, имеющий молекулярную формулу:
или ее фармацевтического препарата, где (a) R1 представляет олигосахарид, включающий N-ацетилглюкозамин, фукозу и ксилозу; и (b) R2 представляет олигосахарид, включающий глюкозу, арабинозу и рамнозу. В своем близком аспекте, настоящее изобретение относится к очистке и характеризации соединения формулы:
или его фармацевтического препарата.
Еще в одном своем аспекте, настоящее изобретение относится к очистке композиции, содержащей тритерпеновый гликозид, имеющий молекулярную формулу:
или ее фармацевтического препарата, где (a) R1 представляет олигосахарид, включающий N-ацетилглюкозамин, глюкозу, фукозу и ксилозу; и (b) R2 представляет олигосахарид, включающий глюкозу, арабинозу и рамнозу. В своем близком аспекте, настоящее изобретение относится к очистке и характеризации соединения, имеющего молекулярную формулу:
В другом своем аспекте, настоящее изобретение касается соединения, включающего тритерпеновую составляющую, олигосахарид и три монотерпеновые единицы. В одном из вариантов, тритерпеновой составляющей является акациевая кислота или олеаноловая кислота.
Важным аспектом настоящего изобретения является получение фармацевтических препаратов, содержащих очищенные и охарактеризованные соединения. В одном из вариантов, фармацевтический препарат представляет собой фармакологически приемлемую среду, включающую буфер, растворитель, разбавитель, инертный носитель, масло, крем или годный в пищу материал. В некоторых аспектах настоящего изобретения, рассматриваемая фармацевтическая композиция, кроме того, содержит агент для направленной доставки. В близких аспектах настоящего изобретения, такой агент направленной доставки способен осуществлять прямую доставку фармацевтической композиции к эпителиальной клетке. В близком варианте настоящего изобретения, таким агентом направленной доставки является антитело, связывающееся с данной эпителиальной клеткой.А
В некоторых вариантах настоящего изобретения, фармацевтическая композиция содержит, по крайней мере, еще одно соединение, которое может уничтожать эпителиальную клетку.
Для соединений по настоящему изобретению был продемонстрирован хемопротективный эффект у мышей, на которых воздействовали канцерогеном DMBA. Следовательно, настоящее изобретение относится к способу подавления инициации и активации эпителиальной клетки млекопитающего до предопухолевого или злокачественного статуса у млекопитающего, включающему введение данному млекопитающему терапевтически эффективного количества фармацевтических композиций, описанных выше. В одном из вариантов настоящего изобретения, эпителиальная клетка является клеткой кожи, клеткой толстой кишки, клеткой матки, клеткой яичника, клеткой поджелудочной железы, клеткой легкого, клеткой мочевого пузыря, клеткой предстательной железы, почечной клеткой или клеткой молочной железы. В близком варианте настоящего изобретения, млекопитающим является человек. Еще в одном близком варианте настоящего изобретения, способом введения фармацевтической композиции является пероральное введение. И еще в одном близком варианте настоящего изобретения способом введения фармацевтической композиции является местное введение. Еще в одном варианте настоящего изобретения, способом введения фармацевтической композиции является внутриопухолевая инъекция. В другом варианте настоящего изобретения, способом введения фармацевтической композиции является внутривенное введение. И еще в одном варианте изобретения, способом введения фармацевтической композиции является ингаляция аэрозолем.
Настоящее изобретение также относится к введению фармацевтических композиций по настоящему изобретению в сочетании с другими способами лечения. В одном из вариантов, такими другими способами лечения являются рентгеновское, ультрафиолетовое, γ- или микроволновое облучение эпителиальной клетки.
Настоящее изобретение также относится к способу стимулирования апоптоза злокачественной клетки млекопитающего, предусматривающему введение этому млекопитающему терапевтически эффективного количества фармацевтических композиций, описанных в данной заявке. В одном из вариантов настоящего изобретения, такой клеткой является клетка кожи, клетка толстой кишки, клетка матки, клетка яичника, клетка поджелудочной железы, клетка легкого, клетка мочевого пузыря, клетка предстательной железы, почечная клетка или клетка молочной железы.
В одном из своих важных аспектов, настоящее изобретение относится к способу предотвращения аномальной пролиферации эпителиальной клетки у млекопитающего, предусматривающему введение этому млекопитающему терапевтически эффективного количества фармацевтических композиций, описанных выше. В одном варианте, такой эпителиальной клеткой является клетка кишечной крипты. В другом варианте настоящего изобретения, такой эпителиальной клеткой является клетка толстой кишки. В близком варианте настоящего изобретения, таким млекопитающим является человек. Еще в одном близком варианте настоящего изобретения, способом введения фармацевтической композиции является пероральное введение. Еще в одном варианте настоящего изобретения, способом введения является местное введение. Еще в одном варианте настоящего изобретения, способом введения является внутриопухолевая инъекция. В другом варианте настоящего изобретения, способом введения фармацевтической композиции является внутривенное введение. В следующем варианте настоящего изобретения, способом введения фармацевтической композиции является ингаляция аэрозолем. Настоящее изобретение также относится к использованию фармацевтических композиций по настоящему изобретению в сочетании с другими способами лечения. В одном из вариантов, такими другими способами лечения являются рентгеновское, ультрафиолетовое, γ- или микроволновое облучение эпителиальной клетки.
Настоящее изобретение также относится к способу лечения млекопитающего от воспаления, включающему введение этому млекопитающему терапевтически эффективного количества описанной здесь фармацевтической композиции, содержащей тритерпеновые соединения. В близком варианте настоящего изобретения, таким млекопитающим является человек. Еще в одном варианте настоящего изобретения, способом введения фармацевтической композиции является пероральное введение. Еще в одном варианте настоящего изобретения, способом введения является местное введение. В другом варианте настоящего изобретения, способом введения фармацевтической композиции является ингаляция аэрозолем.
Другим важным аспектом настоящего изобретения является способ регуляции ангиогенеза у млекопитающего, предусматривающий введение этому млекопитающему терапевтически эффективного количества описанных здесь фармацевтических композиций. Этот способ может быть применен, если этим млекопитающим является человек.
Хотя некоторые из описываемых здесь способов применяются in vitro, однако, предполагается, что и in vivo тритерпеновые гликозидные соединения будут проявлять аналогичные эффекты.
В дополнение к представляемым способам профилактики и лечения раковых опухолей с использованием соединений по настоящему изобретению заявители представляют ряд других путей применения соединений по настоящему изобретению. В частности, соединения по настоящему изобретению могут быть использованы в качестве растворителей, антиоксидантов, противогрибковых и противовирусных агентов, ихтиоцидов или моллюскоцидов, контрацептивов, противогельминтных средств, регуляторов ангиогенеза, средств для защиты от УФ-излучения, отхаркивающих средств, мочегонных средств, противовоспалительных средств, регуляторов метаболизма холестерина, сердечно-сосудистых эффекторов, противоязвенных средств, болеутоляющих средств, седативных средств, иммуномодуляторов, жаропонижающих средств, средств против ломкости капилляров, средств против проявлений старения, средств для повышения содержания коллагена в коже, средств для усиления мужской половой функции и средств для улучшения познавательной способности и памяти.
Краткое описание чертежей
Следующие чертежи являются частью описания настоящего изобретения и включены для дополнительной иллюстрации некоторых его аспектов. Настоящее изобретение может быть лучше понято с помощью отсылки к одному или нескольким чертежам в сочетании с подробным описанием конкретных вариантов.
Фиг.1. Влияние UA-BRF-004-DELEP-F001 на линии опухолевых клеток человека. На фиг.1 проиллюстрировано подавление роста клеточных линий яичников (SK-OV-3, HEY, OVCAR-3), молочной железы (MDA-468), меланомы (А375-М, Hs294t) и эпидермоидных клеток человека (А431), обработанных неочищенным экстрактом бобового растения.
Фиг.2. Влияние UA-BRF-004-DELEP-F023 (фракция 23) на трансформированные и нетрансформированные клеточные линии. На фиг.2 проиллюстрирована цитотоксичность, проявляемая фракцией 23, в отношении клеток яичников (SK-OV-3, OCC1, HEY, OVCAR-3), клетки Т-клеточного лейкоза (Jurkat), простаты (LNCaP), первичных клеток опухоли яичника человека (FTC), фибробластов человека (FS) и эндотелиальных клеток (HUVEC). Уровень цитотоксичности в нетрансформированных клетках составил лишь 15-17%, в то время как в отношении опухолевых клеток она составила 50-95%.
Фиг.3. Влияние фракции 35 (“UA-BRF-004-DELEP-F035” или “F035”) на линии опухолевых клеток человека. На фиг.3 показана цитотоксичность, проявляемая обработанными фракцией 35 клетками яичника (HEY, OVCAR-3, C-1, SK-OV-3), поджелудочной железы (PANC-1) и почек (769-Р, 786-О, А498) человека. Величины IC50 для этих клеточных линий варьировались в пределах 1-6 мкг/мл.
Фиг.4. Влияние фракции 35 на линии лейкозных клеток. На фиг.4 показано, что фракция 35 проявляет сильную цитотоксичность в отношении клеток Jurkat (Т-клеточный лейкоз) при IC50 130 нг/мл и IC50 для клеток REH, KG-1 и NALM-6 (В-клеточные лейкозы) в диапазоне 1-3 мкг/мл.
Фиг.5. Влияние фракции 35 на пролиферацию эндотелиальных клеток. На фиг.5 показано, что фракция 35 является сильным ингибитором пролиферации эндотелиальных клеток при стимуляции bFGF или без таковой.
Фиг.6. Влияние фракции 35 на миграцию эндотелиальных клеток капилляров. На фиг.6 показано отсутствие влияния на миграцию эндотелиальных клеток капилляров, что подтверждает отсутствие токсичности.
Фиг.7. Показаны результаты тонкослойной хроматографии экстрактов проростков и каллюсов. Дорожка 1 - стеблевые каллюсы, сформированные в среде BA-IAA; дорожка 2 - корневые каллюсы, сформированные в среде BA-IAA; дорожка 3 - каллюс из клеток гипокотиля; дорожка 4 - проросток, обработанный метилжасмонатом (100 мкМ) в полутвердой среде; дорожка 5 - контрольный проросток, выращенный в полутвердой среде; дорожка 6 - стандарт F023; дорожка 7 - побег, выращенный в среде ВА; дорожка 8 - проросток, обработанный 50 мкМ метилжасмоната; дорожка 9 - проросток, обработанный 100 мкМ метилжасмоната; дорожка 10 - проросток, обработанный 200 мкМ метилжасмоната; дорожка 11 - контрольный проросток; и дорожка 12 - стандарт F023.
Фиг.8. Приведена фотография мыши SENCAR (слева) и гибридной мыши SENCARxC57B1 (справа), Обеим мышам повторно вводили дозы по 100 нмоль DMBA в течение 8 недель. На 15-й неделе у обеих мышей отмечено развитие множественных папиллом, однако у гибридных мышей SENCAR×C57B1 папилломы были мельче и их число было меньше. Линия С57В1 резистентна к канцерогенезу и у нее не развиваются опухоли.
Фиг.9A-F. Показаны срезы эпидермиса мышей, обработанных ацетоном, DMBA или DMBA + UA-BRF-004-DELEP-F035. Фиг.9А: обработка ацетоном на 4-й неделе. Фиг.9В: обработка ацетоном на 8-й неделе. Фиг.9С: обработка DMBA на 4-й неделе. Фиг.9D: обработка DMBA на 8-й неделе. Фиг.9Е: обработка DMBA + UA-BRF-004-DELEP-F035 на 4-й неделе. Фиг.9F: обработка DMBA + UA-BRF-004-DELEP-F035 на 8-й неделе.
Фиг.10А-В. Продемонстрирован антиоксидантный эффект UA-BRF-004-DELEP-F035 в отношении ДНК через 4 недели. Фиг.10А: показан антиоксидантный эффект после обработки низкой концентрацией UA-BRF-004-DELEP-F035 (0,1 мг на 0,2 мл). Фиг.10В: показан антиоксидантный эффект после обработки высокой концентрацией UA-BRF-004-DELEP-F035 (0,3 мг на 0,2 мл).
Фиг.11А-В. Показана толщина эпидермиса через 4 недели после обработки DMBA и UA-BRF-004-DELEP-F035. Фиг.11А: показано влияние обработки низкой концентрацией UA-BRF-004-DELEP-F035 (0,1 мг на 0,2 мл) на толщину эпидермиса. Фиг.11В: показано