Способ лечения хирургического эндотоксикоза
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к хирургии, и касается лечения "хирургического" эндотоксикоза, в частности перитонита. Для этого используют порошковый продукт столовой свеклы, приготовленный из сублимированного сырья. С первых суток после операции осуществляют энтеральное введение гомогенизированной водной взвеси продукта из расчета 20 г сухого вещества на 300 мл питьевой воды 18-22°С в назоинтестинальный зонд, после интраоперационного отмывания тонкой кишки. Введение проводят 3 раза в сутки, курсом 3-5 дней. Способ обеспечивает одновременную энтеросорбцию, стимуляцию моторики кишечника и нутритивную поддержку. 2 з.п. ф-лы, 5 табл., 8 фиг.
Реферат
Изобретение относится к области медицины, а именно к хирургии, и может быть использовано для лечения хирургического эндотоксикоза путем энтеросорбции с применением пектинсодержащих препаратов.
Метод энтеросорбции, применяемый для детоксикации организма, при трех-четырех разовом приеме энтеросорбента в течение нескольких дней, позволяет достичь эффекта, равного процедуре гемосорбции. Метод неинвазивен, не имеет осложнений, связанных с экстракорпоральной детоксикацией, и более физиологичен. В настоящее время применяется целый ряд энтеросорбентов для лечения патологии органов пищеварения, в т.ч. 1%-ный водный раствор пектина (“Клиническое применение препарата энтеросгель у больных с патологией органов пищеварения”. Новые подходы к терапии. Методические рекомендации для врачей. Под ред. проф. И.В.Маева, Ю.Н.Шевченко, доц. А.Б.Петухова, Москва, 2000, с.5-8). Особого внимания заслуживают высокодисперстные гидрофильные порошковые сорбенты из-за их сравнительно большей сорбирующей поверхности и хорошей текучести в растворе.
Недостатки известных сорбентов следующие: не все известные сорбенты пригодны для длительного введения в кишечник через назоинтестинальный зонд по своей физической форме (отсутствие нужной текучести), что приводит к обтурации зондов и нарушению их функции, известные энтеросорбенты не стимулируют моторику кишечника при его парезе, в т.ч. послеоперационном, что затрудняет эвакуацию связанных токсинов естественным путем, не обладают пробиотическими и нутритивными свойствами, т.е. не влияют на сопутствующую эндотоксикозу, особенно хирургическому, энтеральную недостаточность. Совокупность этих недостатков усложняет и удлиняет лечение больных с синдромом хирургического эндотоксикоза.
Прототипом изобретения является способ детоксикации при перитоните путем интраоперационного удаления токсичного содержимого тонкой кишки через назоинтестинальный зонд с отмыванием ее до чистой воды и последующим пассивным сифонным дренажем кишки на фоне энтеросорбции. Для энтеросорбции используется угольный волокнистый сорбент “Белосорб” стабилизированный крахмальным гелем. “Белосорб” используется в дозе 0,3 г на 1 кг веса в 100 мл геля. Гель приготавливается из расчета 2 г крахмала на 100 мл воды. После введения сорбента дренаж пережимается на 1 час. Процедура повторяется после операции каждые 6 часов. При этом отмечено снижение интоксикации и токсичности кишечного отделяемого. На 4-е сутки после операции отмечали снижение количества кишечного отделяемого с 2400±300 мл до 500±200 мл, что связывали с нормализацией пассажа по кишечнику (В.В.Кирковский. Детоксикационная терапия при перитоните, “Полифакт-Альфа”, Минск, Белоруссия, 1997, с.68-70).
Недостатками прототипа являются: отсутствие стимуляции моторики кишечника, что требует пассивного сифонного дренажа кишки, частое (каждые 6 часов) введение сорбента с пережатием дренажа при каждом сеансе на 1 час, т.е. прекращение декомпрессии кишки на 4 часа в сутки. Кроме этого, использованная сорбирующая смесь не обладает санирующим в отношении кишечной флоры и нутритивным эффектом.
Задачей изобретения является усовершенствование известного способа лечения хирургического эндотоксикоза путем одномоментной энтеросорбции, стимуляции моторики кишечника и нутритивной поддержкой в раннем послеоперационном периоде в условиях энтеральной недостаточности.
Для решения этой задачи мы использовали пектинсодержащий порошковых продукт столовой свеклы из сублимированного сырья, 20 г в 300 мл питьевой воды температурой 18-22 градуса по Цельсию. Раствор вводили в назоинтестинальный зонд болюсно, 3 раза в день, курсом 5-7 дней, с первых суток после операции, на фоне общепринятой послеоперационной терапии.
Порошковый продукт столовой свеклы приготавливается согласно ТУ 9199-013-00353158-97 (разработан впервые), сертификат на продукт №77.72.10.916.П.05042. Оптимальное сохранение состава и свойств сырья, высокую гигроскопичность и сорбционную активность, физическую форму высокодисперстного порошка обеспечивают технологии с использованием сублимации, защищеные патентами №2136182 и №2154969 выданными Роспатентом.
| Анализ образца сухого препарата свеклы | |
| Наименование показателя | Образец свеклы |
| Массовая доля углеводов, % | 67,9 |
| Массовыя доля клетчатки, % | 6,3 |
| Массовая доля лигнина, % | 6,8 |
| Массовая доля пектинов, % | 0,7-1,0 |
| Аминокислоты, мас.%** | |
| Лизин* | 0,30 |
| Гистидин* | 0,25 |
| Аргинин* | 0,35 |
| Аспарогиновая кислота | 0,65 |
| Треонин * | 0,24 |
| Серин | 0,31 |
| Глутаминовая кислота** | 2,79 |
| Пролин | 0,34 |
| Глицин | 0,25 |
| Аланин | 0,47 |
| Цистин | 0,07 |
| Валин | 0,33 |
| Метионин* | 0,09 |
| Изолейцин | 0,25 |
| Лейцин | 0,32 |
| Тирозин | 0,21 |
| Фенилаланин* | 0,19 |
| Йод, % | 0,36 |
| Бетаин, % | 0,469 |
| *незаменимые | |
| **Продукты содержат 17 аминокислот, в т.ч. 2,2-2,79 мас.% глутаминовой. |
Глутамин занимает центральное место в азотистом обмене, являясь предшественником синтеза пурина и пиримидина, является главным пластическим и энергетическим материалом для быстрорастущих клеток - энтероцитов, лимфоцитов и макрофагов. Глутамин - транспортное средство для переноса аммиака в нетоксичной форме из периферической ткани в почки для экскреции и в печень для образования мочевины. Большая часть его метаболизируется в слизистой оболочке тонкой кишки вместо глюкозы, жирных кислот или кетонов, сохраняя их для других жизненно важных органов.
Продукт содержит биологически активных веществ 2%, в т.ч. 0,7-1,0% пектинов (емкость по протопектинам - до 20%, что позволяет восполнять утилизированные пектины при диссоциации в водной среде), бетаин, флавоноиды, иод, калий, натрий, кальций, магний, марганец, железо, цинк, медь, никель, кобальт (хром, свинец, кадмий, ртуть, мышьяк - не обнаружены), бета-каротин, витамины В1, В3, Вс, РР, Н, С, К, мезо-инозит.
Сорбционную активность определяют: большая сорбирующая поверхность за счет физической формы высокодисперстного порошка, гидрофильность до 1:20 за счет сублимации, наличие лигнина, пектинов и протопектинов. Пектины, образуя гидрофильный гель, стимулируют моторику кишечника, в т.ч. при его парезе. Нутритивные возможности определяются пищевой ценностью по углеводам, белкам, про- и витаминам, микроэлементам.
Пектины являются пробиотиками, диссоциируют на короткоцепочечные жирные кислоты (ацетаты, пропионаты, бутираты) обладают цитопротективным эффектом по отношению к энтеро- и колоноцитам, создают условия для сохранения и восстановления собственной микрофлоры кишечника. Водная взвесь обладает высокой текучестью и легко вводится в назоинтестинальные зонды, начиная с диаметра 0,5 см, не закупоривая их.
Способ осуществляется следующим образом. Интраоперационно устанавливается назоинтестинальный зонд и удаляется желудочное и тонкокишечное содержимое, зонд отмывают до чистых промывных вод. С первых суток после операции начинают энтеральную терапию. Для этого готовят водную взвесь порошкового продукта столовой свеклы из расчета 20 г на 300 мл питьевой воды температурой 18-22 градуса по Цельсию. После гомогенизации раствора его вводят болюсно шприцем Жане в назоинтестинальный зонд и зонд перекрывают зажимом на 30 минут. Процедуру повторяют три раза в день в течение 3-5-7 дней. Курс лечения прекращают после исчезновения признаков интоксикации и восстановления моторики кишечника. После этого назоинтестинальный зонд удаляют и начинают естественное питание. Осложнений и побочных действий способа, кроме диареи, не отмечено. Диарея прекращалась самостоятельно через сутки после отмены препарата.
В клинике предложенный способ был применен в лечении 60 больных разлитым перитонитом различной этиологии в токсической и терминальной стадиях с сопутствующей энтеральной недостаточностью разной степени тяжести. Все больные были обследованы общеклинически, лабораторно, инструментально. После операции больные лечились в отделении реанимации. С первых суток в комплексе с общепринятой интенсивной терапией им применен предлагаемый способ лечения. Контрольную группу составили 50 аналогичных больных. Им проводилась только общепринятая интенсивная терапия с декомпрессией кишечника через назоинтестинальный зонд. Для сравнения эффективности предложенного способа с прототипом 40 аналогичным больным проведена энтеросорбция углеродным сорбентом УАО-А. Группы формировались методом парной выборки.
Результаты лечения оценивали по динамике тяжести состояния с использованием шкалы SAPS (Le Gall G.R., 1984), лейкоцитарного индекса интоксикации (ЛИИ), веществ средней молекулярной массы (ВСММ) в плазме крови, длительности назоинтестинальной интубации, скорости разрешения пареза кишечника, летальности.
Клинический пример. Больной В., 34 лет, история болезни №6118 поступил в 3 хирургическое отделение Г.К.Б. №50 27.03.2002 года с направительным диагнозом: проникающее колото-резаное ранение живота, перитонит, через сутки от его получения. При поступлении: общее состояние тяжелое, пульс 120 в 1 минуту, А.Д. 105 и 70 мм рт. столба, одышка, акроцианоз, живот напряжен, в дыхании не участвует, симптом Щеткина положителен во всех отделах, на обзорной рентгенограмме грудной клетки патологии не найдено, на обзорном снимке брюшной полости - пневматоз кишечника, множественные тонкокишечные арки, свободного газа в брюшной полости не найдено. После предоперационной подготовки экстренно оперирован. Операция №386 - первичная хирургическая обработка раны брюшной стенки, лапаротомия, ушивание ран тонкой кишки и большого сальника, санирование и дренирование брюшной полости, назогастральная и назоинтестинальная интубация. На операции: в брюшной полости до 800 мл темной крови и тонкокишечного содержимого, налеты фибрина на париетальной и висцеральной брюшине во всех отделах брюшной полости, два резаных дефекта тонкой кишки и большого сальника, парез тонкой кишки. Послеоперационный диагноз: проникающее ранение живота, ранения тонкой кишки и большого сальника, гемоперитонеум, разлитой фибринозный перитонит, парез тонкой кишки. Через назоинтестинальный зонд эвакуировано 2,5 л застойного содержимого. Для послеоперационного лечения больной переведен в отделение реанимации. При исходном обследовании: тяжесть состояния по SAPS 8,0, ЛИИ 8,5, ВСММ 600. С первых суток после операции, с 28.03.2002 года, выполнена энтеросорбция и энтеростимуляция по предложенному методу в течение 4 суток. Со стороны операционной раны осложнений нет, с 2 суток появился жидкий, свекольно окрашенный стул, на 3 сутки удалены нефункционирующие дренажи из брюшной полости, начата активизация. На 5 сутки тяжесть состояния по SAPS 2,0, ЛИИ 4,5, ВСММ 300. Парез кишечника разрешился, удалены зонды из желудка и тонкой кишки, больной переведен в 3 хирургическое отделение, начато обычное питание, стол 1-й хирургический. На 7 сутки переведен на 15 стол. На 8 сутки операционная рана зажила первичным натяжением, сняты кожные швы. При контрольном УЗИ на 3-5-7 сутки осложнений со стороны брюшной полости нет. На 10 сутки в удовлетворительном состоянии выписан под наблюдение хирурга поликлиники.
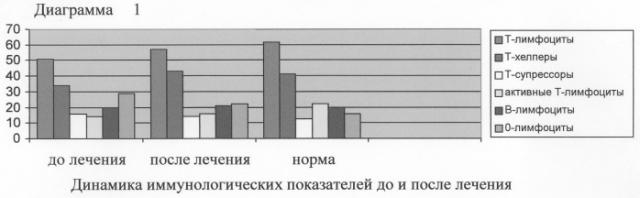
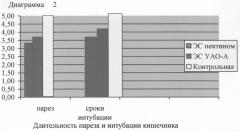
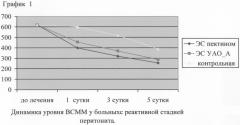
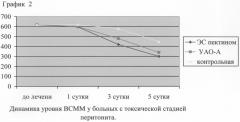
Сравнительная характеристика энтеросорбции ПСП и углеродным сорбентом УАО-А при лечении перитониального хирургического эндотоксикоза изложены в таблицах №№1-5 (стр.11-12), диаграммах 1, 2 (стр.13) и графиках 1-6 (стр.14, 15).
Полученные данные иллюстрируют большую эффективность предложенного способа по сравнению с прототипом и общепринятым способом лечения хирургического эндотоксикоза, в т.ч. на фоне энтеральной недостаточности.
| Таблица №1 | ||||
| Причины перитонита в группах обследованных больных. | ||||
| Причины Перитонита | Контроль n-50 | ЭСПСП n-60 | ЭС УАО-А n-40 | |
| Острый аппендицит | 16 (32%) | 9(15%) | 11(27,5%) | |
| Перфоративная язва желудка и 12-п. кишки. | 9(18%) | 13 (21,6%) | 10 (25%) | |
| Травма органов брюшной полости | 10 (20%) | 3 (5%) | 1 (2,5%) | |
| Острый холецистит | 3 (6%) | 6 (10%) | 3 (7,5%) | |
| Перфорация тонкой кишки | 1 (2%) | 1 (1,66%) | 1 (2,5%) | |
| Перфорация толстой кишки | 2 (4%) | 4 (6,6%) | 3 (7,5%) | |
| ОКН | 4 (6%) | 12 (20%) | 4 (10%) | |
| Послеоперационный перитонит | 2 (4%) | 3 (5%) | 2 (5%) | |
| Гнойные гинекологические заболевания | 1 (2%) | 1 (1,6%) | 1 (2,5%) | |
| Кишечные свищи | 1 (2%) | 5 (8,3%) | 2 (5%) | |
| Прочие | 1 (2%) | 3 (5%) | 2 (5%) | |
| Всего | 50 (100%) | 60 (100%) | 40 (100%) | |
| Таблица №2 | ||||
| Распределение больных по стадиям перитонита | ||||
| Стадии перитонита | Контроль n-50 | ЭСПСП n-60 | Группа с ЭС. УАО-А n-40 | Всего больных n-150 |
| Реактивная | 4 (8%) | 6(10,1%) | 4 ((10%) | 14(9,33%) |
| Токсическая | 43 (86%) | 50 (83,3%) | 35 (87,5%) | 128(85,3%) |
| Терминальная | 3 (6%) | 4 (6,6%) | 1 (2,5%) | 8 (5,33%) |
| Всего | 50 | 60 | 40 | 150 |
| Таблица №3 | |||||
| Характер содержимого брюшной полости у обследованных больных. | |||||
| Характер содержимого | Контроль n-50 | ЭСПСП n-60 | ЭС УАО-А n-40 | Всего n-150 | |
| Серозно-фибринозный | 10 (20%) | 6 (10%) | 8 (20%) | 24 (16%) | |
| Гнойно-фибринозный | 39 (78%) | 52 (86,6%) | 27 (62,5%) | 118 (78,66%) | |
| Желчный | - | 1 (1,66%) | 2 (5%) | 3 (2%) | |
| Каловый | 1 (2%) | 1 (1,66%) | 3 (7,5%) | 5 (3,33%) | |
| Таблица №4 | |||||
| Динамика тяжести состояния обследованных больных по SAPS. | |||||
| Сутки | Контрольная группа | ЭСПСП | ЭС УАО-А | ||
| 1-е | 7,9±0,43 | 7,8±0,54 | 8±0,54 | ||
| 2-е | 7,8±0,54 | 6,8±0,34 | 7,6±0,57 | ||
| 3-е | 7,1±0,76 | 5,9±0,65 | 6,7±0,27 | ||
| 4-е | 6,0±0,39 | 4,2±0,56 | 5,2±0,55 | ||
| 5-е | 5,1±0,21 | 3,4±0,76 | 4,2±0,89 | ||
| 6-е | 3,9±0,54 | 2,7±0,21 | 3,2±0,38 | ||
| 7-е | 2,4±0,87 | 1,9±0,11 | 2±0,87 | ||
| Таблица №5 | |||||
| Сравнительная летальность в разных стадиях перитонита* | |||||
| Токсическая стадия | |||||
| Контроль n-43 | ЭСПСП n-50 | ЭС УАО-А n-35 | |||
| Умерло | % | Умерло | % | Умерло | % |
| 4 | 8 | 1 | 1,6 | 4 | 10 |
| Терминальная стадия | |||||
| Контроль n-3 | ЭСПСП n-4 | ЭС УАО-А n-1 | |||
| умерло | % | умерло | % | Умерло | % |
| 3 | 6 | 3 | 5 | 1 | 2,5 |
| *В реактивной стадии перитонита смертей не было. |
1. Способ лечения хирургического эндотоксикоза с использованием назоинтестинальной декомпрессии через зонд, энтеросорбции и стимуляции моторики кишечника, отличающийся тем, что энтерально вводят гомогенизированную водную взвесь порошка столовой свеклы, изготовленного с применением сублимации.
2. Способ по п.1, отличающийся тем, что используется 20 г сухого вещества на 300 мл питьевой воды 18-22°С в виде гомогенной взвеси.
3. Способ по пп.1 и 2, отличающийся тем, что водную взвесь порошка вводят 3 раза в день курсом 3-5 дней.