Комплекс n,n-диэтилдитиокарбамата натрия с 2-этил-6-метил-3-гидроксипиридином, обладающий противоаллергической активностью
Иллюстрации
Показать всеИзобретение относится к новому комплексу N,N-диэтилдитиокарбамата с 2-этил-6-метил-3-гидроксипиридином формулы
который обладает противоаллергической активностью, что позволяет с его помощью осуществлять фармакологический контроль аллергической реакции за счет торможения функции клеток-мишеней аллергии. 2 ил., 1 табл.
Реферат
Изобретение относится к новым химическим соединениям, обладающим биологической активностью, и может быть использовано для создания фармакологических препаратов с противоаллергическим действием.
Современные представления о механизме развития аллергической реакции позволяют сделать вывод о том, что одним из важнейших факторов в формировании аллергического процесса является вовлечение в него тучных клеток слизистых оболочек и соединительной ткани, а также базофильных лейкоцитов периферической крови (Гущин И.С. "Аллергическое воспаление и его фармакологический контроль", М., Фармарус принт, 1998 г., стр.52-58) Соединение аллергена с антителом на поверхности именно этих клеток запускает механизм секреции медиаторов, которые вызывают патофизиологические изменения (сокращение гладкой мускулатуры, повышение сосудистой проницаемости, гиперсекрецию слизи из слизистых желез), составляющие основу клинических проявлений аллергии.
Установлено, что тучные клетки (ТК) и базофильные лейкоциты, являющиеся основными клетками - мишенями аллергии, вовлекаются в аллергические реакции посредством активации их функции. Поэтому становится все более актуальным направленный поиск новых соединений, способных воздействовать на функциональное состояние клеток - мишеней аллергии.
Известны препараты кромоглициевой кислоты и недокромила натрия (Гущин И.С. "Аллергическое воспаление и его фармакологический контроль", М., Фармарус принт, 1998 г., стр.216-222), противоаллергическую активность которых связывают со стабилизирующим действием на клетки - мишени аллергии. Однако это действие является довольно слабым и проявляется в экспериментальных условиях при высоких концентрациях этих соединений, не имеющих терапевтического значения.
Таким образом, технический результат, получаемый от реализации настоящего изобретения, состоит в создании новых химических соединений, обладающих противоаллергическим действием за счет торможения функции клеток - мишеней аллергии.
Указанный технический результат достигается комплексом N,N-диэтилдитиокарбамата натрия с 2-этил-6-метил-3-гидроксипиридином общей формулы:
обладающим противоаллергической активностью.
Комплексное соединение (аддукт) N,N-диэтилдитиокарбамата натрия с 2-этил-6-метил-3-гидроксипиридином является новым соединением и может быть получено в результате реакции комплексообразования N,N-диэтилдитиокарбамата натрия с 2-этил-6-метил-3-гидроксипиридином в эквимолярных соотношениях, проводимой в безводной среде в присутствии апротонного растворителя.
Образование комплексного соединения происходит за счет донорно-акцепторной связи, обусловленной электронноакцепторными свойствами замещенного 3-гидроксипиридина и высокой электроотрицательностью атомов серы в N,N-диэтилдитиокарбамате натрия.
В соответствии с изобретением обнаружено, что комплексное соединение (аддукт) N,N-диэтилдитиокарбамата натрия с 2-этил-б-метил-3-гидроксипиридином (КДДК) способно воздействовать на аллергический процесс путем подавления активации функций тучных клеток и базофильных лейкоцитов и проявляют тем самым противоаллергическую активность.
Комплексное соединение в соответствии с настоящим изобретением получают следующим образом.
В трехгорлую колбу, снабженную мешалкой, термометром и холодильником, загружают 3,14 г (0,02 Мол) N,N-диэтилдитиокарбамата натрия, приливают 60 мл абсолютного изопропилового спирта и 2 мл ацетона, после чего добавляют 2,76 г (0,02 Мол) 3-гидрокси-6-метил-2-этилпиридина при постоянном перемешивании до полного растворения компонентов. Далее полученный раствор перемешивают при 40° С в течение 3-х часов, затем фильтруют и отгоняют растворитель в вакууме. Полученный осадок перекристаллизовывают из абсолютного изопропилового спирта. Получают 4,25 г белого кристаллического продукта -
N,N-диэтилдитиокарбамато 3-гидрокси-6-метил-2-этилпиридина натрия.
Тпл=130-133° С. Растворим в воде, в спирте.
Найдено, %: С 43,11; Н 7,61; N 7,56; S 17,61.
Вычислено, %: С 43,07; Н 7,51; N 7,73; S 17,69.
ИК-спектр.усм-1: 1385 (S=C<); 1610 (С=С, аром.); 3380 (ОН). Изучение биологической активности соединения в соответствии с изобретением проведено с использованием метода определения высвобождения гистамина из тучных клеток крыс, метода высвобождения гистамина in vitro из базофилов периферической крови человека и метода пассивной кожной анафилаксии in vivo. Исследования предполагают предварительное исключение возможности изучаемого соединения взаимодействовать с реакцией определения гистамина и вызывать в пределах испытываемых концентраций высвобождение гистамина из тучных клеток и базофилов.
Физиологическая активность описываемого соединения показана на примерах 1-3.
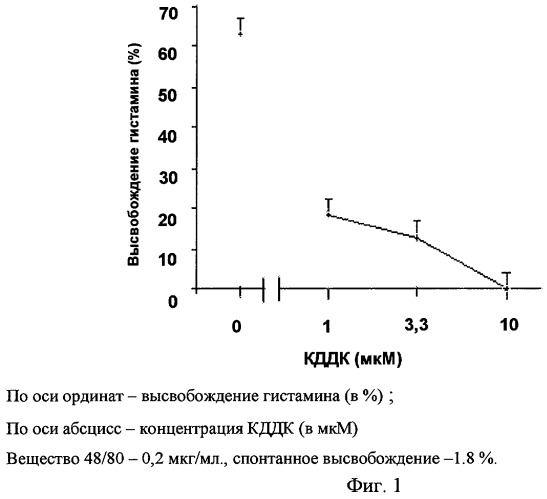
Пример 1. Определение высвобождения гистамина из тучных клеток крыс.
В испытаниях используют беспородных белых крыс-самцов массой 250-300 г.
Тучные клетки (ТК) крыс выделяют из брюшной и грудной полостей центрифугированием на градиенте плотности фикола. Содержание ТК в выделенной взвеси клеток составляло 85-95%. В ряд пробирок, содержащих по 2 мл солевого инкубирующего раствора, предварительно вносят испытуемое соединение в различных концентрациях. В контрольные пробирки испытуемое соединение не вносят. Пробирки выдерживают при температуре 37° С в течение
3 минут, после чего в них вносят по 5 мкл взвеси ТК и инкубируют в течение 20 мин. После инкубации к образцам клеток добавляют стандартный нецитотоксический высвободитель (вещество 48/80), который вызывает быструю активацию ТК, до конечных концентраций: 1 мкг/мл, 0,5 мкг/мл и 0,2 мкг/мл. Реакцию активации ТК останавливают перенесением пробирок на лед, после чего клетки осаждают центрифугированием при 400 g и 4° С в течение 10 мин. Надосадочную жидкость сливают в новые пробирки, клетки лизируют добавлением к осадкам 2 мл дистиллированной воды и встряхиванием на миксере Vortex. В надосадочных и осадочных пробах определяют содержание гистамина спектрофлуорометрическим методом.
Результаты исследований, представленные на Фиг.1 показывают, что КДДК заметно тормозит секрецию гистамина из ТК, вызванную веществом 48/80, а в концентрациях 10 мкМ наблюдается 100% тормозящий эффект.
Пример 2. Определение высвобождения гистамина из базофильных лейкоцитов периферической крови человека.
Для исследования используют кровь больных поллинозом с повышенной чувствительностью к пыльце злаковых трав и деревьев, установленной по предварительно проведенным кожным диагностическиим пробам с аллергеном. Отобирают материал от больных в возрасте от 15 до 34 лет со средней и тяжелой степенью проявления поллиноза в виде ринита, конъюктивита и бронхиальной астмы.
Из крови обследуемых больных по известной методике (Гущин И.С., Лесков В.П., Читаева В.Г., Полсачева В., ж. Иммунология, 1982, №4, с.67-71) получают взвесь мононуклеарньх клеток, содержащих 2-4% базофилов, и готовят пробы с исследуемыми соединениями в концентрациях 10 мкМ, 100 мкМ и 1 мМ. Аллергены (пыльцу трав, деревьев или домашнюю пыль) применяют в диапазоне концентраций от 0,1-10,0 PNU/m1.
В качестве контрольных используют образцы без добавления испытываемого соединения.
Приготовленные образцы инкубируют в течение 40 минут при температуре 37° С, после чего вносят аллерген и продолжают инкубацию клеток в тех же условиях еще 40 мин. Высвобождение гистамина определяют микроспектрофлуорометрическим методом в осадочных порциях без предварительной экстракции и выражают в процентах к общему содержанию гистамина в порции клеток.
Обнаружено, что КДДК подавляет активацию клеток-мишеней человека - базофилов.
Данные, приведенные в таблице 1, свидетельствуют о том что, исследуемое соединение в зависимости от концентрации оказывает четкий угнетающий эффект.
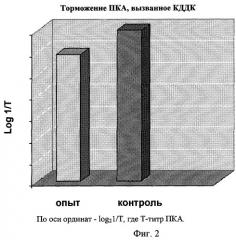
Пример 4. Изучение пассивной кожной анафилаксии (ПКА).
Исследования проводят на беспородных крысах-самцах массой тела 210-240 г.
Реакцию ПКА воспроизводят описанным ранее методом [Levin В.В., Vaz N. М. Int. Arch. Allergy. 1970, р.39-196].
Исследуемое соединение предварительно разводят в количестве 100 мг в 10 мл физиологического раствора и вводят животным внутрибрюшинно в дозе 100 мг на 1 кг массы тела испытуемого животного за 30 мин до внутривенной инъекции разрешающей дозы антигена (овальбумина). В качестве контрольных используют животных, которым вводят 0,9% раствор NaCl.
Результаты оценивают по пороговой кожной реакции, видимой на внутренней стороне кожи. За пороговую реакцию принимают то наибольшее разведение (титр) антиовальбуминовой сыворотки крови, при котором еще возникает прокрашивание кожи.
Графики, представленные на Фиг.2, иллюстрируют снижение титра реакции ПКА при ее воспроизведении на крысах, получивших описываемое соединение.
Таким образом, новое соединение обладает противоаллергической активностью и может быть использовано при разработке новых препаратов для фармакологического контроля аллергической реакции, а, следовательно, является потенциальным противоаллергическим средством.
| Таблица 1Торможение КДДК секреции гистамина из базофилов боль поллинозом, вызванной специфическим аллергеном. | ||||
| Соединение | Высвобождение гистамина без ингибитора (%) | Торможение секреции гистамина в зависимости от концентрации ингибитора (%) | ||
| 1 мкМ | 10 мкМ | 100 мкМ | ||
| КДДК n=11 | 54,22±2,38 | 24,96±2,71* * | 38,27±2,75* * | 100* * |
| Примечание: Торможение выражено в процентах угнетения исходной реакции на аллерген.Приведены значения М±m. n - число опытов. * -р<0,05; ** -р<0,01 в сравнении с соответствующим предшествующим показателем |
Комплекс N,N-диэтилдитиокарбамата натрия с 2-этил-6-метил-3-гидроксипиридином общей формулы:
обладающий противоаллергической активностью.