Способ анализа образца меченого органического соединения методом высокоэффективной жидкостной хроматографии
Иллюстрации
Показать всеИспользование: в аналитической органической химии, биологической химии, медицине. При анализе образца меченого органического соединения методом ВЭЖХ вычерчивают пару хроматограмм: по радиоактивности (№1) и УФ-поглощению (№2) или по радиоактивности (№1), флуоресценции (№2), а также хроматограмму удельной относительно УФ-поглощения (№3) или относительно флуоресценции (№3). Качество анализируемого образца оценивают тем более высоким, чем ближе форма пика анализируемого меченого соединения на третьей хроматограмме к форме трапеции. Способ позволяет повысить точность оценки качества образца анализируемого меченого соединения. 8 ил.
Реферат
Изобретение относится к аналитической органической химии и может найти применение в биологической химии и медицине.
Известен способ анализа образца меченого органического соединения методом высокоэффективной жидкостной хроматографии (ВЭЖХ) путем вычерчивания пары хроматограмм с использованием двух детекторов: по радиоактивности и по УФ-поглощению или по радиоактивности и по флуоресценции и последующего определения качеств меченого образца по результатам визуальной оценки характера пиков анализируемого соединения на хроматограммах (Патент RU №2183123, кл. G 01 N 33/74, опубл. 10.06.2001 г.)
Однако точность определения чистоты анализируемого образца меченого органического соединения при использовании данного известного способа невысокая.
Техническим результатом, достигаемым настоящим изобретением, является повышение точности определения чистоты образца анализируемого меченого соединения.
Указанный технический результат достигается тем, что в способе анализа образца меченого органического соединения методом высокоэффективной жидкостной хроматографии путем вычерчивания пары хроматограмм с использованием двух детекторов: по радиоактивности и по УФ-поглощению или по радиоактивности и по флуоресценции и последующего определения качества анализируемого образца по результатам визуальной оценки характера пиков меченого соединения на хроматограммах отличительной особенностью является то, что дополнительно вычерчивают хроматограмму удельной радиоактивности относительно УФ-поглощения или хроматограмму удельной радиоактивности относительно флуоресценции, а качество анализируемого образца меченого соединения оценивают тем более высоким, чем ближе форма пика меченого соединения на дополнительной хроматограмме к форме трапеции.
При анализе образцов меченых органических соединений методом ВЭЖХ их чистоту принято оценивать тем более высокой, чем “аккуратнее” пик, образуемый ими на хроматограмме. Однако последующее применение количественных методов анализа образца, степень чистоты которого оценена методом ВЭЖХ как высокая, показывает ошибочность такого вывода.
Собственные исследования показали, что результаты анализа образцов меченых органических соединений можно сделать более информативными и достоверными, если в процессе ВЭЖХ вычерчивать не только хроматограмму их радиоактивности и хроматограмму их УФ-поглощения или хроматограмму радиоактивности в сочетании с хроматограммой флуоресценции, но дополнительно вычерчивать третью хроматограмму - хроматограмму удельной радиоактивности относительно УФ-поглощения исследуемого соединения или относительно его флуоресценции.
При высокой чистоте образца в процессе выхода меченого соединения, анализируемого методом ВЭЖХ, величина отношения его радиоактивности к его УФ-поглощению или к его флуоресценции остается постоянной и поэтому кривая в области пика приобретает форму, близкую к трапеции. Если удельная радиоактивность изменяется по мере выхода анализируемого соединения, то это свидетельствует о недостаточной чистоте исследуемого образца.
На фиг.1 изображен общий вид установки, применяемой для анализа образца меченого соединения способом согласно изобретению.
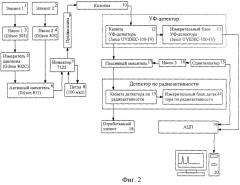
На фиг.2 дана схема установки, изображенной на фиг.1.
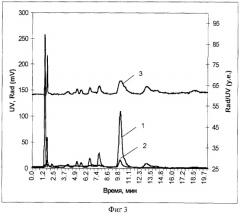
На фиг.3 представлены хроматограммы реакционной смеси при синтезе меченой арахидоновой кислоты. Колонка: Kromasil 100C18(4×150 мм) 7 мкм. Элюент: 20% метанол - 50 мМ аммоний-фосфатный буфер (рН 2,8).
1 - хроматограмма радиоактивности;
2 - хроматограмма УФ-поглощения;
3 - хроматограмма радиоактивности относительно УФ-поглощения.
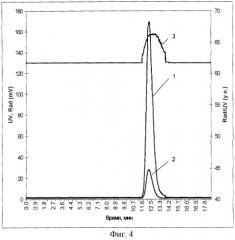
На фиг.4 представлены хроматограммы образца меченой арахидоновой кислоты после его выделения и очистки (после препаративной HPLC). Колонка: Kroinasil 100С18(4×150 мм) 7 мкм. Элюент: 15% метанол - 50 мМ аммонийфосфатный буфер (рН 2,8).
1 - хроматограмма радиоактивности;
2 - хроматограмма УФ-поглощения;
3 - хроматограмма удельной радиоактивности относительно УФ-поглощения.
На фиг.5 представлена хроматограмма образца меченого оланзапина после его очистки (после препаративной HPLC). Колонка: Kromasil 100C18(4×150 мм) 7 мкм. Элюент: ацетонитрил-вода(1:5)+0,1% трифторуксусной кислоты.
1 - хроматограмма радиоактивности;
2 - хроматограмма УФ-поглощения;
3 - хроматограмма удельной радиоактивности относительно УФ-поглощения.
На фиг.6 представлена хроматограмма образца меченого оланзапина после его повторной очистки (после повторной препаративной HPLC). Колонка: Kromasil 100C18(4×150 мм) 7 мкм. Элюент: ацетонитрил-вода(1,5)+0,1% трифторуксусной кислоты.
1 - хроматограмма радиоактивности;
2 - хроматограмма УФ-поглощения;
3 - хроматограмма удельной радиоактивности относительно УФ-поглощения;
На фиг.7 представлена хроматограмма образца дансильного производного, меченного тритием пролина. Колонка: Kromasil 100С18(4×150 мм) 7 мкм. Элюент: метанол - 50 мМ аммонийфосфатный буфер (рН 2.8) (65:35).
1 - хроматограмма радиоактивности;
2 - хроматограмма флуоресценции;
3 - хроматограмма удельной радиоактивности относительно флуоресценции.
На фиг.8 представлена хроматограмма образца дансильного производного, меченнoго тритием пролина после аналитической очистки (аналитической HPLC). Колонка: Kromasil 100С18(4×150 мм) 7 мкм. Элюент: метанол - 50 мM аммонийфосфатный буфер (рН 2.8) (65:35),
1 - хроматограмма радиоактивности;
2 - хроматограмма флуоресценции;
3 - хроматограмма удельной радиоактивности относительно флуоресценции.
Для осуществления способа согласно изобретению удобно использовать установку, общий вид которой и ее схема представлены соответственно на фиг.1 и 2. Установка состоит из двух сосудов (1, 2) с элюентами, управляющего насоса Gilson 305 (3), ведомого насоса Gilson 303 (4), манометрического модуля (измерителя давления) Gilson 802C (5), активного смесителя Gilson 811 (6), инжектора 7125 (7) с петлей (8), предколонки (9), колонки (10), УФ-детектора Jasco UVIDEC-100-1V, состоящего из измерительного блока (11) и кюветы (12), детектора по радиоактивности, состоящего из кюветы (13) и измерительного блока (блока счета) (14), сцинтиллятора (сосуда со сцинтилляционной жидкостью) (15), насоса для подачи сцинтилляционной жидкости (16), смесителя (17), сосуда для сбора отработанного элюента (18), аналого-цифрового преобразователя (19) и компьютера (20). Вместо УФ-детектора можно использовать детектор по флуоресценции.
Для проведения анализа на такой установке элюенты из сосудов 1 и 2 подаются насосами 3 и 4 под управлением насоса 3 и по заданной программе при контроле давления в системе с помощью измерителя давления 5 смешиваются в активном смесителе 6. Из него смесь элюентов подается в инжектор 7 с петлей 8, где в поток элюентов вводится анализируемая проба. Затем приготовленная смесь проходит через предколонку 9 и колонку 10 и поступает в измерительный блок 11 УФ-детектора (или детектора по флуоресценции) в его кювету 12. Далее проба поступает в кювету 13 детектора по радиоактивности с измерительным блоком 14. Предварительно пробу смешивают со сцинтилляционной жидкостью, которую подают из сцинтиллятора 15 насосом 16 в пассивный смеситель 17. Отработанный элюент сбрасывают в сосуд 18. Информацию с детекторов по УФ-поглощению (или по флуоресценции) и по радиоактивности обрабатывают в аналого-цифровом преобразователе 19 на компьютере 20 с использованием программы Мультихром для Windows. На дисплее компьютера получают две пары хроматограмм: по радиоактивности и по УФ-поглощению или по радиоактивности и флуоресценции. Кроме того, на дисплее компьютера наблюдают хроматограмму удельной радиоактивности относительно УФ-поглощения или хроматограмму удельной радиоактивности относительно флуоресценции, по которой судят о качестве анализируемого образца меченого органического соединения.
Ниже приведены примеры, иллюстрирующие изобретение.
Пример 1. Определение чистоты меченной тритием арахидоновой кислоты. Реакционную смесь анализировали методом ВЭЖХ, колонка Kromasil 100С18(4×150 мм) 7 мкм, элюент: 20% метанол – 50 мМ аммонийфосфатный буфер (рН 2,8). Представленные на фиг.3 хроматограммы свидетельствуют о низкой чистоте анализируемого образца. Пик арахидоновой кислоты на хроматограмме 3 удельной радиоактивности УФ-поглощения имеет форму треугольника (время выхода 9,4-10,8). Выделенный образец меченной тритием арахидоновой кислоты подвергли препаративной очистке (препаративной HPLC). Результаты анализа полученного очищенного образца представлены на фиг.4. Колонка Kromasil 100C18(4×150 мм) 7 мкм. Элюент: 15% метанол - 50 мМ аммонийфосфатный буфер (рН 2,8). Пик меченной тритием арахидоновой кислоты на хроматограмме удельной радиоактивности относительно УФ-поглощения приближается к трапециевидной форме, это свидетельствует о повышении степени очистки анализируемого образца.
Пример 2. Определение чистоты меченного тритием оланзапина. Образец меченного тритием оланзапина анализировали способом согласно изобретению после препаративной HPLC. Колонка: Kromasil 100С18(4×150 мм) 7 мкм. Элюент: ацетонитрил-вода (5:1)+0,1% трифторуксусной кислоты. Анализ кривых на фиг.5 свидетельствует о приближении формы пика на хроматограмме удельной радиоактивности относительно УФ-поглощения к трапециевидной форме.
После повторной очистки форма пика (см.фиг.6) свидетельствует о высокой чистоте анализируемого образца.
Пример 3. Определение чистоты дансильного производного меченного тритием пролина. Реакционную смесь анализировали методом ВЭЖХ, колонка Kromasil 100C18(4×150 мм) 7 мкм. Элюент: метанол - 50 мМ аммонийфосфатный буфер (рН2.8) (65:35). Представленные на фиг.7 хроматограммы свидетельствуют о низкой чистоте анализируемого образца. Пик дансильного производного меченого тритием пролина на хроматограмме удельной радиоактивности относительно флуоресценции имеет форму треугольника (время выхода ~7 мин). Выделенный образец дансильного производного меченого тритием пролина подвергли аналитической очистке (аналитической HPLC). Результаты анализа полученного очищенного образца представлены на фиг.8. Колонка: Kromasil 100C18(4×150 мм) 7 мкм. Элюент: метанол - 50 мМ аммонийфосфатный буфер (рН 2.8) (65:35). Соотношение пиков радиоактивности и флуоресценции становится постоянным, это свидетельствует о повышении степени очистки анализируемого образца.
Таким образом, способ согласно изобретению позволяет повысить точность оценки качества образца меченого соединения, анализируемого методом ВЭЖХ.
Способ анализа образца меченого органического соединения методом высокоэффективной жидкостной хроматографии путем вычерчивания пары хроматограмм с использованием двух детекторов: по радиоактивности и УФ-поглощению или по радиоактивности и флуоресценции и последующего определения качества анализируемого образца по результатам визуальной оценки характера пиков меченого соединения на хроматограммах, отличающийся тем, что дополнительно вычерчивают хроматограмму удельной радиоактивности относительно УФ-поглощения или хроматограмму удельной радиоактивности относительно флуоресценции, а качество анализируемого образца оценивают тем более высоким, чем ближе форма пика меченого соединения на дополнительной хроматограмме к форме трапеции.