Производные бензола, способы их получения и содержащие их фармацевтические композиции
Иллюстрации
Показать всеИзобретение относится к новым производным бензола формулы (I),
где А представляет собой группу, выбранную из следующих: -С≡С-, -СН=СН-; -СН2-СН2-; n равно 1 или 2; Х представляет собой атом водорода, хлора или фтора, или метильную, или метоксигруппу; Y представляет собой атом водорода, или атом хлора, или фтора; R1 представляет собой циклогексильную группу, монозамещенную, дизамещенную, тризамещенную или тетразамещенную метильной группой; фенильную группу, монозамещенную или дизамещенную атомом фтора или хлора или метоксигруппой; циклогептильную, трет-бутильную, дициклопропилметильную, 4-тетрагидропиранильную или 1- или 2-адамантильную или адамантан-2-ольную группу; либо R1 представляет собой фенильную группу, причем в этом случае Х и Y оба представляют собой атом хлора; r2 представляет собой атом водорода или (С1-С4)алкильную группу; r3 представляет собой (С5-С7)циклоалкил; и соли этих соединений, образованные присоединением фармацевтически приемлемых кислот, а также их сольваты и гидраты. Изобретение также относится к способам получения соединений формулы (I) и к фармацевтической композиции, способной взаимодействовать с рецепторами сигма-2, на основе этих соединений. Технический результат – получение новых соединений и лекарственных продуктов на их основе в целях лечения аутоиммунных состояний, нарушений частоты сердечных сокращений и борьбы с пролиферацией опухолевых клеток. 8 н. и 10 з.п. ф-лы, 14 табл.
Реферат
Настоящее изобретение относится к производным бензола, содержащим аминную функциональную группу, замещенным алкильной группой и циклоалкильной группой, которые специфически связываются с сигма-рецепторами, в частности с рецепторами периферической нервной системы, к способу получения этих соединений и к их использованию в фармацевтических композициях и, более конкретно, в качестве иммунодепрессантов.
Сигма-рецепторы были выявлены с помощью нескольких лигандов. Прежде всего, можно упомянуть об опиатных соединениях - 6,7-бензоморфанах или SKF-10047 -, в частности о хиральном соединении (+) SKF-10047 (W.R. Martin et al., J. Pharmacol. Exp. Ther. 1976, 197, 517-532; B.R. Martin et al., J. Pharmacol. Exp. Ther. 1984, 231, 539-544). Из этих соединений наиболее часто используют (+)N-аллилнорметазоцин, или (+)NAHM, и (+)пентазоцин. Нейролептический агент галоперидол также является лигандом сигма-рецепторов, как и (+)3-(3-гидроксифенил)-1-пропилпиперидин и (+)3-РРР (В. L. Largent et al., Proc. Nat. Acad. Sci. USA 1984, 81, 4983-4987).
В патенте США 4709094 описаны производные гуанидина, которые являются высокоактивными лигандами, которые специфичны в отношении сигма-рецепторов, и можно упомянуть, в частности, ди-(O-толил)гуанидин, или DTG. Анатомическое распределение сигма-рецепторов в мозге было установлено посредством ауторадиографии после мечения этих рецепторов DTG согласно Е. Weber et al., Proc. Nat. Acad. Sci. USA 1986, 83, 8784-8788, а также лигандами (+)SKF-10047 и (+)3-РРР согласно В. L. Largent et al., J. Pharmacol. Exp. Ther. USA 1986, 238, 739-748. Ауторадиографическое исследование дало возможность четко идентифицировать сигма-рецепторы головного мозга и отличать их от других опиатных рецепторов, а также от фенциклидиновых рецепторов. В частности, сигма-рецепторы распределены в центральной нервной системе и сконцентрированы в стволе головного мозга, лимбической системе и областях, вовлеченных в регуляцию эмоций. Сигма-рецепторы также обнаружены в различных периферических тканях. Различают по меньшей мере два типа сигма-рецепторов: рецепторы сигма-1 и сигма-2. Лиганды типа (+)SKF-10047 избирательно связываются с рецепторами сигма-1, тогда как другие лиганды, такие как DTG, галоперидол или (+)3-РРР демонстрируют значительную аффинность в отношении как сигма-1, так и сигма-2 рецепторов.
В патенте ЕР 461986 описаны соединения формулы
которые избирательно связываются с сигма-рецепторами и которые обладают иммунодепрессивной активностью.
В этом ряду соединений исследован конкретно гидрохлорид (Z)-[3-(3-хлор-4-циклогексилфенил)аллил]циклогексилэтиламина формулы
Можно сослаться, например, на Biological Chemistry. 1997, 272 (43), 27107-27115; Immunopharmacology and Immunotoxicology. 1996, 18 (2), 179-191. Однако соединения формулы (А) обладают специфическим свойством, которое можно рассматривать как недостаток. Этим свойством, которое проявляется во время метаболизации, является зависимость от цитохрома, известного как CYP 2D6.
В 1957 году впервые было высказано предположение, что наследственные различия могут быть ответственны за вариации ответной реакции на лекарственные продукты. Окислительный метаболизм демонстрирует значительные вариации между индивидуумами и расами. Исследование, которое проводилось в течение последних 15 лет, показало, что вариации функциональной экспрессии мультигенного семейства цитохрома Р450 (CYP) являются причиной этих различий. Лишь некоторые изоформы цитохрома Р450 из тех, которые уже определены у человека, участвуют в окислительном метаболизме лекарственных продуктов (Xenobiotica, 1986, 16, 367-378). К настоящему времени на основе их клинической важности идентифицированы CYP 1A2, CYP 2A6, CYP 2C9, CYP 2D6, CYP 2C19, CYP 2E1 и CYP 3A4. Установлено, что CYP 3A4, CYP 2D6 и CYP 2C9 сами ответственны (и в различной степени) за 90% окислительного метаболизма лекарственных продуктов. Хотя функциональная экспрессия этих изоформ регулируется и находится под влиянием целого ряда экологических и физиологических факторов, генетические факторы оказывают наиболее явно выраженное влияние, которое подчеркивает важную роль полиморфизма в окислении лекарственных продуктов. Некоторые из этих полиморфизмов были изучены (в частности, полиморфизмы CYP 2C19 и CYP 2D6). Более конкретно, была продемонстрирована клиническая важность полиморфизма CYP 2D6 в 4-гидроксилировании дебризохина (Clin. Pharmacol. Ther., 1991, 50, 233-238). Генетический полиморфизм CYP 2D6 ответственен за проблематичный метаболизм более чем 30 важных лекарственных продуктов и оказывает влияние на вплоть до 10% кавказского населения (медленные метаболисты). В настоящее время показано, что эта изоформа контролирует биотрансформацию лекарственных продуктов, таких как антиаритмические агенты, β-блокаторы, антигипертензивные агенты, агенты против стенокардии, нейролептики и антидепрессанты. За некоторым исключением, эти лекарственные продукты применяют в психиатрии и сердечно-сосудистой терапии для долгосрочного лечения.
Фармакокинетические результаты являются результатами сугубо количественного порядка: медленно метаболизирующие индивидуумы имеют уровень неизмененного продукта, который выше, чем у остальных. Эти количественные различия оказывают существенное клиническое воздействие на молекулы, которые имеют низкий терапевтический индекс.
Таким образом, генетика в значительной степени оказывает влияние на различия в эффективности и побочных эффектах, наблюдаемых среди индивидуумов. Поэтому важно определить, может ли метаболизм лекарственного продукта быть изменен в случае генетического дефицита фермента или нет.
В соответствии с настоящим изобретением обнаружены новые превосходные бензольные производные для сигма-рецепторов, в частности для сигма-рецепторов периферической нервной системы, которые обладают иммунодепрессивной активностью, но имеют низкую скорость метаболизма и/или небольшую степень или отсутствие вовлечения CYP 2D6 в окислительный процесс.
Соединения по данному изобретению также обладают противоопухолевой активностью и, в частности, они ингибируют пролиферацию раковых клеток.
Более того, продемонстрировано, что эти новые соединения обладают активностью в сердечно-сосудистой системе, более конкретно в контролировании частоты сердечных сокращений.
Соединения по данному изобретению также обладают активностью в отношении апоптоза.
Так, в одном из своих аспектов настоящее изобретение относится к соединениям формулы
где А представляет собой группу, выбранную из следующих: -С≡С-, -СН=СН-; -СН2-СН2-;
n равно 1 или 2;
Х представляет собой атом водорода, хлора или фтора или метильную или метоксигруппу;
Y представляет собой атом водорода или атом хлора или фтора;
R1 представляет собой циклогексильную группу, монозамещенную, дизамещенную, тризамещенную или тетразамещенную метильной группой; фенильную группу, монозамещенную или дизамещенную атомом фтора или хлора или метоксигруппой; циклогептильную, трет-бутильную, дициклопропилметильную, бицикло[3.2.1]октанильную, 4-тетрагидропиранильную, 4-тетрагидротиопиранильную или 1-или 2-адамантильную или адамантан-2-ольную группу; либо R1 представляет собой фенильную группу, причем понятно, что в этом случае Х и Y иные, чем водород;
R2 представляет собой атом водорода или (С1-С4)алкильную группу, возможно замещенную трифторметильной группой;
R3 представляет собой (С5-С7)циклоалкил;
и солям этих соединений, образованным присоединением фармацевтически приемлемых кислот, а также их сольватам и гидратам.
Термин "алкил" означает линейный или разветвленный насыщенный углеводородный одновалентный радикал.
Термин "(С1-С4)алкил" означает алкильный радикал, включающий в себя от 1 до 4 атомов углерода.
В соответствии с еще одним аспектом данное изобретение относится к соединениям формулы (I), где А представляет собой группу, выбранную из следующих: -С≡С-, -СН=СН-, -СН2-СН2-;
n равно 1 или 2;
Х представляет собой атом водорода, хлора или фтора или метильную или метоксигруппу;
Y представляет собой атом водорода или атом хлора или фтора;
R1 представляет собой циклогексильную группу, монозамещенную, дизамещенную, тризамещенную или тетразамещенную метильной группой; фенильную группу, монозамещенную или дизамещенную атомом фтора или хлора или метоксигруппой; цикпогептильную, трет-бутильную, дициклопропилметильную, бицикло[3.2.1]октанильную, 4-тетрагидропиранильную, 4-тетрагидротиопиранильную или 1-или 2-адамантильную группу; либо R1 представляет собой фенильную группу, причем понятно, что в этом случае Х и Y иные, чем водород;
R2 представляет собой (С1-С4)алкильную группу, возможно замещенную трифторметильной группой;
R3 представляет собой (С5-С7)циклоалкил;
и солям этих соединений, образованным присоединением фармацевтически приемлемых кислот, а также их сольватам и гидратам.
В соответствии с еще одним аспектом данное изобретение относится к соединениям формулы
где А представляет собой группу, выбранную из следующих: -С≡С-, -СН=СН-, -СН2-СН2-;
Х представляет собой атом водорода или хлора;
Y представляет собой атом водорода или атом хлора;
R1 представляет собой циклогексил, монозамещенный, дизамещенный, тризамещенный или тетразамещенный метильной группой; фенильную группу, замещенную атомом хлора, метоксигруппой или одним или двумя атомами фтора; трет-бутильную или 1-или 2-адамантильную группу; либо R1 представляет собой фенильную группу, причем понятно, что в этом случае Х и Y оба представляют собой атом хлора;
R2 представляет собой (С2-С3)алкил;
и солям этих соединений, образованным присоединением фармацевтически приемлемых кислот, а также их сольватам и гидратам.
В соответствии с еще одним аспектом данное изобретение относится к соединениям формулы (I) и (I.1), в которых А представляет собой группу -СН=СН-в (Z) конфигурации, и солям этих соединений, образованным присоединением фармацевтически приемлемых кислот, а также их сольватам и гидратам. В соответствии с еще одним аспектом данное изобретение относится к соединениям, как они определены выше, в которых Х представляет собой атом хлора, а Y представляет собой атом водорода или хлора, и солям этих соединений, образованным присоединением фармацевтически приемлемых кислот, а также их сольватам и гидратам.
В соответствии с еще одним аспектом данное изобретение относится к соединениям, как они определены выше, в которых R1 представляет собой 3,3,5,5-тетраметилциклогексильную, или 3,3-диметилциклогексильную, или 4,4-диметилциклогексильную группу; фенильную группу, монозамещенную или дизамещенную атомом фтора, или замещенную в положении 4 атомом хлора; или 1-или 2-адамантильную группу; и солям этих соединений, образованным присоединением фармацевтически приемлемых кислот, а также их сольватам и гидратам.
Следующие соединения:
[(Z)-3-(4-адамантан-2-ил-3-хлорфенил)пропен-2-ил]циклогексилэтиламин;
[(Z)-3-(4-адамантан-2-илфенил)пропен-2-ил]циклогексилэтиламин;
{(Z)-3-[4-(4,4-диметилциклогексил)-2-хлорфенил]пропен-2-ил}-циклогексилэтиламин;
[(Z)-3-(4-адамантан-1-ил-3-хлорфенил)пропен-2-ил]циклогексилэтиламин;
[(Z)-3-(4-адамантан-2-ил-3,5-дихлорфенил)пропен-2-ил]циклогексилэтиламин;
[(Z)-3-(4-адамантан-2-ил-3,5-дихлорфенил)пропен-2-ил]циклогексил(2-метилэтил)амин;
а также их соли, образованные присоединением фармацевтически приемлемых кислот, их сольваты и гидраты составляют еще один аспект данного изобретения.
В частности, данное изобретение относится к [(Z)-3-(4-адамантан-2-ил-3,5-дихлорфенил)пропен-2-ил]циклогексилэтиламину, а также его солям, образованным присоединением фармацевтически приемлемых кислот, сольватам и гидратам.
Соли соединений по данному изобретению получают по методикам, хорошо известным специалистам в данной области техники.
Соли соединений формулы (I) по настоящему изобретению включают соли с неорганическими или органическими кислотами, которые дают возможность разделения или подходящей кристаллизации соединений формулы (I), а также фармацевтически приемлемых солей.
Подходящими кислотами, которые могут быть упомянуты, являются пикриновая кислота, щавелевая кислота или оптически активная кислота, например винная кислота, дибензоилвинная кислота, миндальная кислота или камфорсульфоновая кислота и кислоты, которые образуют физиологически приемлемые соли, такие как гидрохлорид, гидробромид, сульфат, гидросульфат, дигидрофосфат, малеат, фумарат, 2-нафталинсульфонат или пара-толуолсульфонат. Гидрохлориды являются наиболее предпочтительными из солей соединений формулы (I). В том случае, когда соединение по данному изобретению содержит один или более чем один асимметрический атом углерода, оптические изомеры этого соединения составляют неотъемлемую часть данного изобретения. Если соединение по данному изобретению проявляет стереоизомерию, например аксиально-экваториального типа или Z-E типа, то данное изобретение включает в себя все стереоизомеры данного соединения.
Настоящее изобретение включает в себя соединения формулы (I) в форме чистых изомеров, а также в форме смеси изомеров в любом соотношении. Соединения (I) выделяют в форме чистых изомеров традиционными способами разделения. Например, можно использовать фракционную перекристаллизацию соли рацемической смеси с оптически активной кислотой или основанием, принцип которой хорошо известен, или стандартные хроматографические способы на хиральной стационарной фазе или нехиральной стационарной фазе; например, можно использовать разделение на силикагеле или C18-привитом силикагеле, элюируя смесями, такими как хлорированные растворители/спирт. Вышеупомянутые соединения формулы (I) включают также соединения, в которых один или более чем атом водорода, углерода или галогена, в частности хлора или фтора, заменены их радиоактивным изотопом, например тритием или углеродом-14. Такие меченые соединения пригодны для исследований метаболизма или фармакокинетики в биохимических тестах в качестве лигандов рецептора.
Функциональные группы, которые могут находиться в молекуле соединений формулы (I) и в промежуточных соединениях, могут быть защищены, перманентно или временно, защитными группами, которые обеспечивают окончательный синтез ожидаемых соединений. Реакции введения и удаления защитных групп осуществляют способами, хорошо известными специалистам в данной области техники. Выражение "временная защитная группа для аминов, спиртов, фенолтиолов или карбоновых кислот" означает защитные группы, такие как группы, описанные в Protective Groups in Organic Synthesis, Greene T. W. and Wuts P. G. M., ed. John Willey and Sons, 1991 и в Protecting Groups, Kocienski P. J., 1994, Georg Thieme Verlag. Специалист в состоянии выбрать подходящие защитные группы. Соединения формулы (I) могут содержать группы-предшественники других функциональных групп, которые последовательно образуются на одной или более чем одной стадии.
Объектом настоящего изобретения также является способ получения соединений формулы (I), отличающийся тем, что:
1) когда А представляет собой группу -C≡C-,
а) либо, если n=1, проводят реакцию Манниха между фенилацетиленовым производным формулы
где R1, Х и Y являются такими, как определено для (I), формальдегидом и амином (1) HNR2R3, причем R2 и R3 являются такими, как определено для (I);
б) либо проводят реакцию сочетания Сузуки между соединением формулы
где X, Y, n, R2 и R3 являются такими, как определено для (I), a Z представляет собой бром, йод или трифторметансульфонатную группу (OTf), и производным бора (2) формулы R1-B(OR)2, где R представляет собой атом водорода или алкильную или арильную группу, в присутствии основания и металлического катализатора;
в) либо, когда R1 представляет собой циклогексильную группу, монозамещенную, дизамещенную, тризамещенную или тетразамещенную метильной группой; циклогептильную, 4-тетрагидропиранильную, 4-тетрагидротиопиранильную или адамантильную группу, проводят реакцию сочетания между соединением (1а), в котором Z представляет собой атом йода или брома, и кетоном (3), соответствующим R1, представленным в присутствии основания с получением промежуточного соединения формулы
где X, Y, n, R2 и R3 являются такими, как определено для (I); указанное соединение (I’) затем восстанавливают в селективных условиях;
г) либо проводят реакцию сочетания между амином формулы
где n, R2 и R3 являются такими, как определено для (I), и соединением формулы
где R1, Х и Y являются такими, как определено для (I), а Z представляет собой атом брома или йода или трифторметилсульфонатную группу (трифлат, или OTf);
2) когда А представляет собой группу -СН=СН-, проводят гидрирование, водородом в момент выделения или в присутствии циклогексена, соединения формулы (I), где А представляет собой ацетиленовую группу -С≡С-, с получением этиленового соединения (I) в форме смеси Z и Е изомеров, либо это гидрирование проводят в присутствии металлического катализатора на носителе с получением этиленового соединения (I) в Z форме, либо, альтернативно, соединение (I), в котором А представляет собой ацетиленовую группу -С≡С-, подвергают взаимодействию с гидридом металла с получением этиленового соединения (I) в Е форме;
3) когда А представляет собой группу –СН2-СН2-, проводят гидрирование соединения (I), в котором А представляет собой группу -СН=СН-или -C≡C-.
Стадию 1а способа по изобретению проводят при нагревании, предпочтительно при температуре между 80°С и 90°С, в полярном растворителе, таком как 1,2-диметоксиэтан или 1,4-диоксан. Чтобы способствовать реакции конденсации, можно использовать катализатор, например металлическую соль, такую как хлорид меди II или хлорид меди III.
На стадии 1б данного способа реакцию сочетания Сузуки предпочтительно проводят между соединением (Ia), в котором Z представляет собой OTf, и производным бора (2) формулы R1-B(OH)2. Реакцию проводят в присутствии основания, такого как гидроксид, алкоксид, фосфат или карбонат щелочного или щелочно-земельного металла, более конкретно фосфат калия или карбонат натрия. Реакцию проводят в присутствии металлического катализатора, например катализатора на основе меди, олова или, предпочтительно, палладия, такого как тетракис(трифенилфосфин)палладий, возможно с использованием галогенида, такого как хлорид лития, действующего как сокатализатор. Способ осуществляют при нагревании при температуре между 60°С и 80°С в инертном растворителе, таком как толуол или 1,2-диметоксиэтан, или, предпочтительно, в двухфазной среде толуольный/водный раствор, возможно с долей спирта, такого как этанол. Реакция сочетания Сузуки исследована во многих публикациях, таких как, например, Synth. Commun., 1981, 11 (7), 513-519 и J. Org. Chem., 1993, 58 (8), 2201-2208. Бороновые кислоты (2) R1-B(OH)2 имеются в продаже или их синтезируют стандартным способом из соответствующих галогенопроизводных, предпочтительно бромопроизводных R1Br, путем воздействия например триметилборатом в присутствии основания, такого как трет-бутиллитий.
На стадии 1в реакцию сочетания предпочтительно проводят на соединении (Ia), где Z представляет собой атом брома, в присутствии основания, такого как н-бутиллитий, в инертном растворителе, предпочтительно диэтиловом эфире, при низкой температуре, предпочтительно в пределах от -80°С до -70°С. Восстановление (I’) до (I) проводят в селективных условиях, например в соответствии со способом, описанным в Tetrahedron, 1995, 51, 11043-11062, путем воздействия хлортриметилсиланом и йодидом натрия в смеси ацетонитрил/хлорированный растворитель, такой как дихлорметан, с последующей обработкой уксусной кислотой в присутствии цинка, либо, альтернативно, путем воздействия йодоводородной кислоты или путем ионного гидрирования под воздействием тетраборгидрида натрия в трифликовой (трифторметансульфоновой) кислоте.
На стадии 1 г данного способа реакцию сочетания проводят в присутствии палладиевого катализатора, одного или более чем одного третичного амина и возможно хлорида лития. Предпочтительно используют соединение (III), где Z представляет собой трифлат, и данный способ осуществляют в присутствии палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий или дихлорбис(трифенилфосфин)палладий, и возможно сокатализатора, такого как йодид меди. Когда Z представляет собой трифлат, используют также хлорид лития. Эту реакцию сочетания предпочтительно проводят в присутствии триэтиламина и пиридина при температуре дефлегмации реакционной смеси. Для этого типа сочетания, известного как сочетание Соногашира, можно сослаться на J. Org. Chem., 1993, 58, 7368-7376 и 1998, 63, 1109-1118; Syn. Lett., 1995, 1115-1116 и Synthesis, 1987, 981. Для получения соединений (I), где А представляет собой группу -СН=СН-, в Z-форме, гидрирование обычно проводят в присутствии циклогексена и металлического катализатора на носителе, такого как палладий на сульфате бария или карбонате кальция, или никель Ренея, или, предпочтительно, катализатор Линдлара, в растворителе, который является инертным для этой реакционной среды, такого как петролейный эфир или спиртовой растворитель. Для получения соединений (I) в Е-форме предпочтительно используемый гидрид металла представляет собой диизобутилалюминия гидрид (DIBALH) в инертном растворителе, таком как толуол.
Для получения соединений (I), где А представляет собой группу -СН2-СН2-, гидрирование обычно проводят в спирте, например этаноле, в присутствии катализатора, такого как оксид платины или, предпочтительно, палладий-на-угле.
Относительно методов восстановления алкенов и алкинов, используемых выше, можно сослаться на "Catalytic Hydrogenation. Techniques and Applications in Organic Chemistry", Robert L. Augustine, 1965, Narcel Dekker, Inc. New York.
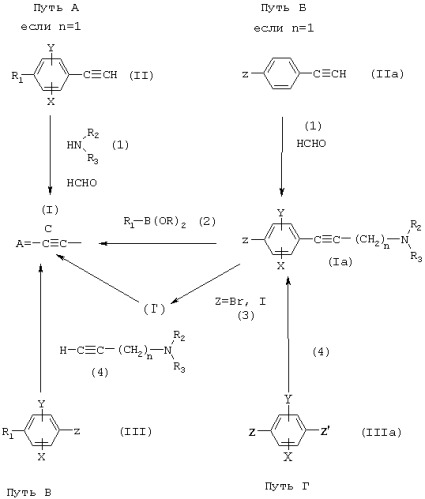
Общий способ получения соединений (I), где А представляет собой ацетиленовую группу -С≡С-, описан на схеме 1, представленной ниже.
СХЕМА 1
На схеме 1 А=-С≡С-, X, Y, n, R1, R2 и R3 являются такими, как определено для (I), R представляет собой атом водорода или алкильную или арильную группу, Z представляет собой атом брома или йода или трифлат, и, когда Z представляет собой бром или йод, Z’ представляет собой трифлат, или же Z’ представляет собой атом брома или йода. Важность природы заместителей Z и Z’ в реакции сочетания, обозначенной Путь Г, конкретизирована ниже.
Соединение (II) получают путем обработки хлоракролеина формулы
где X, Y и R1 являются такими, как определено для (I), в основной среде, предпочтительно воздействуя гидроксидом натрия в растворителе, таком как тетрагидрофуран или, предпочтительно, 1,4-диоксан, при температуре дефлегмации растворителя.
Хлоракролеин (IV) получают из ацетофенона формулы
где X, Y и R1 являются такими, как определено для (I), воздействуя комплексом Вилсмейера. Используют, например, хлорид (хлорметилен)диметиламмония, представляющий собой коммерческий комплекс Вилсмейера, или комплекс Вилсмейера, полученный из дизамещенного формамида, объединенного с оксалилхлоридом, оксихлоридом фосфора или фосгеном. Этот способ обычно осуществляют в хлорированном растворителе или эфире при температуре между -20°С и 40°С. Более конкретно, используют комплекс Вилсмейера, полученный из диметилформамида и оксалилхлорида в растворителе, таком как дихлорметан или 1,2-диметоксиэтан, при температуре между -10°С и 10°С.
Для этого типа реакции можно сослаться, например, на J. Chem. Soc. (С), 1970, 2484-2488 и Angew. Chem. Internat. Ed., 1963, 2, 98-99.
Ацетофеноны (V) известны или их получают известными способами, такими как способы, описанные в Gazz. Chim. Ital., 1949, 79, 453-457 и J. Am. Chem. Soc., 1947, 69,1651-1652.
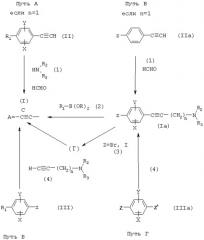
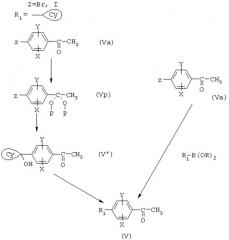
Схема 2 иллюстрирует способы, используемые для получения соединений (V).
СХЕМА 2
На схеме 2 X, Y и R1 являются такими, как определено для (I), Су является таким, как определено для (I'), Z представляет собой атом брома или йода или OTf, R представляет собой атом водорода или алкильную или арильную группу, и Р представляет собой защитную группу для кетонной функциональной группы, такую как метил.
Соединения (V) могут быть получены непосредственно из соединений (Va) путем воздействия соединением бора R1-B(OH)2 (2), как описано для превращения из (Ia) в (I). Кетонная функциональная группа соединения (Va) также может быть защищена традиционным образом, например путем воздействия триалкилортоформиатом в соответствующем спирте в присутствии кислоты, такой как пара-толуолсульфоновая кислота.
Полученное таким образом соединение (Vp) подвергают взаимодействию с кетоном в условиях, описанных для превращения из (Ia) в (I’). С кетонной функциональной группы удаляют защиту путем гидролиза в кислотной среде с получением соединения (V’). Указанное соединение (V’) затем восстанавливают в мягких условиях, описанных для превращения (I’) в (I).
В некоторых случаях, например когда R1 представляет собой 4,4-диметилциклогексильную или 4-тетрагидропиранильную группу, может образовываться промежуточное соединение формулы
где Х=О или -С(СН3)2, которое после предварительной защиты кетонной функциональной группы и гидрирования, например, в присутствии палладия-на-угле в метаноле и последующего удаления защиты с кетонной функциональной группы кетона дает целевое соединение (V).
Соединение (V), где Х и/или Y иные, чем водород, может быть получено из соединений (V), где Х=Y=Н, способами, хорошо известными специалистам в данной области. Например, когда Х и/или Y представляет собой атом хлора, хлорирование ароматического ядра проводят путем воздействия газообразным хлором в присутствии кислоты Льюиса, предпочтительно трихлорида алюминия, в хлорированном растворителе, таком как дихлорметан, предпочтительно при 0°С.
Соединения (Va) также имеются в продаже или могут быть получены способами, известными специалистам в данной области.
Например, когда Z представляет собой трифлат, соединение (Va) может быть получено, как изображено на схеме 3:
СХЕМА 3
На схеме 3 Х и Y являются такими, как определено для (I). Соединения (VIII) имеются в продаже или их получают стандартными способами.
В соответствии с еще одним из аспектов объектом настоящего изобретения также являются соединения формулы (Iа)
где X, Y, n, R2 и R3 являются такими, как определено для (I), а Z представляет собой атом брома, или атом йода, или OTf. Эти соединения являются новыми и являются ключевыми промежуточными соединениями в синтезе соединений (I).
Настоящее изобретение также относится к способу получения производных (Iа), отличающемуся тем, что:
- либо, когда n=1, проводят реакцию Манниха между фенилацетиленовым производным формулы
где X и Y являются такими, как определено для (I), a Z представляет собой атом брома, или атом йода, или OTf, формальдегидом и амином (1) HNR2R3;
- либо проводят реакцию сочетания между амином формулы
где R2, R3 и n являются такими, как определено для (I), и производным формулы
где Х и Y являются такими, как определено для (I), Z представляет собой атом брома, или йода, или трифлат, и Z’ представляет собой атом брома или йода, если Z представляет собой трифлат, в противном случае Z’ представляет собой трифлат, в присутствии палладиевого катализатора, одного или более чем одного третичного амина и возможно хлорида лития.
Реакцию Манниха проводят в таких же условиях, как условия, описанные для превращения из (II) в (I).
Реакцию Соногашира, описанную для сочетания соединений (III) и (4), используют для сочетания соединений (IIIa) и (4). Когда Z представляет собой трифлат, а Z’ представляет собой атом брома или йода, способ осуществляют в отсутствие хлорида лития. С другой стороны, когда Z представляет собой атом брома или йода, а Z’ представляет собой трифлат, способ осуществляют в присутствии хлорида лития. Использование хлорида лития создает возможность управлять реакцией сочетания.
Пропаргиламины (4) (в случае, когда n=1) получают традиционным образом, например согласно Tetrahedron Lett. 1989, 30 (13), 1679-1682, начиная с амина (1) HNR2R3 и 3-бромпропина, путем воздействия карбонатом калия в ацетонитриле при температуре между 50°С и 80°С.
Соединения (III), где Z=OTf, обычно традиционно получают из соответствующих спиртов формулы
где X, Y и R1 являются такими, как определено для (I), путем воздействия трифторметансульфонового ангидрида (трифликового ангидрида) в пиридине. Сами спирты (IX) получают из соединений формулы
где Z" представляет собой атом брома или йода, способами, описанными ранее для превращения (Iа) в (I) или (Va) в (V). Соединения (IХа) имеются в продаже или их получают способами, которые хорошо известны специалистам в данной области.
Соединение (IIа) получают из хлоракролеина формулы
где Х и Y являются такими, как определено для (I), а Z представляет собой атом брома или йода или OTf, который сам получают из ацетофенона формулы
где X, Y и Z являются такими, как определено выше для (IVa), способами, описанными для превращения (IV) в (II) и (V) в (IV).
Соединения по изобретению были подвергнуты биохимическим и фармакологическим исследованиям. Соединения формулы (I) и их фармацевтически приемлемые соли, гидраты и сольваты специфически связываются с сигма-рецепторами, в частности с сигма-рецепторами периферической нервной системы, также известными как рецепторы сигма-2.
Аффинность в отношении рецепторов сигма-1 исследовали in vitro на мембранах головного мозга морских свинок с использованием 3H-(+)-3PPP в качестве лиганда согласно De Haven-Hudkins et al., Life Science, 1993, 53, 41-48. (+)-Пентазоцин специфически связывается с рецепторами сигма-1. Фрагмент мембраны головного мозга морских свинок готовят обычными способами. Препарат мембран (0,3 мг белка/мл) инкубируют в течение 150 минут при 37°С в присутствии 0,5 нМ [3Н]-(+)-пентазоцина. Неспецифическое связывание определяют в присутствии 10 мкМ (+)-пентазоцина. Мембраны затем фильтруют и промывают 3 раза. Отфильтрованный материал анализируют с целью определения специфически связанной фракции [3H]-пентазоцина. В этих условиях соединения по изобретению, примеры которых следуют ниже, имеют значения ИК50 между 0,1 нМ и 100 нМ.
Способность соединений по изобретению взаимодействовать с рецепторами сигма-2 тестировали in vitro на мембранах селезенки крыс, используя в качестве лиганда [3H]-DTG, в соответствии с R. Paul et al. Journal of Neuroimmunology, 1994, 52, 183-192. Препарат мембран (1 мл) инкубируют с 2 нМ [3H]-DTG в течение 90 минут при 20°С. Величину неспецифического связывания оценивают в присутствии 10 мкМ DTG или галоперидола. Мембраны фильтруют и промывают дважды, и отфильтрованный материал анализируют с целью определения количества специфически связанного [3Н]-DTG. Соединения по изобретению обладают активностью в отношении сигма-2 между 1 нМ и 500 нМ.
Соединение примера 44, приведенного ниже, тестировали на связывание на мембранах, извлеченных из клеток млекопитающих и дрожжей, экпрессирующих либо сигма-1, сигма-2, либо стерин-изомеразу человека (Human sterol isomerase (HIS)). Результаты этих испытаний показывают, что соединения по изобретению проявляют очень высокую аффинность к рецепторам сигма-1 и сигма-2 и HIS. В приведенной ниже таблице представлены данные по аффинности соединения примера 44 к указанным рецепторам и HIS по сравнению с данными для известных из предшествующего уровня техники лигандов сигма-рецепторов.
| Лиганды/рецепторы | Сигма-1 (нМ) | HIS (нМ) | Сигма-2 (нМ) |
| Соединение примера 44 | 0,40+/-0,04 | 0,29+/-0,02 | 25+/-2 |
| (+)пентазоцин | 4,3+/-0,2 | >1000 | 2900+/-500 |
| (-)пентазоцин | 62+/-3 | >1000 | 75+/-10 |
| (+) 3-РРР | 31 | >1000 | 158+/-11 |
| DTG | 38+/-1 | >1000 | 38+/-3 |
Из таблицы видно, что аффинность типичного представителя заявленных соединений (соединения примера 44) значительно выше аффинности других классических лигандов сигма-рецепторов, которые не связываются с указанными тремя рецепторами одновременно.
1 - Соединения по изобретению также испытывали в тестах на иммунодепрессивную активность.
D-Галактозамин, SEB (энтеротоксин В Staphylococcus) и LPS (липополисахариды) были получены от Sigma Chemical Co (St Louis, МО). SEB содержит менее 0,00029% эндотоксина (тест "лизат амебоцитов лимулус", Bioproduct, Walkersville, MD). Эти молекулы растворяют в фосфатном буферном растворе; соединения по изобретению растворяют в растворе, содержащем 5% этанола, 5% Твин 80 и 90% воды.
Используют самок мышей Balb/C возрастом от 6 до 8 недель, доставленных из питомника Charles River (Франция) и самок мышей C57BL/6 и B6D2F1 возрастом 8 недель, доставленных из питомника IFFA CREDO (Domaine des Oncins, BP 0109, 69592 L'Arbresle Cedex, Франция).
Измерение цитокинов: 5 мышам внутрибрюшинно инъецируют соединения или один растворитель за 30 минут до введения LPS (10 мкг/мышь внутривенно) или перорально за 1 час до LPS. Образцы крови отбирают путем ретро-глазничной или сердечной пункции через 1 час 30 минут после инъекции LPS. Образцы центрифугируют и получают сыворотку крови. Сыворотку крови хранят при -80°С до анализа. Содержание TNF-α и IL-10 определяют с помощью набора ELISA (Genzyme, Cambridge). Тесты проводят согласно инструкциям по использованию.
Токсический шок: Соединения вводят внутрибрюшинно 10 животным. Через 30 минут SEB (Staphylococcus энтеротоксин В, Sigma St. Louis, МО) вводят в количестве 10 мкг/мышь внутривенно, и вводят D-галактозамин (20 мг/мышь, внутрибрюшинно).
Смерть наблюдают через 48 часов.
Болезнь ТПХ (трансплантат-против-хозяина): Тестируемые соединения или только растворитель (в качестве контроля) инъецируют самкам B6D2F1 (H2b × H2d) мышей внутрибрюшинно. Через 4 часа им инъецируют 7,5×107 C57BL/6 (H2b) мононуклеарных клеток селезенки мыши, чтобы инициировать ТПХ. Всех животных умерщвляют через одну неделю после трансплантации и измеряют увеличение массы их селезенки, вызванное ТПХ. Рассчитывают следующий показатель:
Результаты выражают следующим образом:
где PS - процент спленомегалии.
Измерение Т клеточной пролиферации: Суспензии клеток готовят, используя селезенки мышей Balb/C. Красные кровяные тельца сначала лизируют в ходе краткого гипотонического шока, достигаемого с использованием стерильной дистиллированной воды. Остальные клетки (белые кровяные тельца) дважды промывают культуральной средой (RPMI 1640, содержащей 2% термически инактивированной сыворотки эмбрионов коров, 2 мМ L-глутамина, 1 мМ пирувата натрия, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина и 15 мМ PIPES (пиперазин-N,N-бис(2-этансульфоновой кислоты)), заблаговременно доведенной до рН 6,6. Жизнеспособность клеток, определяемая с использованием трипанового синего, всегда превышает 95% при этом способе приготовления. Спленоциты в концентрации 6×106 клеток/мл культивируют с тестируемыми продуктами в плоскодонных 96-луночных планшетах (Falcon, Becton Dickinson, Lincoln Park, NJ) в присутствии 2 мкг/мл SEB. Четыре лунки готовят для каждой концентрации тестируемых продуктов. Инкубацию проводят при 37°С в инкубаторе для клеточных культур (