Способ пластики гепатикохоледоха трубчатым тонкокишечным трансплантатом
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к хирургии для лечения заболеваний и повреждений внепеченочных желчных путей. Сущность: дистальный анастомоз формируют между концом тонкокишечного трансплантата и нисходящей ветвью двенадцатиперстной кишки, причем создают инвагинационный арефлюксный клапан путем рассечения серозного и мышечного слоя не более 5 мм, прокола слизистого слоя, ориентацией трансплантата вдоль нисходящей ветви 12-перстной кишки и 4-6 серо-серозными швами, линию анастомоза погружают в складку стенки 12-перстной кишки, что восстанавливает отток желчи в 12-перстной кишки. 4 ил.
Реферат
Предлагаемое изобретение относится к медицине, а именно к хирургии, и может быть использовано для хирургического лечения заболеваний и повреждений внепеченочных желчных путей.
Проблема хирургического лечения стриктур магистральных желчных протоков до настоящего времени остается нерешенной, тогда как они в 7,2-41,4% случаев являются причиной повторных вмешательств на желчевыводящих путях (В.Н.Климов и соавт., 1980, Inbansi et al., 1984 и др.).
Большинство авторов высказываются о преимуществе операций, при которых восстанавливают желчеотток непосредственно в двенадцатиперстную кишку (А.А.Шалимов и соавт., 1993 и др.).
Однако подавляющее большинство предложенных вариантов пластики внепеченочных желчных протоков не отвечают всем главным требованиям, предъявляемым к трансплантату желчных путей, а именно, трансплантат должен иметь полноценную слизистую оболочку, индифферентную к постоянному воздействию желчи; он должен перистальтировать, тем самым направлять ток желчи в ДПК и препятствовать рефлюксу дуоденального содержимого в желчное дерево. И, наконец, по длине и диаметру трансплантат должен быть близким к размерам общего желчного и печеночного протока.
Предложенные аллотрансплантаты из различных материалов не имеют слизистой, ригидны, не способны перистальтировать, таким образом, подвержены облитерации желчными камнями и даже при механической проходимости могут вызывать явления холестаза. Различные трансплантаты из венозной стенки склонны к рубцеванию и замещению соединительной тканью.
Таким образом, разработка новых способов пластики внепеченочных желчных протоков является актуальной задачей хирургии.
В качестве аналогов взяты следующие способы оперативного лечения:
1. Гепатикоеюностомия по А.А.Шалимову (Шалимов А.А., Шалимов С.А., Ничитайло М.Е., Доманский Б.В. "Хирургия печени и желчевыводящих путей", Киев, "Здоров'я", 1993, стр. 473-475).
После иссечения рубцовых тканей и освобождения дистального конца общего печеночного протока производят его мобилизацию в проксимальном направлении. Петлю тощей кишки, необходимую для анастомоза, выключают по Ру или Шалимову, подводят к задней поверхности протока так, чтобы последний ложился поперек кишки по длине всей своей свободной части. При малом диаметре протока (5 мм и менее) по задней поверхности его делают продольный разрез длиной 5-8 мм. Непосредственно перед культей протока продольно вскрывают просвет тощей кишки в соответствии с диаметром протока и разрезом его. Отдельными 3-4 швами с интервалом между ними 1,5 мм нитью из не рассасывающейся ткани фиксируют боковые стенки протока к стенке кишки поперек нее. Так же отдельными швами нитью из рассасывающегося материала на атравматической игле сшивают края протока и кишки при точном сопоставлении слизистых оболочек. Затем серо-серозными швами анастомоз инвагинируют в складку кишки для уменьшения регургитационного рефлюкса из кишечника.
Недостатком операции является то, что двенадцатиперстную кишку выключат из пассажа желчи, что существенно влияет на качество пищеварения.
2. Способ пластики внепеченочных желчных протоков пупочной аутовеной, предварительно подготовленной в среде 199, предложенный О.М.Горбуновым (Горбунов О.М., Сахно Р.Д. Клиническая оценка способа аутовенозной пластики внепеченочных желчных протоков. // Вестник хирургии, 1994. - Т.152. - №3-4. - С.55-60).
Под местной анестезией иссекают сегмент большой подкожной вены длиной 6 см, который погружают в стерильную колбу с поддерживающей питательной средой 199, которую помещают в холодильник с температурой +3°С на 7 суток.
По истечении этого срока выполняют лапаротомию, выделяют дистальный и проксимальный концы желчных протоков. Осуществляют пластику дефекта подготовленным аутовенозным сегментом на дренаже-каркасе из полиэтиленовой трубки диаметром 0,6 см. Проксимальный конец ее вводят в один из долевых протоков, дистальный проводят транспапиллярно в двенадцатиперстную кишку. Аутопластику выполняют сшиванием концов консервированной аутовены с концами - проксимальным и дистальным - гепатикохоледоха супрамидной нитью 6/0 на атравматической игле узловыми матрацными швами. Недостатки:
- необходимо предварительно готовить аутовену для трансплантации в специальной среде;
- невозможно добиться полноценной эпителизации венозного трансплантата, таким образом, всегда остается опасность ее рубцевания;
- стенка аутовены, замещаясь рубцом, не способна перистальтировать и, следовательно, активно участвовать в поступательном продвижении желчи в двенадцатиперстную кишку, препятствовать рефлюксу дуоденального содержимого.
В качестве прототипа взят способ пластики гепатикохоледоха, представленный В.И.Кочиашвили в “Атласе хирургических вмешательств на желчных путях” (М., “Медицина”, 1971. - С.123-124).
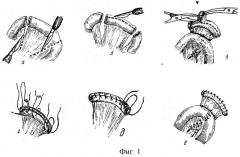
Способ выполняют следующим образом. Изолируют сегмент тонкой кишки на участке брыжейки достаточной длины, чтобы беспрепятственно переместить его в подпеченочное пространство. Трансплантат готовят путем резекции 1/2 диаметра стенки кишки по противобрыжеечному краю и сшивания свободных краев кишки между собой (фиг.1). Между концами трансплантата и концами общего печеночного и общего желчного протоков формируют анастомозы.
Недостатки:
- способ неприменим при грубом рубцовом изменении дистальной части общего желчного протока и большого дуоденального сосочка;
- при отсутствии дополнительной фиксации трансплантата в подпеченочном пространстве возможно возникновение натяжения по линии швов анастомоза с дальнейшим развитием его несостоятельности и стриктуры;
- при отсутствии оментизации трансплантата в подпеченочном пространстве возможно вовлечение его стенок в грубый рубцово-спаечный процесс, который препятствует перистальтике, что может вызвать явления холестаза;
- при формировании трансплантата внешним диаметром более 1 см в отдаленном послеоперационном периоде за счет растяжения стенок кишки диаметр сформированной трубочки становится намного больше диаметра внепеченочных желчных протоков, что может приводить к застою желчи, нарушению ее продвижения по трансплантату и снижению арефлюксных свойств созданной конструкции.
Задачи:
обеспечить беспрепятственный пассаж желчи в двенадцатиперстную кишку;
предотвратить рефлюкс дуоденального содержимого в желчные протоки.
Сущность предлагаемого способа заключается в том, что дистальный анастомоз формируют между концом трансплантата и нисходящей ветвью двенадцатиперстной кишки, причем линию шва дистального анастомоза инвагинируют в складку стенки двенадцатиперстной кишки, трансплантат за листки брыжейки фиксируют в подпеченочном пространстве к тканям гепатодуоденальной связки отдельными швами-связками и выполняют оментизацию трансплантата выкроенными прядями большого сальника.
Способ осуществляют следующим образом.
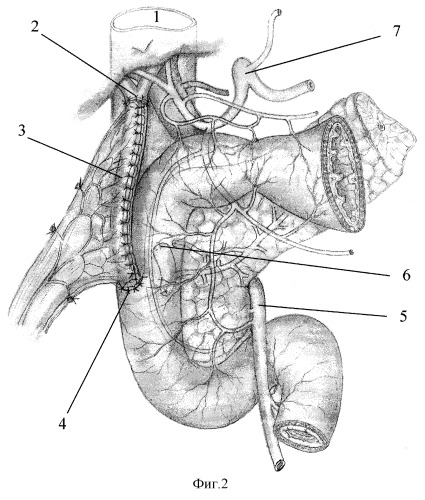
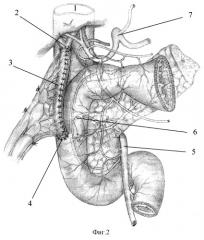
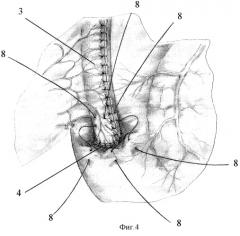
Описание способа иллюстрировано на фиг.2-4,
где:
1 - нижняя полая вена;
2 - анастомоз между общим печеночным протоком и тонкокишечным трансплантатом;
3 - тонкокишечный трансплантат;
4 - анастомоз между тонкокишечным трансплантатом и ДПК;
5 - верхняя брыжеечная артерия;
6 - зарубцованная культя холедоха;
7 - чревный ствол;
8 - швы, инвагинирующие линию анастомоза в ДПК;
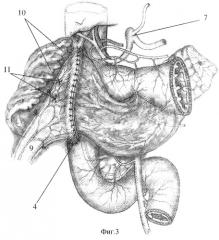
9 - брыжейка трансплантата;
10 - прядь сальника, окутывающая трансплантат;
11 - завязанные швы-связки, фиксирующие брыжейку трансплантата.
Выделяют и готовят к анастомозированию конец общего печеночного протока.
Выделяют из сращений и мобилизуют панкреато-дуоденальный комплекс. Для облегчения мобилизации вертикальной ветви ДПК вместе с головкой поджелудочной железы с целью гидравлической препаровки тканей и уменьшения травматичности манипуляций парадуоденально и парапанкреатически вводят достаточное количество раствора новокаина. Рассекают брюшину вдоль вертикальной ветви двенадцатиперстной кишки и фасциальные листки между двенадцатиперстной кишкой, задней поверхностью головки поджелудочной железы и паранефральной клетчаткой, нижней полой веной.
Выбирают участок тонкой кишки длиной 10-12 см на расстоянии 40-80 см от связки трейца. Учитывая архитектонику сосудов брыжейки соответственно предполагаемым границам пересечения кишки, рассекают брюшинные листки брыжейки тонкой кишки, перевязывают и пересекают сосуды аркад с сохранением магистрального кровоснабжения.
По выбранным границам пересекают кишку так, чтобы получить изолированный участок длиной 8-10 см. Непрерывность тонкой кишки восстанавливают прецизионным анастомозом “конец в конец” однорядным серозно-мышечно-подслизистым швом мононитью.
Строго по противобрыжеечному краю выкроенного сегмента тонкой кишки продольно иссекают участок кишечной стенки, оставляя лоскуты шириной 0,5 см от краев брыжейки. При сильном кровотечении из сосудов подслизистого слоя их лигируют. Свободные края кишечной стенки сшивают между собой однорядными серозно-мышечно-подслизистыми узловыми швами монофиламентной нитью.
Таким образом формируют тонкую (внешним диаметром до 1 см) трубочку из кишки на участке брыжейки. Сквозь аутотрансплантат проводят тонкую перфорированную на всем протяжении дренажную трубочку такой длины, чтобы она выступала из концов трансплантата на 3-4 см. Дренаж необходим в ближайшем послеоперационном периоде для беспрепятственного тока желчи на время стихания воспалительной реакции в зонах анастомозов и в целом в трансплантате.
В правой части брыжейки поперечно-ободочной кишки в бессосудистой зоне проделывают окно. Через него в подпеченочное пространство к воротам печени перемещают подготовленный трансплантат, который укладывают изоперистальтически по отношению к току желчи от ворот печени вдоль печеночно-двенадцатиперстной связки и далее вдоль нисходящей ветви двенадцатиперстной кишки (фиг.2).
Далее готовят лоскуты большого сальника для оментизации в зависимости от его величины, характера кровоснабжения и повреждений, полученных на предыдущих операциях. Правую половину сальника отделяют от поперечной ободочной кишки, затем ее расщепляют вдоль, чтобы получить применительно к конкретной ситуации 2-3 отдельных лоскута с хорошим кровоснабжением.
Правый краевой лоскут оставляют для оментизации на завершающем этапе всего мобилизованного панкреато-дуоденального комплекса вместе с трансплантатом.
Другой сальниковый лоскут укладывают и расправляют на переднелатеральной поверхности гепатодуоденальной связки. Его верхний край фиксируют к тканям ворот печени под задней стенкой конца общего печеночного протока. На сальник укладывают трансплантат, а его верхнелатеральный свободный край используют после формирования проксимального анастомоза для окутывания последнего (фиг.3).
Таким образом, сформированный заново внепеченочный желчный проток вместе с проксимальным анастомозом оказывается полностью окружен сальниковым футляром, который отделяет трансплантат и зону проксимального анастомоза от рубцовых тканей и сосудов гепатодуоденальной связки. Тем самым предотвращается образование грубых рубцовых сращений между трансплантатом и окружающими рубцовыми тканями и сосудами, что позволяет кишечной трубочке свободно перистальтировать.
Между концом общего печеночного протока и концом трансплантата формируют прецизионный однорядный анастомоз узловыми швами рассасывающимся синтетическим шовным материалом 5/0-6/0 узлами вне просвета протока. При этом шов на кишке серозно-мышечно-подслизистый, на конце протока - без захвата слизистой оболочки. Через анастомоз в правый или левый долевой проток продвигают конец “скрытого” дренажа.
Для дополнительной фиксации оптимального положения трансплантата и исключения натяжения по линии швов анастомоза формируют связочный аппарат. Он представляет собой несколько 8-образных швов тонкой мононитью, в которые захватываются листки брюшины (без сосудов!) брыжейки трансплантата, далее нить проходит сквозь подлежащий сальниковый лоскут (в бессосудистой зоне!) и через рубцовые ткани гепатодуоденальной связки. Швы затягивают не туго, только до соприкосновения тканей. Формируют от 2 до 4 швов-связок (фиг.3).
Далее приступают к формированию анастомоза с двенадцатиперстной кишкой. При этом трансплантат располагают вдоль нисходящей ветви двенадцатиперстной кишки. Анастомоз формируют на границе ее средней и нижней трети по переднелатеральной стенке.
Отверстие в стенке двенадцатиперстной кишки проделывают следующим образом: серозную и мышечную оболочки рассекают на протяжении не более 5 мм, а слизистую вскрывают проколом, т.к. отверстие в стенке кишки легко растяжимо и позволяет сформировать хороший анастомоз, просвет которого будет в последующем хорошо смыкаться. Формируют прецизионный однорядный анастомоз узловыми серозно-мышечно-подслизистыми швами рассасывающимся монофиламентным синтетическим шовным материалом 6/0 узлами наружу. (фиг.2, 3). При этом конец “скрытого” дренажа проводят в просвет двенадцатиперстной кишки. С помощью 4-6 серо-серозных швов линию швов анастомоза погружают в складку стенки двенадцатиперстной кишки, таким образом усиливая арефлюксные свойства формируемого соустья. Швы располагают в межсосудистых промежутках для исключения нарушения кровоснабжения в анастомозированных стенках (фиг.4).
Выкроенным ранее латеральным (правым) лоскутом большого сальника укрывают переднюю поверхность головки поджелудочной железы, вертикальную ветвь двенадцатиперстной кишки, тонкокишечный трансплантат. Свободный край сальникового лоскута заводят под мобилизованную головку двенадцатиперстной кишки, укладывая его между последней и нижней полой веной. В таком положении сальник фиксируют несколькими отдельными швами.
Левую половину большого сальника расправляют и укладывают на петли тонкого кишечника. Дренируют подпеченочное пространство двухпросветным дренажем.
Пример
Больная Д., 60 лет. Поступила со стриктурой гепатикохоледоха и полным наружным желчным свищем, сформировавшимися в результате ятрогенного повреждения протоков во время холецистэктомии.
13.09.01 г. больная оперирована. Под общим обезболиванием с ИВЛ выполнена расширенная верхнесрединная лапаротомия с иссечением старого послеоперационного рубца и аппаратной коррекцией доступа ранорасширителем Сигала. В подпеченочном пространстве - выраженный спаечный процесс - к висцеральной поверхности печени подпаяны большой сальник, ободочная кишка, антральный отдел желудка. После разделения сращений выделена гепатодуоденальная связка и взята на держалку. Из рубцовых тканей гепатодуоденальной связки выделен общий печеночный проток, который заканчивается полной облитерацией на расстоянии 2,5 см от бифуркации. Ширина протока до 1,5 см. Ниже в тканях гепатодуоденальной связки определяются рубцовые ткани. Выполнена мобилизация вертикальной ветви ДПК вместе с головкой поджелудочной железы. Дистальный отдел холедоха обнаружить среди рубцов не представляется возможным.
Решено выполнить пластику трубчатым трансплантатом из сегмента тонкой кишки. Правая половина большого сальника отделена от ободочной кишки и расщеплена на 2 лоскута. Выбран сегмент тонкой кишки на расстоянии 40 см от связки трейца длиной 8 см. Соответственно выбранному сегменту мобилизована брыжейка тонкой кишки, кишка пересечена. Противобрыжеечный край тонкой кишки резецирован и из сегмента кишки сформирована трубочка длиной 8 см, диаметром 8 мм. Трансплантат перемещен через окно в мезоколон в подпеченочное пространство и уложен изоперистальтически от ворот печени к ДПК. На гепатодуоденальную связку под трансплантат уложена прядь большого сальника, верхний край которой фиксирован в воротах печени под концом общего печеночного протока. Сформирован однорядный прецизионный анастомоз между концом общего печеночного протока и концом трансплантата. Свободным краем пряди сальника выполнена оментизация анастомоза. Через трансплантат проведен тонкий перфорированный на всем протяжении дренаж. На границе средней и нижней трети вертикальной ветви ДПК выполнена точечная дуоденотомия. Сформирован однорядный анастомоз между концом трансплантата и ДПК. Перед наложением швов на переднюю стенку анастомоза в ДПК проведен конец скрытого дренажа, который фиксирован рассасывающейся нитью к линии швов анастомоза. С помощью 6 серо-серозных швов выполнена инвагинация линии шва анастомоза в складку стенки ДПК. Правым латеральным лоскутом большого сальника оментизирован панкреато-дуоденальный комплекс вместе с трансплантатом. Имеющийся транспеченочный дренаж (установленный до операции под контролем ультразвука) оставлен для декомпрессии в раннем послеоперационном периоде. Непрерывность тонкой кишки в нижнем этаже брюшной полости восстановлена анастомозом конец в конец. Установлены дренажи в малый таз и подпеченочное пространство. Брюшная стенка ушита послойно наглухо.
Послеоперационный период протекал гладко. Желчеистечение по оставленному чрезпеченочному дренажу к 12 суткам уменьшилось с 500 до 100 мл в сутки. Дренаж перекрыт и больная выписана. При контрольном обследовании через 1 месяц самочувствие хорошее. При выполнении контрольной холангиоргафии контраст свободно проникает через трансплантат в ДПК. При этом имеется отчетливая перистальтика трансплантата. Удален чрезпеченочный дренаж. Во время дуоденоскопии удален “скрытый” дренаж, при этом анастомоз расположен на некотором возвышении стенки ДПК, просвет его сомкнут. Отмечено порционное поступление желчи в ДПК. При рентгеноскопическом исследовании пассажа контрастного вещества по ДПК и выполнении провоцирующих проб (напряжение брюшной стенки, положение Тренделенбурга) рефлюкса в желчные протоки не выявлено.
При обследовании через год жалоб не предъявляет. Биохимические маркеры холестаза в пределах нормы. Клинические и УЗ-признаки холангита и дуодено-билиарного рефлюкса отсутствуют.
Использование способа позволяет добиться восстановления желчеоттока в двенадцатиперстную кишку, что благотворно сказывается на процессе пищеварения и его регуляции. Наличие у трансплантата полноценной стенки со слизистой оболочкой и перистальтирующим мышечным слоем препятствует возникновению сужения вновь образованных желчных путей и анастомозов. Инвагинационный дистальный анастомоз между трансплантатом и двенадцатиперстной кишкой позволяет добиться поступательного продвижения желчи в кишечник, препятствуя попаданию кишечного содержимого в желчное дерево. Таким образом, применение методики приводит к надежному выздоровлению больных, возвращая их к полноценной жизни и труду.
Способ пластики гепатикохоледоха, включающий использование в качестве трансплантата цилиндрической кишечной трубки, сформированной из изолированного сегмента тонкой кишки на сосудистой ножке путем резекции стенки кишки по противобрыжеечному краю и сшиванием ее свободных краев, отличающийся тем, что дистальный анастомоз формируют между концом тонкокишечного трансплантата и нисходящей ветвью двенадцатиперстной кишки, причем создают инвагинационный арефлюксный клапан путем рассечения серозного и мышечного слоев не более 5 мм, прокола слизистого слоя, ориентацией трансплантата вдоль нисходящей ветви двенадцатиперстной кишки и 4-6 серосерозными швами линию анастомоза погружают в складку стенки двенадцатиперстной кишки.