Иммуногенный конъюгат бета-пропионамид-связанного полисахарида с белком, использующийся в качестве вакцины
Иллюстрации
Показать всеИзобретение относится к иммунологии. Предоставляются новые иммуногенные конъюгаты β-пропионамидсвязанного полисахарида и N-пропионамидсвязанного олигосахарида с белком, а также способ получения этих конъюгатов. Конъюгаты используют для получения вакцин против инфекционных заболеваний и рака, что позволяет расширить арсенал медицинских препаратов, используемых для лечения этих заболеваний. 5 н. и 44 з.п. ф-лы, 1 ил., 8 табл.
Реферат
Настоящее изобретение относится к иммуногенным конъюгатам β-пропионамидсвязанного полисахарида с белком и к способам получения этих конъюгатов из бактерий, дрожжей или раковых клеток. Эти конъюгаты используются в качестве вакцин.
Бактериальные инфекции, вызываемые грамположительными бактериями, такими как Streptococcus, Staphylococcus, Enterococcus, Bacillus, Corynebacterium, Listeria, Erysipelothrix и Clostridium, и грамотрицательными бактериями, такими как Haemophilus, Shigella, Vibrio cholerae, Neisseria и некоторые типы Esherichia coli, вызывают значительную заболеваемость во всем мире. Этот факт вместе с возникающей устойчивостью, которую проявляют бактерии по отношению к антибиотикам, определяет необходимость разработки бактериальных вакцин. Например, streptococci представляют собой большой и разнообразный род грамположительных бактерий, который был подразделен на несколько групп на основе антигенности и структуры полисахаридов их клеточных стенок (26, 27). Две из этих групп связаны с серьезными инфекциями человека. Streptococci группы А вызывают ряд инфекционных нарушений, включая "стрептококковое горло", ревматическую лихорадку, стрептококковое импетиго и сепсис. Streptococci группы В являются важными перинатальными патогенами в США, а также в развивающихся странах (37).
Грамотрицательные бактерии также являются существенной причиной заболеваний. До разработки и применения в последнее время полисахарид-белковых вакцин, направленных против бактерии Haemophilus influenzae типа b (Hib), бактериальные инфекции Hib являлись причиной многочисленных случаев задержки умственного развития у детей. Инфекции N. menigitidis и Е.coli K1 ответственны за неонатальный менингит. Штаммы грамотрицательных бактерий, Е. coli, связаны с серьезными заболеваниями, включая гибель организма, наступающую в результате потребления мяса, зараженного штаммами Е. coli.
Конъюгаты полисахаридов с другой иммуногенной молекулой, такой как полипептид или белок, использовались для инициирования гуморальных иммунных ответов на ряд грамотрицательных и грамположительных бактерий. Конъюгирование полисахарида или олигосахарида с полипептидом превращает иммунный ответ на полисахарид или олигосахарид, который обычно является Т-независимым, в Т-зависимый ответ.
В предыдущем уровне техники раскрывается как прямое, так и непрямое соединение полисахаридов с белками с образованием конъюгатов (итог подведен в ссылке (11) и патенте США №5 306 492). Методы конъюгирования включают в себя диазосочетание, тиоэфирное связывание, амидирование, восстановительное аминирование и тиокарбамоилирование для присоединения к белковому носителю.
Gever et al., Med. Microbiol. Immunol., 165: 171-288 (1979) описали получение конъюгатов некоторых капсульных полисахаридных фрагментов Klebsiella pneumoniae с нитрофенилэтиламиновым линкером путем восстановительного аминирования и присоединение производного сахара с помощью азосочетания.
В патенте США №4 057 685, McIntire, описан липополисахарид Escherichia coli с пониженной токсичностью, ковалентно связанный с белковым антигеном в результате взаимодействия с галогенангидридом.
В патенте США №4 356 170, Jennings et al., описывается получение полисахарид-белковых конъюгатов методом восстановительного аминирования.
В патенте США №4 673 574, 4 761 283 и 4 808 700, Anderson, описано получение иммуногенных конъюгатов, включающих в себя продукт восстановительного аминирования иммуногенного капсульного полисахаридного фрагмента, полученного из капсульного полимера Streptococcus pneumoniae или Н. influenzae, содержащего восстанавливающий конец, полученный с помощью таких методов, как окислительное расщепление периодатом или путем гидролиза гликозидной связи, и бактериальный токсин или токсоид в качестве белкового носителя.
В патенте США №4 459 286, Hillman et al., описано получение полисахарид-белкового конъюгата путем активации полисахарида Н. influenzae типа b цианбромидом, получения производного активированного полисахарида со спейсерной молекулой, 6-аминокапроновой кислотой и присоединения основного белка внешней мембраны Neisseria meningitidis с использованием водорастворимого карбодиимида с образованием связи амидного типа с белком через сложный ряд связующих звеньев от спейсера 6-аминокапроновой кислоты до полисахарида.
В патенте США №4 965 338, Gordon, описано получение водорастворимого ковалентного конъюгата полисахарида с дифтерийным токсоидом, где чистый полисахарид Н. influenzae типа b активируют цианбромидом и сразу смешивают с дифтерийным токсоидом, модифицированным ADH-спейсером.
В патенте США №4 663 160, Tsay et al., описан детоксифицированный полисахарид грамотрицательных бактерий, ковалентно связанный с детоксифицированным белком, полученным из тех же видов грамотрицательных бактерий, посредством фрагмента, имеющего 4-12 атомов углерода.
В патенте США №4 619 828, Gordon et al., описаны конъюгаты молекул полисахаридов патогенных бактерий, таких как Haemophilus influenzae типа В, Streptococcus pneumoniae, Neisseria meningitidis и Escherichia coli, с Т-зависимыми антигенами, такими как дифтерийный и столбнячный токсоиды.
В патенте США №4 711 779, Porro et al., описаны вакцины на основе конъюгатов гликопротеинов, обладающие трехвалентной иммуногенной активностью, содержащие антигенные детерминанты капсульных полисахаридов грамположительных бактерий, а также либо CRM197, столбнячный токсоид, либо коклюшный токсин.
В патенте США №5 306 492, Porro, описан конъюгат олигосахарида с белком-носителем, полученный путем взаимодействия олигосахарида, имеющего концевую восстанавливающую группу, с диаминометаном в присутствии пиридинборана, эта реакция представляет собой восстановительное аминирование, взаимодействия аминированного олигосахаридного продукта с молекулой, имеющей две функциональные группы, и затем взаимодействия активированного олигосахаридного продукта с белком-носителем.
В патенте США №5 192 540, Kuo et al., описан конъюгат олигосахарида с белком, включающий в себя продукт восстановительного аминирования окисленного полирибозил-рибитолфосфат полисахаридного фрагмента, полученного из капсульного полисахарида Haemophilus influenzae типа В, и белка внешней мембраны Haemophilus influenzae типа В.
В публикации заявки на европейский патент №ЕР 0747063 А2 описан модифицированный капсульный полисахарид, содержащий различные производные сиаловой кислоты, и гетеробифункциональную линкерную молекулу, связанную с молекулой носителя. Линкеры используются для N-алкилирования приблизительно до 5 остатков сиаловой кислоты на полисахарид. Затем оставшиеся аминогруппы ацилируют пропионовым или уксусным ангидридом.
Существует потребность в более эффективных очищенных иммуногенных полисахарид-белковых конъюгатах, которые могут быть получены более простым способом и с более высоким выходом, для широкомасштабного получения вакцин на основе иммуногенных полисахарид-белковых конъюгатов.
Данное изобретение связано с иммуногенным конъюгатом β-пропионамидсвязанного полисахарида и β-пропионамидсвязанного олигосахарида с белком.
Целью данного изобретения является предоставление способа получения иммуногенных конъюгатов β-пропионамидсвязанного полисахарида с белком, который имеет преимущества по сравнению с применяющимися в настоящее время методологиями. Дальнейшей целью данного изобретения является предоставление фармацевтических композиций, вакцин и других иммунологических реагентов, полученных на основе иммуногенных конъюгатов β-пропионамидсвязанного полисахарида с белком.
Предоставляется способ получения иммуногенных полисахарид-белковых конъюгатов, который включает в себя де-N-ацетилирование полисахарида или олигосахарида путем основного или ферментативного гидролиза с последующим N-акрилоилированием N-деацетилированного полисахарида. N-акрилоилированный полисахарид непосредственно присоединяется к носителю-белку с образованием иммуногенного конъюгата β-пропионамидсвязанного полисахарида с белком.
Полисахариды капсулы и клеточной поверхности можно экстрагировать в соответствии с данным изобретением либо из клеточных супернатантов бактерий, дрожжей или млекопитающих, или непосредственно из клеток бактерий, дрожжей или млекопитающих, путем гидролиза неустойчивой к действию основания связи, которая связывает полисахарид с другими клеточными компонентами, или путем ферментативного гидролиза. Часть N-ацетильных групп, удаленных в результате гидролиза с полисахарида, заменяют на N-акрилоильные группы, которые, в свою очередь, непосредственно связаны с белком, с образованием конъюгата согласно изобретению.
В одном аспекте данного изобретения предоставляются олигосахариды и полисахариды, которые непосредственно присоединены к белку (белкам) по нескольким положениям.
В другом аспекте данного изобретения предоставляется способ иммунизации млекопитающего против бактериальных или дрожжевых инфекций, или рака, который включает в себя введение млекопитающему эффективного количества вакцины согласно изобретению для предотвращения инфекции от болезнетворного организма или рака.
Аспектом настоящего изобретения является способ индуцирования продукции антител у млекопитающих с помощью конъюгатов β-пропионамидсвязанного полисахарида с белком, которые защищают млекопитающее от инфекции или болезни.
Другим аспектом данного изобретения являются иммуноглобулин и выделенное антитело, продуцирующееся в ответ на иммунизацию конъюгатами β-пропионамидсвязанного полисахарида с белком. Такие иммуноглобулин и выделенное антитело используются в качестве лекарственных препаратов и диагностических реагентов.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖА
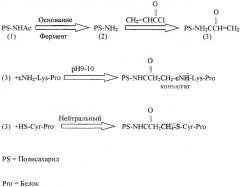
Чертеж 1. Схематическое изображение способа получения иммуногенных конъюгатов β-пропионамидсвязанного полисахарида с белком.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном изобретении представлены новые полисахарид-белковый конъюгат и олигосахарид-белковые конъюгаты, применяющиеся в качестве иммуногенов и вакцин против бактериальных инфекций, дрожжевых инфекций, а также в качестве противораковых лекарственных препаратов. Полисахариды или олигосахариды, использующиеся для образования иммуногенных конъюгатов β-пропионамидсвязанного полисахарида с белком, получают из источников полисахаридов или олигосахаридов, которые включают в себя, не ограничиваясь ими, грам(+) или грам(-) бактерии, дрожжи, раковые клетки или раковые ткани и т.п., в которых полисахарид или олигосахарид служит в качестве вирулентного фактора клеток при формировании защитных механизмов хозяина. Полисахарид-белковые конъюгаты настоящего изобретения образуются в результате непосредственного присоединения N-акрилоилированного полисахарида к белку путем присоединения нуклеофильных участков белков по Михаэлю.
Полисахариды или олигосахариды могут быть получены из ряда источников, включая грамотрицательные, грамположительные бактерии, дрожжи, раковые клетки или рекомбинантные формы каждого из них, путем основного или ферментативного гидролиза связи, которая соединяет полисахарид или олигосахарид с клеточными компонентами. Полисахарид или олигосахарид можно экстрагировать из организма или клетки путем приведения в контакт организма или клетки, или раствора, содержащего фрагменты организма или клетки, с основанием или ферментом. Затем, после основного или ферментативного гидролиза полисахарид или олигосахарид можно выделить с помощью ряда методов. Неограничивающими примерами грамположительных бактерий и их рекомбинантных штаммов, подходящих для применения в соответствии с данным изобретением, являются Streptococci, Staphylococci, Enterococci, Bacillus, Corynebacterium, Listeria, Erysipelothrix и Clostridium. В частности, применение Streptococci является более предпочтительным, и применение типов Ia, Ib, II, III, IV, V и VIII Streptococci группы В является наиболее предпочтительным. Неограничивающие примеры грамотрицательных бактерий и их рекомбинантных штаммов, подходящих для применения в соответствии с данным изобретением, включают в себя Haemophilus influenzae, Neisseria meningitides, Escherichia coli, Salmonella typhi, Klebsiella pneumoniae Pseudomonas aeruginosa. В частности, применение Н. influenzae типа b, N. meningitides типов В, С, Y и W135, Е.coli K1 и Е.coli K92 является более предпочтительным. Примеры дрожжей, подходящих для применения в настоящем изобретении, включают в себя, не ограничиваясь ими, Cryptococcus neoformans. Примеры раковых клеток или раковых тканей, подходящих для применения в настоящем изобретении, включают в себя, не ограничиваясь ими, мелкоклеточную карциному легких, нейробластому, рак молочной железы, карциному ободочной кишки и т.п.
Для гидролиза полисахарида или олигосахарида в водном или органическом растворителе в соответствии с данным изобретением с помощью способов, известных в данной области, может использоваться широкий ряд условий. Степень гидролиза N-ацетильных связей углеводов может контролироваться с помощью условий реакции. В одном воплощении по меньшей мере приблизительно 50% N-ацетильных групп удаляют в результате гидролиза, предпочтительно удаляют приблизительно от 50% до 100%, более предпочтительно удаляют приблизительно 90% или более нативных N-ацетильных групп. В особом воплощении приблизительно 95% или более N-ацетильных групп полисахарида подвергают гидролизу путем обработки гидролизующим реагентом.
Капсульные полисахариды, которые экстрагируются в присутствии основания, представляют собой такие полисахариды, у которых отсутствует какой-либо неустойчивый к действию основания заместитель, который не может быть замещен, такой как O-ацетильные группы, необходимые для проявления иммуногенности. Другие капсульные полисахариды, которые экстрагируются в присутствии основания, представляют собой полисахариды, у которых отсутствует фосфодиэфирная связь и остатки уроновой кислоты, присоединенные по 4 положению.
В предпочтительном воплощении основного гидролиза КПС (капсульные полисахариды) экстрагируют из группы В Streptococci (GBS). В наиболее предпочтительном воплощении КПС экстрагируют из GBS типов Ia, Ib, II, III, V и VIII.
В другом предпочтительном воплощении основного гидролиза КПС экстрагируют из S.pneumoniae. В более предпочтительном воплощении основного гидролиза КПС экстрагируют из S.pneumoniae типов III, IV и XIV.
В другом предпочтительном воплощении основного гидролиза КПС экстрагируют из бактерий Neisseria или Escherichia. В более предпочтительном воплощении основной экстракции КПС экстрагируют из Neisseria meningitidis типов В, С, Y или W135, Escherichia coli K1 или Escherichia coli K92.
Полисахариды, которые подвержены ферментативному деацетилированию, представляют собой такие полисахариды, у которых отсутствует какой-либо неустойчивый к ферменту заместитель, необходимый для проявления иммуногенности, в которых заместитель не может быть заменен или замещен иммуногенным фрагментом, эти полисахариды включают в себя, не ограничиваясь ими, GBS и т.п.
А. Получение N-акрилоилированных полисахаридов
1. Деацетилирование полисахаридов
а) Исходные вещества
Полисахарид или олигосахарид может быть получен с помощью щелочного или ферментативного гидролиза из концентрированных бактериальных клеток, дрожжевых клеток или клеток млекопитающих, или рекомбинантных форм этих клеток, или из супернатантов гомогенизированных клеток, или из кондиционированной среды, с помощью стандартных методов, известных в данной области. Полисахарид или олигосахарид может быть выделен и очищен с помощью стандартных методов, известных в данной области. В качестве исходного вещества также может быть использован полисахарид или олигосахарид из коммерческих источников.
Методы выделения полисахарида зависят от конкретного использующегося полисахарида. Общим методом является использование ионного детергента для образования комплекса с заряженным полисахаридом. Этот комплекс осаждают и выделяют. Затем комплекс растворяют в растворе с высокой ионной силой, таком как раствор хлорида кальция, и затем полисахарид осаждают этанолом.
Выделенные и очищенные полисахариды и олигосахариды, полученные для использования в данном изобретении, предназначенные для применения для человека, предпочтительно содержат менее, чем 1% примесей нуклеиновых кислот и белка. Вследствие присутствия неорганических солей после очистки часто наблюдается чистота, степень которой составляет 80-100% углеводов.
b) Основной гидролиз
Для удаления N-ацетильных групп очищенные полисахариды или олигосахариды можно обработать основаниями. Неограничивающими примерами оснований, которые могут использоваться в соответствии с данным изобретением, являются NaOH, КОН, LiOH, NаНСО3, Na2CO3, К2СО3, KCN, Еt3N, NH3, H2N2H2, NaH, NaOMe, NaOEt или KOtBu. Такие основания, как NaOH, КОН, LiOH, NaH, NaOMe или KOtBu наиболее эффективно используются в интервале 0,5 N-5,0 N. Такие основания, как NaHCO3, Na2CO3, К2СО3 и KCN могут использоваться в таких высоких концентрациях, какие только допускает их растворимость. Органические основания, такие как Et3N, могут использоваться в среде в высоких (50-100%) концентрациях, пока присутствует такой агент, как вода или спирт, для воздействия на гидролиз. Такие основания как NH3 или H2N2H2 могут использоваться почти в любой концентрации, включая 100%. Можно использовать такие растворители, как вода, спирты (предпочтительно C1-C4), диметилсульфоксид, диметилформамид или смеси этих и других органических растворителей. Растворы оснований, включающие в себя воду, являются наиболее предпочтительными.
Интервал рН, наиболее эффективный для удаления N-ацетильных групп с полисахарида или олигосахарида, составляет приблизительно от 9 до 14, причем оптимальное значением рН составляет приблизительно 12. Затем N-деацетилированный полисахарид очищают от оставшихся реагентов путем ультраочистки с использованием мембран или диализа с помощью стандартных методов, известных в данной области.
с) Ферментативный гидролиз
Для ферментативного удаления N-ацетильных групп с полисахарида или олигосахарида можно использовать фермент N-деацетилазу. В одном из воплощений фермент N-деацетилазу используют для удаления N-ацетильных остатков с полисахаридов или олигосахаридов, как описано в ссылках 47, 48 и 49. При ферментативном гидролизе полисахарид или олигосахарид и фермент деацетилазу смешивают с соответствующей ферментативной буферной системой при соответствующих рН и температуре и оставляют взаимодействовать на период, достаточный для удаления N-ацетильных групп. Для получения N-деацетилированного полисахарида в одном из воплощений полисахарид и фермент N-деацетилазу смешивают с соответствующей ферментативной буферной системой, например 50 мМ MES, 10 мМ MnCl2, pH 6,3 при 37°С, в течение 60 минут. Реакцию останавливают с помощью соответствующего останавливающего раствора, например 1М монохлоруксусной кислоты, 0,5М NaOH, 2M NaCl, или путем разбавления соответствующим буферным раствором.
2. N-акрилоилирование полисахарида
Щелочной или ферментативный гидролиз полисахарида или олигосахарида приводит к удалению N-ацетильных групп с сиаловой кислоты и аминосахарных остатков полисахаридов или олигосахаридов. После гидролиза полисахарид или олигосахарид подвергают N-акрилоилированию до необходимой степени с помощью ряда акрилоилирующих агентов.
В одном воплощении этот способ включает в себя добавление акрилоилирующего реагента для N-акрилоилирования N-деацетилированного полисахарида или олигосахарида. Примеры акрилоилирующих реагентов включают в себя, не ограничиваясь ими, акрилоилхлорид, акрилоилангидрид, акриловую кислоту и дегидратирующий агент, такой как DCC, CH2CHCOCN и т.п., использующийся в избытке в концентрации, составляющей приблизительно 1М. В способе N-акрилоилирования N-деацетилированного полисахарида pH доводят до значения, находящегося в интервале приблизительно от 9 до 11, предпочтительно равного приблизительно 10, и поддерживают это значение в течение реакции. Температура в процессе реакции составляет приблизительно от 2°С до 8°С, предпочтительно приблизительно 4°С. Реакцию проводят в течение периода, составляющего приблизительно 1 час. Полученный N-акрилоилированный полисахарид или N-акрилоилированный олигосахарид является арилоилированным по меньшей мере на 95% или больше.
В. Получение конъюгатов β-пропионамидсвязанного полисахарида с белком
Полисахарид или олигосахарид данного изобретения при образовании конъюгата с другой иммуногенной молекулой, такой как полипептид или белок, может использоваться для индуцирозания в организме гуморального ответа на ряд грамотрицательных и грамположительных бактерий, дрожжей и раковых образований. Конъюгирование полисахарида или олигосахарида с полипептидом превращает иммунный ответ на полисахарид или олигосахарид, который обычно является Т-независимым, в Т-зависимый ответ. Соответственно, предпочтительный размер полипептида - это такой размер, который является достаточным для обеспечения превращения ответа из Т-независимого в Т-зависимый. С целью предоставления вторичного иммуногена может быть полезным использование более маленьких полипептидов. Молекулярная масса белка-носителя обычно составляет приблизительно от 50 000 до 500 000.
Предпочтительные белки-носители включают в себя, не ограничиваясь ими, столбнячный токсоид, дифтерийный токсоид, субъединицу В холерного токсина, белки внешней мембраны Neisseria meningitidis, С-β белок из Streptococcus группы В, С-β белок из Streptococcus группы В, не связывающий IgA, токсоид Pseudomonas aeruginosa, коклюшный токсоид, синтетический белок, содержащий остатки лизина или цистеина, и т.п. Белком-носителем может быть нативный белок, химически модифицированный белок, детоксифицированный белок или рекомбинантный белок. Молекулы конъюгатов, полученные в соответствии с данным изобретением, что касается белкового компонента, могут представлять собой мономеры, димеры, тримеры и молекулы с более высокой степенью сшивки.
Данное изобретение предоставляет возможность получать молекулы конъюгатов, в которых белок связан с полисахаридом или олигосахаридом через одно или несколько положений на полисахариде или олигосахариде. Размер полисахарида или олигосахарида может широко варьировать. Один или несколько полисахаридов или олигосахаридов может быть перекрестно связанным с одним или несколькими белками. Конъюгаты настоящего изобретения предпочтительно представляют собой решетчатые структуры. Точки присоединения находятся между остатками лизина или цистеина белка и N-акрилоильными группами полисахарида или олигосахарида.
В одном из способов получения иммуногенного полисахарид-белкового конъюгата выделенный полисахарид (глюкозаминогликан), у которого остатки сахара, составляющие его повторяющиеся единицы, содержат свободные аминогруппы или N-ацильные группы (например, N-ацетильные группы), вначале подвергают гидролизу с использованием основания или фермента для удаления части или всех его N-ацильных групп. Свободные аминогруппы затем подвергают N-ацилированию с помощью N-акрилоирующего реагента с образованием N-акрилоилированного полисахарида, описанного выше. Затем N-акрилоилированный полисахарид непосредственно присоединяют к белку в условиях оптимальных рН, температуры и времени для образования иммуногенного конъюгата β-пропионамидсвязанного полисахарида с белком.
В одном из воплощений для обеспечения оптимальной реакционной способности свободных ε-аминогрупп остатков лизина в белке конъюгирование проводят при рН выше 9,0, предпочтительно при рН, составляющем приблизительно от 9,0 до 10,0. В другом воплощении для обеспечения оптимальной реакционной способности тиоловых (SH) групп остатков цистеина в белке конъюгирование проводят при нейтральном рН, составляющем приблизительно 7,0. Выбор рН для осуществления способа конъюгирования может быть основан на количестве реакционноспособных групп в конкретном белке-носителе. Например, способ, в котором используют белок, составленный из более реакционноспособных остатков лизина по сравнению с остатками цистеина, предпочтительно проводят при основных значениях рН. Способ конъюгирования, в котором используют белок, составленный из более реакционноспособных остатков цистеина по сравнению с остатками лизина, предпочтительно проводят при нейтральных значениях рН.
Реакцию конъюгирования можно проводить в забуферивающих реагентах, включающих, но не ограничивающихся буферным реагентом, включающим карбонатный/бикарбонатный, боратный, фосфатный буфер и т.п. Температура реакции конъюгирования составляет по меньшей мере приблизительно 25°С, предпочтительно приблизительно 37°С, в течение периода, предпочтительно составляющего приблизительно 24 часа. Ключевая реакция включает 1,4-конъюгатное присоединение (по Михаэлю) нуклеофильных цистеиновых тиоловых групп или лизиновых ε-NH2 групп белков с N-акрилоилированными остатками сахаров, как описано Romanowska et al. (46), которые присутствуют в повторяющихся единицах полисахарида, как показано на чертеже. В полученном конъюгате β-пропионамидсвязанного полисахарида с белком соотношение полисахарида к белку составляет приблизительно от 0,1 до 0,6.
Гликозильные остатки полисахарида, имеющие N-ацильные группы, ответственные за непосредственное конъюгирование с остатками цистеина и/или лизина белка, включают в себя, не ограничиваясь ими, глюкозамин, галактозамин, маннозамин, фукозамин, сиаловые кислоты и т.п. Полисахарид может быть получен из таких природных источников, как бактериальные, дрожжевые или раковые клетки, или из синтетических источников. Синтетические источники включают в себя химический синтез, ферментативный синтез и хемоферментативный синтез. Синтез может представлять собой синтез de novo или модификацию природных углеводов. Выделенные природные углеводы могут быть модифицированы путем изменения функциональных групп углеводных остатков или путем добавления или удаления углеводных остатков.
Размер полисахарида или олигосахарида, предназначенного для применения в получении конъюгатов β-пропионамидсвязанного полисахарида и β-пропионамидсвязанного олигосахарида с белком настоящего изобретения, может варьировать при конъюгирования с белком-носителем. Как определено в данном документе, олигосахарид, предназначенный для применения в настоящем изобретении, включает в себя по меньшей мере 10 остатков сахаров и предпочтительно от 10 до 50 остатков сахаров. Полисахарид, как определено в данном документе, включает в себя более 50 остатков сахаров и может включать в себя около 600 или более остатков. В некоторых случаях для усиления иммуногенности требуются конъюгаты больших размеров. Способы данного изобретения обеспечивают применение полисахаридов очень большого размера, так как в один полисахарид можно ввести много реакционноспособных участков. Другим преимуществом данного способа по сравнению с предшествующим уровнем техники является то, что не происходит изменений в заряженных функциональных группах полисахарида или олигосахарида, которые часто взаимодействуют с эпитопом, ответственным за иммунитет, или образуют часть такого эпитопа.
С. Вакцины
Данное изобретение также направлено на получение вакцин. В соответствии с данным изобретением выделенные конъюгаты β-пропионамидсвязанного полисахарида с белком, описанные выше, могут быть использованы в качестве антигена, вызывающего образование антител, активных против полисахарида или олигосахарида и, следовательно, активных против организма или клетки, из которых был выделен этот полисахарид или олигосахарид. Вакцины настоящего изобретения могут представлять собой комбинационную или мультикомпонентную вакцину, дополнительно включающую в себя наряду с конъюгатом β-пропионамидсвязанного полисахарида с белком, другие компоненты, включающие в себя, но не ограничивающиеся ими, дифтерийно-столбнячно-коклюшную (DTP), столбнячно-дифтерийную (Тd), DTaP, DTap-Hib вакцины, DTap-IPV-Hib вакцину и т.п., и их сочетания, для предоставления мультифункциональной вакцины, использующейся для иммунизации против ряда организмов или клеток, вызывающих заболевания.
Вакцины данного изобретения могут обеспечивать активный или пассивный иммунитет. Вакцины, предназначенные для обеспечения активного иммунитета, включают в себя выделенный и очищенный N-акрилоилированный полисахарид или олигосахарид, конъюгированный по меньшей мере с одним антигенным пептидом.
D. Фармацевтические композиции
Фармацевтические композиции данного изобретения могут включать в себя по меньшей мере один полисахарид-белковый конъюгат и фармакологически приемлемые носители, такие как физиологический солевой раствор, декстрозу, глицерин, этанол или т.п. В другом воплощении фармацевтическая композиция включает в себя другой иммуногенный фрагмент, такой как пептид, или композиции, включающие в себя антитела, образование которых вызывается одним из КПС данного изобретения. Композиция может также включать в себя адъюванты для усиления иммунного ответа у реципиента. Такими адъювантами могут быть адъюванты на основе алюминия, такие как квасцы, или длинноцепочечные алкильные адъюванты, такие как стеарилтирозин (см. патент США с серийным №583 372, поданный 9/17/90; европейский патент, ЕР 0 549 617 B1; Moloney et al., патент США №4 258 029), мурамилдипептид (MDP) или его производное, монофосфориллипид A (MPL), сапонин (Quil-A) и т.п. См. также Jennings, et al., патент США №5 683 699 и Paoletti et al., J. Infectious Diseases 1997; 175:1237-9. Фармацевтическая композиция может также включать в себя один или несколько дополнительных иммуногенов, включающих в себя, но не ограничивающихся ими, дифтерийно-столбнячно-коклюшный (DTP), столбнячно-дифтерийный (Td), DTaP, DTaP-Hib, DTaP-IPV-Hib и т.п., и их сочетания. Особенно эти фармацевтические композиции могут применяться в качестве вакцин.
Для индуцирования пассивного иммунитета фармацевтическая композиция может включать в себя поликлональные или моноклональные антитела, их производные или фрагменты и их рекомбинантные формы. Количество антитела, фрагмента или производного является терапевтически или профилактически эффективным количеством, которое определяется с помощью стандартных клинических методик.
Лекарственные препараты данного изобретения могут быть введены субъекту с помощью методов, которые, как известно в данной области, являются эффективными. К ним относятся интрадермальный, интраперитонеальный, внутривенный, подкожный, внутримышечный, пероральный и интраназальный способы введения, но не только они.
Композиции данного изобретения могут включать в себя подходящие для вакцин стандартные носители, буферы или консерванты, известные специалистам в данной области, включающие в себя, не ограничиваясь ими, любой подходящий фармацевтически приемлемый носитель, такой как физиологический солевой раствор, или другие подходящие для инъекции жидкости. В вакцинах могут также присутствовать обычные добавочные агенты, например стабилизаторы, такие как лактоза или сорбит, и адъюванты для усиления иммунного ответа, такие как фосфат или гидроксид алюминия, или сульфат- и стеарилтирозин. Вакцины, полученные
в соответствии с данным изобретением, могут также использоваться в качестве компонентов мультивалентных вакцин, которые вызывают образование иммунного ответа против множества инфекционных агентов.
Вакцины настоящего изобретения вводят в количествах, достаточных для индуцирования продукции антител как составной части иммунного ответа. Для индуцирования продукции антител IgG и IgM вакцина может быть введена парентерально или может быть доставлена к мембранам слизистых оболочек для индуцирования продукции антител IgA на поверхности тканей. Дозировка может быть установлена на основании размера, веса или возраста субъекта, получающего вакцину. Гуморальный ответ у субъекта можно отслеживать путем анализа титра антител или бактерицидной активности и увеличивать его в случае необходимости усиления ответа. Обычно разовая доза для ребенка составляет приблизительно 10 мкг вакцины, включающей в себя конъюгат, на дозу или приблизительно 0,5 мкг-20 мкг/килограмм. Взрослые получают дозу, составляющую приблизительно 0,5-20 мкг/килограмм вакцины, включающей в себя конъюгат. Для вакцины, включающей в себя конъюгат КПС с белком, обычная доза составляет приблизительно 25 мкг каждого индивидуального КПС на дозу. То есть вакцина против streptococcus группы В может включать в себя 25 мкг каждого из КПС из каждого из девяти серотипов.
Е. Антитела
Образование антител против полисахарида может индуцироваться с помощью любого хорошо известного в данной области метода. В соответствии с одним из подходов образование антител может индуцироваться путем введения выделенного иммуногенного конъюгата β-пропионамидсвязанного полисахарида с белком животному-хозяину. Животным-хозяином могут быть крыса, мышь, отличные от человека приматы или человек, но этот список не является ограничивающим. Предпочтительно хозяином является человек. В одном из воплощений иммунологические ответы могут быть усилены путем применения известных в данной области адъювантов.
С помощью любого из хорошо известных в данной области методов могут быть также получены моноклональные антитела против полисахарида. В соответствии с одним из методов используют культуры гибридомных клеточных линий (Kohler and Milstein (1975) Nature 256: 495-497). Моноклональными антителами против полисахарида могут быть человеческие моноклональные антитела, химерные моноклональные антитела или гуманизированные моноклональные антитела, полученные с помощью любого из хорошо известных в данной области методов. В соответствии с одним из подходов могут быть получены химерные моноклональные антитела, которые содержат нечеловеческий (напр., мышиный) антигенсвязывающий домен, соединенный с человеческой константной областью (Takeda et al. (1985) Nature 314: 452). Гуманизированные антитела могут быть получены в соответствии с методиками Queen et al., патент США №5 585 089 и патент США №5 530 101. С помощью известных в данной области методов могут быть сконструированы одноцепочечные антитела (патент США №4 946 778; Davis, G.Т. et al., 1991 Biotechnology 9: 165-169; Pluckthun, A. 1990 Nature 347: 497-498). Домены константных областей антител могут быть модифицированы с помощью известных в данной области методов (WO 89/07142).
Антитела против полисахарида или олигосахарида могут быть очищены с помощью любой из хорошо известных в данной области методик, включающих в себя, не ограниваясь ими, иммуноабсорбционную или иммуноаффинную хроматографию или другие хроматографические методы (напр., ВЭЖХ). Антитела могут быть также выделены в виде иммуноглобулиновых фракций из сыворотки, плазмы или клеточной культуральной среды.
Молекулами антител данного изобретения могут являться интактные молекулы иммуноглобулинов, по существу интактные молекулы иммуноглобулинов или те фрагменты молекул иммуноглобулинов, например фрагменты Fab, которые содержат антигенсвязывающий участок. Молекулы антител могут принадлежать к любому классу, включая IgG, IgM и IgA.
Фрагменты антител против КПС могут быть получены с помощью любого из известных в данной области методов (Campbell (1985) Laboratory Techniques in Biochemistry and Molecular Biology, Vol. 13, Burdon, et al. (eds.), Elsevier Science Publishers, Amsterdam).
Антитело или его антигенсвязывающий фрагмент может использоваться в качестве терапевтического агента для обеспечения пассивной защиты от заболеваний, вызываемых грам(+), грам(-) бактериями или дрожжами. Антитело или его антигенсвязывающий фрагмент также может использоваться в качестве диагностического реагента в стандартном иммунологическом анализе для регистракции и/или идентификации бактерий, дрожжей или раковых клеток. Антитело может поставляться в виде только набора или вместе со стандартными реагентами для иммунологического анализа.
В другом воплощении данного изобретении антитела против полисахарида или олигосахарида данного изобретения могут использоваться в качестве лекарственного препарата в терапевтическом или профилактическом применении для передачи пассивного иммунитета субъекта-хозяина другому субъекту (т.е. для усиления иммунного ответа субъекта против грамположительных или грамотрицательных бактерий или дрожжей, или для обеспечения ответа у пациентов, имеющих риск иммунных заболеваний, или у паци