Ароматическая сульфонгидроксамовая кислота в качестве ингибитора металлопротеаз
Иллюстрации
Показать всеИзобретение относится к области медицины и касается способа лечения заболеваний, связанных с патологической активностью матриксных металлопротеаз, с помощью соединений формулы I, соединений формулы I, а также способа получения указанных соединений. Изобретение повышает эффективность лечения. 25 с. и 111 з.п. ф-лы, 152 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к ингибиторам протеиназ (протеаз) и, в частности, к применению производных ароматической сульфонгидроксамовой кислоты, которые, помимо прочего, являются избирательными ингибиторами матриксных металлопротеиназ, предназначенными для лечения состояний, связанных с патологической активностью матриксных металлопротеиназ, к самим избирательным ингибиторам, к композициям ингибиторов протеиназ, к промежуточным продуктам, предназначенным для синтеза ингибиторов протеиназ, и к способу получения ингибиторов протеиназ.
Предпосылки создания изобретения
Соединительная ткань, составляющие внеклеточного матрикса и базальные мембраны, являются необходимыми компонентами организма всех млекопитающих. Эти компоненты представляют собой биологический материал, который обеспечивает жесткость, дифференциацию, присоединение, а в некоторых случаях и эластичность биологических систем, включая организм человека и других млекопитающих. Компоненты соединительной ткани включают, например, коллаген, эластин, протеогликаны, фибронектин и ламинин. Они представляют собой биохимические составляющие или являются компонентами таких структур, как кожа, кость, зуб, сухожилие, хрящ, базальная мембрана, кровеносные сосуды, роговица и стекловидное тело.
В нормальных состояниях процессы превращения и/или репарации соединительной ткани контролируются и находятся в состоянии равновесия. Нарушение по какой-либо причине этого баланса приводит к многочисленным болезненным состояниям. Ингибирование ферментов, ответственных за нарушение равновесия, обеспечивает механизм контроля указанного разложения ткани и, следовательно, является средством лечения этих заболеваний.
Разложение соединительной ткани или компонентов соединительной ткани происходит под воздействием ферментов протеиназ, которые выделяются из расположенных в ткани клеток и/или из внедрившихся воспалительных или опухолевых клеток. Основным классом ферментов, осуществляющих эту функцию, являются зависимые от цинка металлопротеиназы (металлопротеазы).
Ферменты металлопротеазы подразделяют на классы, некоторые представители которых имеют несколько различных принятых названий. Их примерами являются коллагеназа I (матриксная металлопротеаза-1 (ММП-1), коллагеназа фибробластов, КФ 3.4.24.3), коллагеназа II (ММП-8, коллагеназа нейтрофилов, КФ 3.4.24.34), коллагеназа III (ММП-13), стромелизин 1 (ММП-3, КФ 3.4.24.17), стромелизин 2 (ММП-10, КФ 3.4.24.22), протеогликаназа, матрилизин (ММП-7), желатиназа А (ММП-2, желатиназа с молекулярной массой 72 кДа, коллагеназа базальной мембраны, КФ 3.4.24.24), желатиназа В (ММП-9, желатиназа с молекулярной массой 92 кДа, КФ 3.4.24.35), стромелизин 3 (МММ-11), металлоэластаза (ММП-12, ЧМЭ, эластаза макрофага человека) и мембранная ММП (ММП-14). ММП является аббревиатурой или акронимом от понятия "матриксная металлопротеаза", а присоединенные к этому акрониму цифры позволяют отличать друг от друга различных конкретных представитей групп ММП.
Неконтролируемое разложение соединительной ткани металлопротеазами является причиной многих патологических состояний. Их примерами являются ревматоидный артрит, остеоартрит, септический артрит, изъязвление роговицы, эпидермиса или желудка, периодонтит, протеинурия, болезнь Альцгеймера, коронарный тромбоз и заболевание кости. Также могут иметь место нарушения процессов репарации повреждения. Это может вызывать нарушение процесса заживления ран, приводящее к слабой репарации, сращению и рубцеванию. Последние из указанных нарушений могут привести к физическому недостатку и/или к временной потере трудоспособности, например к появлению спаек после хирургического вмешательства.
Металлопротеазы также участвуют в биосинтезе фактора некроза опухоли (TNF) и ингибируют продуцирование или активность TNF и родственных ему соединений, что является важным клиническим методом лечения болезней. Например, TNF-α представляет собой цитокин, который, как предполагается в настоящее время, первоначально продуцируется в виде связанной с клеткой молекулы с молекулярной массой 28 кДа. Затем происходит выделение активной формы с молекулярной массой 17 кДа, которая может обусловливать многочисленные вредные воздействия in vitro и in vivo. Например, TNF может вызывать и/или оказывать воздействия на воспалительные процессы, ревматоидный артрит, аутоиммунное заболевание, рассеянный склероз, отторжение трансплантата, фиброзные заболевания, рак, инфекционные болезни, малярию, инфекции, вызываемые микобактериями, менингит, лихорадку, псориаз, сердечно-сосудистые/легочные явления, такие как постишемическое перфузионное повреждение, застойная сердечная недостаточность, кровотечение, коагуляция, альвеолярное повреждение вследствие гипероксии, радиационное повреждение и острые фазы реакций типа тех, которые обнаруживаются при инфекциях и сепсисе и во время шока, например септического шока и гемодинамического шока. Хроническое выделение активного TNF может вызвать кахексию и анорексию. TNF может привести к смерти и одноврменно с этим TNF может помогать контролировать рост опухолевых клеток.
TNF-α -конвертаза представляет собой металлопротеазу, участвующую в образовании растворимого TNF-α . Ингибирование TNF-α -конвертазы (ТАСЕ) ингибирует продуцирование активного TNF-α . Соединения, которые ингибируют как активность ММП, так и производство TNF-α , описаны в WO 94/24140, WO 94/02466 и WO 97/20824. Установлено, что соединения, которые ингибируют такие ММП, как коллагеназа, стромелизин и желатиназа, также обладают способностью ингибировать выделение TNF (Gearing и др., Nature 376. 555-557 (1994), McGeehan и др.. Nature 376. 558-561 (1994)). Существует необходимость в эффективных ингибиторах ММП. Кроме того, сохраняется необходимость в агентах, являющихся эффективными ингибиторами TNF-α -конвертазы.
ММП также принимают участие в других биохимических процессах у млекопитающих. Они участвуют в регуляции овуляции, послеродовой инволюции матки, возможно, в имплантации, в расщеплении АПП (β -амилоидный предшественник протеина) с образованием амилоидной бляшки и в инактивации ингибитора α 1-протеазы (α 1-ПИ). Ингибирование этих металлопротеаз позволяет регулировать фертильность и лечить или предупреждать болезнь Альцгеймера. Кроме того, увеличение и сохранение уровней эндогенного или введенного лекарства, являющегося ингибитором серинпротеазы, или биохимического агента, такого как α 1-ПИ, способствует лечению или предупреждению таких болезней, как эмфизема, заболевания легких, воспалительные болезни и болезни, связанные со старением, такие как потеря упругости и эластичности кожи или органа.
Ингибирование определенных ММП также может оказаться целесообразным в других случаях. Лечение рака и/или ингибирование метастазов и/или ингибирование ангиогенеза являются примерами таких подходов к лечению болезней, когда избирательное ингибирование такого фермента или ферментов, как стромелизин, желатиназа А или В или коллагеназа III, вероятно, существенно более важно, чем ингибирование коллагеназы I (ММП-1). Лекарственное средство, которое не ингибирует коллагеназу I, может обладать наиболее ценным терапевтическим профилем. Еще одной важной болезнью, при которой разложение хряща в воспаленных суставах, вероятно, по меньшей мере частично обусловлено ММП-13, выделяющейся из таких клеток, как стимулированные хондроциты, является остеопороз, наибольший эффект при лечении которого может быть достигнут за счет применения лекарственных средств, одним из механизмов действия которых является ингибирование ММП-13 (см., например, Mitchell и др., J. Clin. Invest., 97: 761-768 (1996) и Reboul и др., J. Clin. Invest., 97: 2011-2019 (1996)).
Известен ряд ингибиторов металлопротеаз. Их примеры включают природные биохимические агенты, такие как тканевые ингибиторы металлопротеиназ (ТИМП), α 2-макроглобулин и их аналоги или производные. Эти эндогенные ингибиторы представляют собой молекулы протеинов с большой молекулярной массой, которые образуют неактивные комплексы с металлопротеазами. Описан целый ряд пептидоподобных соединений меньшего размера, которые ингибируют металлопротеазы. Установлено, что меркаптоамидпептидильные производные ингибируют АСЕ in vitro и in vivo. Ангиотензинпревращающий фермент (АСЕ) участвует в продуцировании ангиотензина II, соединения, являющегося эффективным сосудосуживающим агентом у млекопитающих, и ингибирование этого фермента приводит к снижению кровяного давления.
Ингибиторы металлопротеаз (ММП), представляющие собой амид- или пептидиламидсодержащие соединения, несущие тиольную группу, известны например, из WO 95/12389, WO 96/11209 и патента US 4595700. Ингибиторы ММП, несущие гидроксаматную группу, известны из многочисленных публикаций, таких как WO 95/29892, WO 97/24117, WO 97/49679 и ЕР 0780386, в которых описаны соединения, имеющие углеродный скелет, и в WO 90/05719, WO 93/20047, WO 95/09841 и WO 96/06074, в которых описаны гидроксаматы, имеющие пептидильные скелеты или пептидоподобные скелеты, и такие соединения также описаны в статьях Schwartz и др., Progr. Med. Chem., 29: 271-334 (1992), а также Rasmussen и др., Pharmacol. Ther., 75(1): 69-75 (1997) и Denis и др., Invest. New Drugs, 15(3): 175-185 (1997).
Одной из возможных проблем, связанных с известными ингибиторами ММП, является то, что такие соединения часто проявляют одинаковое или близкое ингибирующее действие в отношении всех ферментов ММП. Так, например, для соединения из класса пептидоподобных гидроксаматов, известного под названием батимастат, установлено, что значения IС50 составляют от примерно 1 до примерно 20 нмоль (нМ) в отношении каждой из таких ММП, как ММП-1, ММП-2, ММП-3, ММП-7 и ММП-9. Для маримастата, другого пептидоподобного гидроксамата, который является еще одним ингибитором широкого спектра ММП, установлено, что спектр его ингибирующей активности очень близок с таковым батимастата за исключением того, что значение IC50 маримастата в отношении ММП-3 составляет 230 нМ (Rasmussen и др., Pharmacol. Ther., 75(1): 69-75 (1997)).
Предварительный анализ данных, полученных на фазе I/II при исследовании пациентов, у которых в результате применения маримастата достигнуто успешное быстро прогрессирующее лечение плотных злокачественных опухолей (прямой кишки, поджелудочной железы, яичника, предстательной железы), показал зависящее от дозы уменьшение уровня карциномных антигенов, которые использовались в качестве косвенных маркеров биологической активности. Хотя маримастат и проявил определенный уровень активности в отношении этих маркеров, тем не менее при этом обнаружены побочные токсичные действия. Наиболее часто встречающимся связанным с лекарством токсичным действием маримастата, выявленным при клинических испытаниях, оказалась боль скелетных мышц и ригидность, часто затрагивающая небольшие суставы кистей рук, распространяясь далее на руку и плечо. Короткий перерыв в 1-3 недели в лечении с последующим уменьшением доз позволяет продолжить лечение (Rasmussen и др., Pharmacol. Ther., 75(1): 69-75 (1997)). Возможно, причиной этого является отсутствие специфического ингибирующего действия в отношении ММП.
В WO 98/38163, опубликованной 3 сентября 1998 г., описана большая группа ингибиторов ММП и ТАСЕ из класса гидроксаматов. Соединения, описанные в WO 98/38163, содержат один или два заместителя, соседних с функционально активным гидроксаматом, и заместитель, который может представлять собой ароматическую сульфонильную группу в соседнем положении по отношению к одному или к обоим этим заместителям.
В WO 98/37877, опубликованной 3 сентября 1998 г., описаны соединения, которые содержат 5-7-членное гетероциклическое кольцо в соседнем положении относительно функционально активного гидроксамата и могут содержать ароматическую сульфонильную группу по соседству с гетероциклическим кольцом.
Хотя многие из известных ингибиторов ММП, такие как батимастат, маримастат и гидроксаматы, описанные в WO 98/37877 и WO 98/38163, и обладают широким спектром активности в отношении ММП, однако эти соединения не обладают выраженным избирательным действием с точки зрения их ингибирующей активности. Это отсутствие избирательности может быть причиной боли скелетных мышц и ригидности, которые обнаружены при их применении. Кроме того, может оказаться терапевтически целесообразным применять лекарственное средство, которое является избирательным с точки зрения активности по сравнению с обычно применяемыми активными соединениями, чтобы лечение могло быть более точно направлено на патологическое состояние, имеющееся у хозяина-млекопитающего. Ниже описан способ лечения хозяина-млекопитающего, имеющего состояние, связанное с патологической активностью матриксных металлопротеаз, с использованием соединения, которое избирательно ингибирует одну или несколько ММП, но при этом является менее активным в отношении по крайней мере ММП-1.
Краткое изложение сущности изобретения
Настоящее изобретение относится к способу лечения, включающему введение хозяину-млекопитающему, который имеет состояние, связанное с патологической активностью матриксных металлопротеаз, эффективного количества рассматриваемой ароматической сульфонгидроксамовой кислоты, которая является ингибитором металлопротеаз. Рассматриваемая молекула проявляет, помимо прочего, очень высокую ингибирующую активность в отношении одного или большего количества ферментов металлопротеаз (ММП), таких как ММП-2, ММП-9 и ММП-13, но обладает существенно меньшей ингибирующей активностью по крайней мере в отношении ММП-1. Под понятием "существенно меньшая" подразумевают, что для рассматриваемого соединения в приведенном ниже в данном описании опыте по оценке ингибирования in vitro соотношение значений IС50 в отношении одной или нескольких ММП, таких как ММП-2, ММП-9 или ММП-13, и его значения IС50 в отношении ММП-1, например IС50 ММП-2, IС50 ММП-1, составляет менее примерно 1:10, предпочтительно менее примерно 1:100 и наиболее предпочтительно менее примерно 1:1000. Изобретение также относится к определенным соединениям, которые избирательно ингибируют активность одной или нескольких таких ММП, как ММП-2, ММП-9 и ММП-13, но обладают существенно меньшей ингибирующей активностью в отношении по крайней мере ММП-1, а также к композиции, содержащей такой ингибитор ММП в качестве действующего вещества. Изобретение также относится к промежуточным продуктам, предназначенным для получения рассматриваемой молекулы ароматической сульфонгидроксамовой кислоты, и к способу получения молекулы ароматической сульфонгидроксамовой кислоты.
В целом, одним из объектов настоящего изобретения является способ лечения, включающий введение эффективного количества рассматриваемой ароматической сульфонгидроксамовой кислоты, являющейся ингибитором металлопротеаз, которая избирательно ингибирует активность матриксных металлопротеаз, хозяину-млекопитающему, имеющему состояние, связанное с патологической активностью металлопротеаз. Применяемый ингибитор фермента имеет строение, представленное приведенной ниже формулой (I), или является его фармацевтически приемлемой солью:
где R1 и R2 оба обозначают гидрид или R1 и R2 вместе с атомами, к которым они присоединены, образуют 5-8-членное кольцо, содержащее в кольце один, два или три гетероатома, представляющих собой кислород, серу или азот.
R3 в формуле I обозначает необязательно замещенный арильный или необязательно замещенный гетероарильный радикал. Когда R3 обозначает замещенный арильный или гетероарильный радикал, то указанный заместитель выбирают из группы, включающей арил, гетероарил, аралкил, гетероаралкил, арилокси-, арилтио-, аралкокси-, гетероаралкоксигруппу, аралкоксиалкил, арилоксиалкил, аралканоилалкил, арилкарбонилалкил, аралкиларил, арилоксиалкиларил. аралкоксиарил, арилазоарил, арилгидразиноарил, алкилтиоарил, арилтиоалкил, алкилтиоаралкил, аралкилтиоалкил, аралкилтиоарил, сульфоксид или сульфон любого из тиозаместителей, и сконденсированную кольцевую структуру, включающую два или большее количество 5-6-членных колец, выбранных из группы, включающей арильный, гетероарильный, карбоциклический и гетероциклический радикалы.
Заместитель, связанный с арильным или гетероарильным радикалом, который включает радикал R3, сам может быть замещен одним или большим количеством заместителей; т.е. замещающий заместитель необязательно является замещенным. Когда арильный или гетероарильный радикал является замещенным и замещающий фрагмент (группа, заместитель или радикал) сам является замещенным, последний заместитель независимо друг от друга выбирают из группы, включающей цианогруппу, перфторалкил, трифторметокси-, трифторметилтиогруппу, галоалкил, трифторметилалкил, аралкоксикарбонил, арилоксикарбонил, гидроксигруппу, галоген, алкил, алкокси-, нитрогруппу, тиол, гидроксикарбонил, арилокси-, арилтиогруппу, аралкил, арил, арилкарбониламино-, гетероарилокси-, гетероарилтиогруппу, гетероаралкил, циклоалкил, гетероциклоокси-, гетероциклотио-, гетероциклоамино-, циклоалкилокси-, циклоалкилтио-, гетероаралкокси-, гетероаралкилтио-, аралкокси-, аралкилтио-, аралкиламино-, гетероциклогруппу, гетероарил, арилазо-, гидроксикарбонилалкокси-, алкоксикарбонилалкоксигруппу, алканоил, арилкарбонил, аралканоил, алканоилокси-, аралканоилоксигруппу, гидроксиалкил, гидроксиалкокси-, алкилтио-, алкоксиалкилтиогруппу, алкоксикарбонил, арилоксиалкоксиарил, арилтиоалкилтиоарил, арилоксиалкилтиоарил, арилтиоалкоксиарил, гидроксикарбонилалкокси-, гидроксикарбонилалкилтио-, алкоксикарбонилалкокси-, алкоксикарбонилалкилтио-, аминогруппу, где азот аминогруппы является (I) незамещенным или (II) замещенным одним или двумя заместителями, независимо друг от друга выбранными из группы, включающей алкил, арил, гетероарил, аралкил, циклоалкил, аралкоксикарбонил, алкоксикарбонил, арилкарбонил, аралканоил, гетероарилкарбонил, гетероаралканоил и алканоил, или (III) где азот аминогруппы и два присоединенных к нему заместителя образуют 5-8-членное гетероцикло- или гетероарильное кольцо, содержащее 0-2 дополнительных гетероатома, представляющих собой азот, кислород или серу, и само этот кольцо является (а) незамещенным или (б) замещенным одной или двумя группами, независимо друг от друга выбранными из группы, включающей арил, алкил, гетероарил, аралкил, гетероаралкил, гидрокси-, алкоксигруппу, алканоил, циклоалкил, гетероциклоалкил, алкоксикарбонил, гидроксиалкил, трифторметил, сконденсированный с бензольным кольцом гетероциклоалкил, гидроксиалкоксиалкил, аралкоксикарбонил, гидроксикарбонил, арилоксикарбонил, сконденсированную с бензольным кольцом гетероциклоалкоксигруппу, сконденсированный с бензольным кольцом циклоалкилкарбонил, гетероциклоалкилкарбонил и циклоалкилкарбонил, карбониламиногруппу,
где азот карбониламиногруппы является (I) незамещенным или (II) представляет собой реакционноспособный амин аминокислоты, или (III) является замещенным одним или двумя радикалами, выбранными из группы, включающей алкил, гидроксиалкил, гидроксигетероаралкил, циклоалкил, аралкил, трифторметилалкил, гетероциклоалкил, сконденсированный с бензольным кольцом гетероциклоалкил, сконденсированный с бензольным кольцом циклоалкил и N,N-диалкилзамещенную алкиламиноалкильную группу, или (IV) азот карбоксамидогруппы и два присоединенных к нему заместителя образуют 5-8-членное гетероцикло-, гетероарильное или сконденсированное с бензольным кольцом гетероциклоалкильное кольцо, которое само может быть незамещенным или может быть замещено одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей алкил, алкоксикарбонил, нитрогруппу, гетероциклоалкил, гидроксигруппу, гидроксикарбонил, арил, аралкил, гетероаралкил
и аминогруппу, где азот аминогруппы является (I) незамещенным или (II) замещенным одним или двумя заместителями, независимо друг от друга выбранными из группы, включающей алкил, арил и гетероарил. или (III) где азот аминогруппы и два присоединенных к нему заместителя образуют 5-8-членное гетероцикло- или гетероарильное кольцо,
и аминоалкильную группу где азот аминоалкила является (I) незамещенным или (II) замещенным одним или двумя заместителями, независимо друг от друга выбранными из группы, включающей алкил, арил, аралкил, циклоалкил, аралкоксикарбонил, алкоксикарбонил и алканоил, или (III) где азот аминоалкила и два присоединенных к нему заместителя образуют 5-8-членное гетероцикло- или гетероарильное кольцо.
В предпочтительном варианте осуществления R и R вместе с атомами, к которым они присоединены, образуют 6-членное кольцо.
Радикал R3 предпочтительно имеет длину, превышающую длину пентильной группы[-(СН2)4СН3-цепь] и более предпочтительно превышающую длину примерно гексильной группы[-(СН2)5СН3-цепь]. Радикал R3 предпочтительно имеет длину, меньшую чем длина икозильной группы[-(СН2)19CH3-цепь], и более предпочтительно длину, меньшую чем длина стеарильной группы[-(СН2)17СН3-цепь]. Предпочтительно группа R3 содержит 2 или большее количество 5-6-членных колец. Рассматриваемая группа R3 при вращении вокруг оси, проходящей через связанное с SO2 1-положение и связанное с заместителем 4-положение 6-членного кольца или через связанное с SO2 1-положение и связанное с заместителем 3-или 4-положение 5-членного кольца, образует трехмерное пространство, наибольший размер которого в направлении, перпендикулярном указанной оси вращения, равен длине от примерно одного фуранильного кольца до примерно двух фенильных колец.
Предпочтительно также, чтобы радикал R3 представлял собой арильную или гетероарильную группу с одним кольцом, которая является 5- или 6-членной и сама замещена в ее 4 положении, когда она представляет собой 6-членное кольцо, или в ее 3 или 4 положении, когда она представляет собой 5-членное кольцо, необязательно замещенным заместителем, выбранным из группы, включающей другую арильную или гетероарильную группу с одним кольцом, С3-С14алкильную группу, N-пиперидильную группу, N-пиперазильную группу, феноксигруппу, тиофеноксигруппу, 4-тиопиридильную группу, фенилазогруппу и бензамидогруппу. Заместитель 5- или 6-членной арильной или гетероарильной группы сам может быть замещен, как указано выше.
Предпочтительное соединение, предназначенное для применения в рассматриваемом способе, имеет строение, соответствующее приведенной ниже формуле II, или является его фармацевтически приемлемой солью:
где
R14 обозначает гидрид, фармацевтически приемлемый катион или C(W)R5, где W обозначает О или S, а R15 выбирают из группы, включающей С1-С6алкил, арил, С1-С6алкоксигруппу, гетероарилС1-С6алкил, С3-С8 циклоалкил-С1-С6алкил, арилокси-, арС1-С6алкоксигруппу, арС1-С6алкил, гетероарил и аминоС1-С6алкил, где азот аминоалкила является (I) незамещенным или (II) замещенным одним или двумя заместителями, независимо друг от друга выбранными из группы, включающей С1-С6алкил, арил, арС1-С6алкил, С3-С8циклоалкил-С1-С6алкил, арС1-С6алкоксикарбонил, С1-С6алкоксикарбонил и С1-С6алканоил, или (III) азот аминоС1-С6алкильной группы и два присоединенных к нему заместителя образуют 5-8-членное гетероцикло- или гетероарильное кольцо,
m равно 0, 1 или 2,
n равно 0, 1 или 2
р равно 0, 1 или 2,
сумма m+n+p равна 1, 2, 3 или 4,
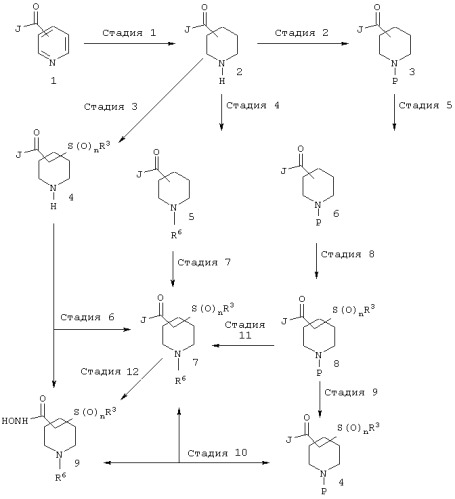
(а) один из заместителей X, Y и Z выбирают из группы, включающей С(O), NR6, О, S, S(O), S(O)2 и NS(O)2R7, а два остальных заместителя из группы, включающей X, Y и Z, обозначают CR8R9 и CR10R11, или
(б) Х и Z или Z и Y вместе образуют фрагмент, который выбирают из группы, включающей NR6C(O), NR6S(O), NR6S(O)2, NR6S, NR6O, SS, NR6NR6 и ОС(O), при этом один оставшийся заместитель из группы, включающей X, Y и Z, обозначает CR8R9, или
(в) n равно 0 и X, Y и Z вместе образуют фрагмент, выбранный из группы, включающей
где
волнистые линии обозначают связи с атомами изображенного кольца, R6 и R6' независимо друг от друга выбирают из группы, включающей гидрид, С1-С6алканоил, С6арил-С1-С6алкил, ароил, бис(С1-С6алкокси-С1-С6алкил)-С1-С6алкил, С1-С6алкил, С1-С6галоалкил, С1-С6лерфторалкил, С1-С6трифторметилалкил, С1-С6перфторалкокси-С1-С6алкил, С1-С6алкокси-С1-С6алкил, С3-С6циклоалкил, С3-С8гетеропиклоалкил, С3-С8гетероциклоалкилкарбонил, С6арил, С5-С6гетероцикло, С5-С6гетероарил, С3-С8циклоалкил-С1-С6алкил, С6арилокси-С1-С6алкил, гетероарилоксиС1-С6алкил, гетероарилС1-С6алкоксиС1-С6алкил, гетероарилтиоС1-С6алкил, С6арилсульфонил, С1-С6алкилсульфонил, С5-С6гетероарилсульфонил, карбоксиС1-С6алкил, С1-С4 алкоксикарбонил-С1-С6алкил, аминокарбонил, С1-С6алкилиминокарбонил, С1-С6арилиминокарбонил, С1-С6гетероциклоиминокарбонил, С6арилтио-С1-С6алкил, С1-С6алкилтио-С1-С6алкил, С6арилтио-С3-С6алкенил, С1-С4алкилтио-С3-С6алкенил, С5-С6гетероарил-С1-С6алкил, галоС1-С6алканоил, гидроксиС1-С6алканоил, тиолС1-С6алканоил, С3-С6алкенил, С3-С6алкинил, С1-С4алкокси-С1-С4алкил, С1-С5алкоксикарбонил, арилоксикарбонил, NR8R9-С1-С5алкилкарбонил, гидроксиС1-С5алкил, аминокарбонил, где азот в аминокарбониле является (I) незамещенным или (II) замещенным одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей С1-С6алкил, арС1-С6алкил, С3-С8циклоалкил и С1-С6алканоил, гидроксиаминокарбонил, аминосульфонил, где азот в аминосульфонильной группе является (I) незамещенным или (II) замещенным одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей С1-С6алкил, apС1-С6алкил, С3-С8циклоалкил и С1-С6алканоил, аминоС1-С6алкилсульфонил, где азот аминоС1-С6алкилсульфонильной группы является (I) незамещенным или (II) замещенным одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей С1-С6алкил, apС1-С6алкил, С3-С8циклоалкил и С1-С6алканоил, и аминоС1-С6алкил, где азот аминоалкильной группы является (I) незамещенным или (II) замещенным одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей С1-С6алкил, арС1-С6алкил, С3-С8циклоалкил и С1-С6алканоил,
R7 выбирают из группы, включающей арилалкил, арил, гетероарил, гетероциклогруппу, С1-С6алкил, С3-С6алкинил, С3-С6алкенил, С1-С6карбоксиалкил и С1-С6гидроксиал,
R8 и R9, и R10, и R11 независимо друг от друга выбирают из группы, включающей гидрид, гидроксигруппу, С1-С6алкил, арил, арС1-С6алкил, гетероарил, гетероарС1-С6алкил, С2-С6алкинил, С2-С6алкенил, тиолС1-С6алкил, С1-С6алкилтио-С1-С6алкил, циклоалкил, циклоалкилС1-С6алкил, гетероциклоалкилС1-С6алкил, С1-С6алкокси-С1-С6алкил, аралкоксиС1-С6алкил, С1-С6алкокси-С1-С6алкокси-С1-С6алкил, гидроксиС1-С6алкил, гидроксикарбонилС1-С6алкил, гидроксикарбониларС1-С6алкил, аминокарбонилС1-С6алкил, арилоксиС1-С6алкил, гетероарилоксиС1-С6алкил, арилтиоС1-С6 алкил, гетероарилтиоС1-С6алкил, сульфоксид или сульфон любого из этих тиозаместителей, перфторС1-С6алкил, трифторметилС1-С6алкил, галоС1-С6алкил, алкоксикарбониламиноС1-С6алкил и аминоС1-С6алкил, где азот аминоалкильной группы является (I) незамещенным или (II) замещенным одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей С1-С6алкил, apС1-С6алкил, циклоалкил и С1-С6алканоил, или где R8 и R9 или R10 и R11 вместе с атомами, к которым они присоединены, образуют карбонильную группу, или R8 и R9 или R10 и R11, или R8 и R10 вместе с атомами, к которым они присоединены, образуют 5-8-членное карбоциклическое кольцо или 5-8-членное гетероциклическое кольцо, содержащее один или два гетероатома, которые представляют собой азот, кислород или серу, при условии, что только один из радикалов R8 и R9 или R10 и R11 обозначает гидроксигруппу,
R12 и R12' независимо друг от друга выбирают из группы, включающей гидрид, С1-С6алкил, арил, арС1-С6алкил, гетероарил, гетероаралкил, С1-С6алкинил, С1-С6алкенил, тиолС1-С6алкил, циклоалкил, циклоалкилС1-С6алкил, гетероциклоалкилС1-С6алкил, С1-С6алкокси-С1-С6алкил, аралкоксиС1-С6алкил, аминоС1-С6алкил, С1-С6алкокси-С1-С6алкокси-С1-С6алкил, гидроксиС1-С6алкил, гидроксикарбонил С1-С6алкил, гидроксикарбониларС1-С6алкил, аминокарбонилС1-С6алкил, арилоксиС1-С6алкил, гетероарилоксиС1-С6алкил, С1-С6алкилтио-С1-С6алкил, арилтиоС1-С6алкил, гетероарилтиоС1-С6алкил, сульфоксид или сульфон любого из этих тиозаместителей, перфторС1-С6алкил, трифторметилС1-С6алкил, галоС1-С6алкил, алкоксикарбониламиноС1-С6алкил и аминоС1-С6алкил, где азот аминоалкильной группы является (I) незамещенным или (II) замещенным одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей С1-С6алкил, арС1-С6алкил, циклоалкил и С1-С6алканоил,
R13 выбирают из группы, включающей гидрид, бензил, фенил, С1-С6алкил, С1-С6алкинил, С2-С6алкенил и С1-С6гидроксиалкил, и
G-A-R-E-Y представляет собой заместитель, который предпочтительно имеет длину, превышающую длину пентильной группы, и более предпрочтительно имеет длину, превышающую длину гексильной группы. Заместитель G-A-R-E-Y предпочтительно имеет длину, меньшую чем длина икозильной группы, и более предпочтительно меньшую чем длина стеарильной группы.
В этом заместителе G обозначает арильную или гетероарильную группу;
А выбирают из группы, включающей
(1) -О-,
(2) -S-,
(3) -NR17-,
(4) -CO-NR17-или-NR17-CO-, где R17 обозначает водород, С1-С4алкил или фенил,
(5) -СО-O- или -O-СО-,
(6) -O-СО-О-,
(7) -НС=СН-,
(8) -NH-CO-NH-,
(9) -С=С-,
(10) -NH-CO-O-или-O-CO-NH-,
(11) -N=N-.
(12) -NH-NH-и
(13) -CS-N(R18)-или-N(R18)-CS-, где R18 обозначает водород, С1-С4алкил или фенил, или
(14) А отсутствует, a G непосредственно присоединен к R,
R обозначает фрагмент, выбранный из группы, включающей алкил, алкоксиалкил, арил, гетероарил, циклоалкил, гетероциклоалкил, аралкил, гетероаралкил, гетероциклоалкилалкил, циклоалкилалкил, циклоалкоксиалкил, гетероциклоалкоксиалкил, арилоксиалкил, гетероарилоксиалкил, арилтиоарил, гетероарилтиоарил, циклоалкилтиоалкил и гетероциклоалкилтиоалкил, где арильный или гетероарильный, или циклоалкильный, или гетероциклоалкильный заместитель является (I) незамещенным или (II) замещенным одним или двумя радикалами, выбранными из группы, включающей галоген, алкил, перфторалкил, перфторалкокси-, перфторалкилтиогруппу, трифторметилалкил, аминогруппу, алкоксикарбонилалкил, алкокси-, С1-С2алкилендиоксигруппу, гидроксикарбонилалкил, гидроксикарбонилалкиламино-, нитро-, гидроксигруппу, гидроксиалкил, алканоиламиногруппу и алкоксикарбонил, и R не обозначает алкил или алкоксиалкил, когда А обозначает -О- или -S-,
Е выбирают из группы, включающей
(1) -CO(R19)- или -(R19)СО-, где R19 обозначает гетероциклоалкил или циклоалкил,
(2) -CONH-или-HNCO-,
(3) -СО-,
(4) -SO2-R19- или -R19-SO2-,
(5) -SO2- и
(6) -NH-SO2- или -SO2-NH, или
(7) Е отсутствует и R непосредственно присоединен к Y, и Y отсутствует или его выбирают из группы, включающей гидрид, алкил, алкоксигруппу, галоалкил, арил, аралкил, циклоалкил, гетероарил, гидрокси-, арилокси-, аралкокси-, гетероарилоксигруппу, гетероаралкил, перфторалкокси-, перфторалкилтиогруппу, трифторметилалкил, алкенил, гетероциклоалкил, циклоалкил, трифторметил, алкоксикарбонил и аминоалкил, где арильная или гетероарильная, или гетероциклоалкильная группа является (I) незамещенной или (II) замещенной одним или двумя радикалами, независимо друг от друга выбранными из группы, включающей алканоил, галоген, нитрогруппу, аралкил, арил, алкокси- и аминогруппу, где азот в аминогруппе является (I) незамещенным или (II) замещенным одним или двумя группами, независимо друг от друга выбранными из группы, включающей гидрид, алкил и аралкил. Особенно предпочтительное соединение, предназначенное для применения в предлагаемом способе, имеет строение, соответствующее приведенной ниже формуле III, или представляет собой его фармацевтически приемлемую соль:
где m, n, р, X, Z, Y и R14 имеют значения, указанные выше для формулы II, а значения радикала R, которые приведены ниже, представляют собой подгруппу значений, приведенных ранее для заместителей G-A-R-E-Y.
Таким образом, R3 обозначает радикал, включающий арильную или гетероарильную группу с одним кольцом, которая является 5- или 6-членной и сама замещена в 4-положении, когда она представляет собой 6-членное кольцо, и в 3- или в 4-положении, когда она представляет собой 5-членное кольцо, заместителем, выбранным из группы, включающей тиофенокси-, 4-хлорфенокси-, 3-хлорфенокси-, 4-метоксифенокси-, 3-бензодиоксол-5-илокси-, 3,4-диметилфенокси-, 4-фторфенокси-, 4-фтортиофенокси-, фенокси-, 4-трифторметоксифенокси-, 4-трифторметилфенокси-, 4-(трифторметилтио)фенокси-, 4-(трифторметилтио) тиофенокси-, 4-хлор-3-фторфенокси-, 4-изопропоксифенокси-, 4-изопропилфенокси-, (2-метил-1,3-бензотиазол-5-ил)окси-, 4-(1Н-имидазол-1-ил)фенокси-, 4-хлор-3-метилфенокси-, 3-метилфенокси-, 4-этоксифенокси-, 3,4-дифторфенокси-, 4-хлор-3-метилфенокси-, 4-фтор-3-хлорфенокси-, 4-(1Н-1,2,4-триазол-1-ил)фенокси-, 3,5-дифторфенокси-, 3,4-дихлорфенокси-, 4-циклопентилфенокси-, 4-бром-3-метилфенокси-, 4-бромфенокси-, 4-метилтиофенокси-, 4-фенилфенокси-, 4-бензилфенокси-, 6-хинолинилокси-, 4-амино-3-метилфенокси-, 3-метоксифенокси-, 5,6,7,8-тетрагидро-2-нафталинилокси-, 3-гидроксиметилфеноксигруппу, N-пиперидил, N-пиперазинил и 4-бензилоксифеноксигруппу.
Более предпочтительное соединение, предназначенное для применения в предлагаемом способе, имеет строение, соответствующее приведенной ниже формуле IV, или представляет собой его фармацевтически приемлемую соль:
где R3 имеет значения, указанные выше для формулы I, более предпочтительно указанные для формулы II (где эта группа R3 представляет собой заместитель G-A-R-E-Y), и более предпочтительно также значения, указанные для формулы III, и Z выб