Способ получения сульфатов двух-, трех- и четырехвалентного марганца или их смесей
Иллюстрации
Показать всеИзобретение относится к технологии получения сульфатов марганца разной степени окисления. Сульфаты двух-, трех- и четырехвалентного марганца или их смеси получают взаимодействием оксидов марганца MnO, Mn2O3, Mn3O4 и MnO2 любого происхождения с концентрированной серной кислотой. Взаимодействие проводят в бисерной мельнице вертикального типа со стеклянным бисером диаметром 1,5-2 мм, в которую последовательно вводят нереагирующий с концентрированной серной кислотой растворитель, марганецсодержащий реагент и серную кислоту. Используют марганецсодержащий реагент, измельченный до размеров частиц 1 мм и менее и 79,8-90%-ную серную кислоту в мольном стехиометрическом избытке в отношении марганецсодержащего реагента 1,20-1,72. Далее включают бисерную мельницу и ведут процесс при 5-25°С в течение 5-10 мин при соотношении масс растворителя и реагентов 2,33:1-10:1. Растворитель отделяют от бисера и продукта фильтрованием. Локализованный в виде пленки в основном на поверхности бисера и частично стенках реактора сульфат марганца или смесь сульфатов растворяют в серной кислоте соответствующей концентрации либо вводят в новый процесс, проводимый в этой же бисерной мельнице, с сульфатом марганца (III) или (IV) в качестве окислителя. Техническим результатом является быстрое и количественное взаимодействие оксидов марганца с концентрированной серной кислотой при комнатных температурах в условиях тонкого перетира твердой фазы в бисерной мельнице. 1 з.п. ф-лы, 2 табл.
Реферат
Изобретение относится к технологии получения сульфатов марганца разной степени окисления, в том числе и из природных материалов, и может быть использовано в отраслях применения этих соединений в качестве селективных окислителей, катализаторов, сырья для получения иных соединений, а также при первичной переработке марганцевых руд.
Известно, что сульфаты двух-, трех- и четырехвалентного марганца, получают в результате воздействия серной кислоты разной концентрации на определенные соединения марганца в отсутствие или же в присутствии дополнительных окислителей или же восстановителей (Реми Г. Курс неорганической химии. Т.2. М.: Мир, 1966, 836 с.).
Известен способ извлечения марганца из марганецсодержащих окисленных руд (а.с. СССР №1054302), включающий обработку исходной руды галогенводородной кислотой в смеси с серной кислотой при молярном отношении окислов марганца высших степеней окисления в пересчете на МnO2 к галогенводородной кислоте 0,45-0,6, окислов марганца всех форм в пересчете на марганец к серной кислоте 0,8-1,1 и концентрации ионов SO
| 2- |
| 4 |
МnО+Н2SO4→MnSO4+Н2O
Мn3O4+2НВr+3H2SO4→3MnSO4+Br2+4Н2О
Мn2O3+2НВr+2H2SO4→2MnSO4+Br2+3Н2O
МnO2+2HBr+H2SO4→MnSO4+Br2+2H2O
т.е. бромистоводородная кислота в данной системе выступает как восстановитель. Поэтому одной из целей данного изобретения является повышение выхода галогена.
Известен способ получения соединений трехвалентного марганца (а.с. СССР №442150), в соответствии с которым окисление соединений двухвалентного марганца осуществляют путем обработки его кислым экстрагентом - раствором органической кислоты в керосине с последующей реэкстракцией соединений трехвалентного марганца водным раствором неорганической кислоты, например фосфорной, пирофосфорной или серной. При этом в качестве органической кислоты используют жирные кислоты с числом атомов углерода С7-С9, нафтеновые или смоляные кислоты.
Наиболее близким к заявляемому является способ получения сульфатов двух-, трех- и четырехвалентного марганца или их смесей путем прямого взаимодействия оксидов марганца МnО, Мn2О3, Мn3O4 и MnO2 любого происхождения или марганецсодержащих минералов с концентрированной серной кислотой (Лидин Р.А. и др. Химические свойства неорганических веществ. М.: Химия, 1996, c.396-402).
Недостатком указанного способа является то, что для превращения каждого марганецсодержащего сырья в соответствующий сульфат марганца требуются существенно разные условия, при этом проводимый процесс часто в той или иной степени сопровождается изменением валентного состояния марганца, что существенно снижает его селективность. Так, например, оксид марганца (III) и метагидроксид марганца превращаются в сульфат марганца (III) при обработке холодной 50%-ной серной кислотой. Получать сульфат марганца (IV) аналогичным способом с использованием более концентрированной серной кислоты уже не удается, поскольку с холодной кислотой процесс не идет, а при нагревании до 110° С основными продуктами являются Мn2(SO4)3 и О2 (газ). Mn(SO4)2 удается получать окислением сульфата марганца (II) перманганатом калия в среде концентрированной серной кислоты. В целом же частичное или полное изменение валентного состояния марганца в сырье при образовании марганецсодержащих продуктов явление обычное для рассматриваемого способа.
Задача предлагаемого решения заключается в том, чтобы сделать возможным быстрое и количественное превращение в соответствующие валентному состоянию марганца в исходном сырье сульфаты оксидов и карбонатов марганца, в том числе и природного происхождения, во взаимодействии с концентрированной серной кислотой при комнатных температурах в условиях тонкого перетира твердой фазы в бисерной мельнице.
Поставленная задача достигается тем, что в бисерную мельницу вертикального типа со стеклянным приводимым во вращение и иные перемещения лопастной мешалкой бисером диаметром 1,5-2 мм вводят нереагирующий с серной кислотой растворитель, марганецсодержащее твердое предварительно измельченное до размеров частиц 1 мм и менее сырье и концентрированную (79,8-90%) серную кислоту в мольном стехиометрическом избытке в отношении марганецсодержащего реагента 1,20-1,72, включают бисерную мельницу и ведут процесс при 5 -25°С в течение 5-10 мин при исходном соотношении масс растворителя и реагентов 2,33:1-10:1, после чего растворитель отделяют от бисера и продукта фильтрованием, а локализованный в виде пленки в основном на поверхности бисера и частично стенках реактора сульфат марганца или смесь сульфатов растворяют в серной кислоте соответствующей концентрации, либо вводят в новый процесс, проводимый в этой же бисерной мельнице с сульфатом марганца (III) или (IV) в качестве окислителя. При этом в качестве растворителя используют кипящий ниже 100° С низкомолекулярный парафиновый углеводород или же смесь этих углеводородов.
Характеристика используемого сырья.
МnО2 природный (марганец окись, водная ГОСТ 4470-70), технический (по ТУ 6-10-1808-81), реактивный (ТУ 6-09-2962-78), отходы витаминной промышленности (искусственная паста по ТУ 6-14-831-72).
Мn2O3 реактивный (ТУ 6-09-3364-78) либо полученный при сжигании ацетата марганца (II) в муфельной печи в интервале температур 600±20° С.
Мn3O4, полученный при сжигании искусственной пасты МnО2 при температуре 960±15° С при ограниченном доступе воздуха.
Марганецсодержащие минералы: родохрозит формулы МnСО3; манганизит формулы МnО; манганит формулы МnO3·Н2О; гаусманит формулы Мn3O4; браунит формулы 3MnO2·4MnO· SiO2 (содержание Мn2O3 - 78,3%; МnО -11,7%; SiO2 - 10%).
Серная кислота концентрированная (ГОСТ 14262-78)
Гексан МРТУ 6-09-2937-66
Гептан эталонный (ТУ 6-09-4520-77)
Петролейный эфир ГОСТ 11992-66
Получение сульфатов двух-, трех-, четырехвалентного марганца или их смесей заключается в следующем. В бисерную мельницу вертикального типа со стеклянным бисером в качестве перетирающего агента последовательно загружают парафиновый растворитель, марганецсодержащее сырье и серную кислоту в расчетных количествах и соотношениях. Включают бисерную мельницу и проводят процесс в течение 5-10 мин.
По истечении указанного времени перетир прекращают и сливают растворитель через нижний сливной патрубок с фильтровальной перегородкой на входе, имеющей размеры ячеек не более 0,5-1 мм. Оставшийся на бисере и стенках реактора сульфат марганца или же смесь сульфатов растворяют в серной кислоте соответствующей концентрации, либо в бисерную мельницу загружают содержащую восстановитель новую реакционную смесь для проведения целевого окислительно-восстановительного процесса с сульфатом марганца (III) или (IV) в качестве окислителя. При необходимости остатки парафинового растворителя целевого процесса удаляют путем продувки через бисерную мельницу воздуха либо другого газа.
Пример 1.
В лабораторную бисерную мельницу вертикального типа с 250 г стеклянного бисера диаметром 1,5-2 мм в качестве перетирающего агента, приводимого во вращение и иные перемещения лопастной мешалкой (n=1440 об/мин), вводят 227 г гептана, 4,48 г измельченного до размеров частиц 1 мм и менее реактивного МnO2 и 18,22 г 83%-ной серной кислоты при температуре 11,5° С. Включают бисерную мельницу и ведут трибохимический процесс в течение 5 мин. За это время температура в зоне реакции практически не меняется и достигается практически количественное расходование МnO2. Останавливают перемешивание в бисерной мельнице, открывают запорный кран на сливном патрубке, на входе которого расположена фильтровальная перегородка с диаметром отверстий 0,5-1 мм, и сливают растворитель в специально предназначенную емкость. Анализ проб растворителя показывает отсутствие в нем как компонентов загрузки, так и продуктов превращения. Практически нет и измельченной твердой фазы, которая полностью осталась в виде пленки сульфата Mn(IV) на поверхности бисера и частично на стенках стакана бисерной мельницы. Степень превращения МnO2 превысила 99%.
Закрывают кран сливного патрубка, вводят 7 г салицилового альдегида, 200 г гептана и 0,075 моля бромоводородной кислоты, включают перемешивание и ведут новый окислительно-восстановительный процесс до практически полного израсходования Мn(SO4)2 как окислителя. На достижение 97,8%-ной степени расходования сульфата марганца (IV) потребовалось в выбранных условиях при 17° C 54 мин.
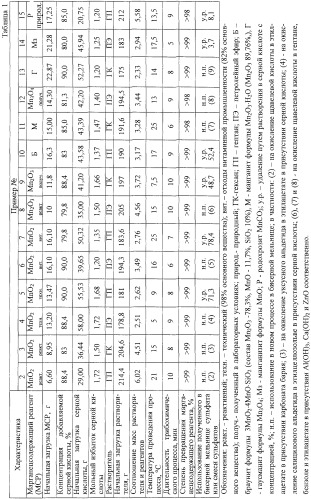
Примеры 2-15.
Оборудование и порядок проведения процесса аналогичны описанным в примере 1. Отличаются природой используемого марганецсодержащего реагента и растворителя, концентрацией серной кислоты и ее мольным избытком, температурой и длительностью проведения основного процесса, соотношением масс загружаемых растворителя и реагентов и способом удаления получаемого продукта из бисерной мельницы. Все эти данные сведены в табл.1.
Примеры 16-30.
Марганецсодержащий реагент, оборудование и порядок проведения процесса аналогичны описанным в примере 13. Отличаются скоростью вращения механической мешалки, размерами используемого бисера, соотношением масс бисера и загрузки, а также фракционным составом марганецсодержащего реагента. Полученные результаты сведены в табл.2.
Положительный эффект предлагаемого решения состоит в следующем:
1. Процесс прост в исполнении и не требует никаких вспомогательных и дополнительных веществ, кроме представленной парафиновым углеводородом жидкой фазы.
2. Процесс протекает быстро и в чрезвычайно мягких температурных условиях. Ему не нужен ни дополнительный подвод, ни отвод тепла, что существенно упрощает технологическую схему и конструкцию реакционного аппарата.
3. Получаемые продукты твердые и практически нерастворимые в жидкой фазе системы. Но они легко локализуются на твердых поверхностях (в основном перетирающего агента) и довольно прочно удерживаются в таком виде. Более того, на этих же поверхностях не без участия продукта надежно удерживается и избыточная серная кислота, а также реакционная вода. Следовательно, при практически количественном превращении марганецсодержащего реагента имеет место самоотделение жидкой фазы (растворителя), которую остается просто слить и без всякой очистки использовать многократно.
4. Конечное состояние продукта предоставляет выбор его использования в новом окислительно-восстановительном процессе без выноса из бисерной мельницы, либо удаление из бисерной мельницы с помощью подходящего растворителя (серной кислоты определенной концентрации для сульфатов марганца (III) и (IV) или разбавленной кислоты, а то и просто воды для сульфата марганца (II)).
1. Способ получения сульфатов двух-, трех- и четырехвалентного марганца или их смесей путем прямого взаимодействия оксидов марганца МnО, Мn2О3, Мn3O4 и MnO2 любого происхождения или марганецсодержащих минералов с концентрированной серной кислотой, отличающийся тем, что данное взаимодействие проводят в бисерной мельнице вертикального типа со стеклянным бисером диаметром 1,5-2 мм, приводимым во вращении и иные перемещения лопастной мешалкой, куда последовательно вводят не реагирующий с концентрированной серной кислотой растворитель, марганецсодержащий предварительно измельченный до размеров частиц 1 мм и менее реагент и 79,8÷90%-ную серную кислоту в мольном стехиометрическом избытке в отношении марганецсодержащего реагента 1,20÷1,72, включают бисерную мельницу и ведут процесс при 5-25°С в течение 5-10 мин при соотношении масс растворителя и реагентов 2,33:1÷10:1, после чего растворитель отделяют от бисера и продукта фильтрованием, а локализованный в виде пленки в основном на поверхности бисера и частично стенках реактора сульфат марганца или смесь сульфатов растворяют в серной кислоте соответствующей концентрации либо вводят в новый процесс, проводимый в этой же бисерной мельнице, с сульфатом марганца (III) или (IV) в качестве окислителя.
2. Способ по п.1, отличающийся тем, что в качестве растворителя используют кипящий ниже 100°С низкомолекулярный парафиновый углеводород или же смесь этих углеводородов.