Способ определения функциональной активности компонента c3 комплемента человека по классическому пути активации
Иллюстрации
Показать всеИзобретение относится к медицинской иммунологии, а именно к способам определения функциональной активности компонентов комплемента в сыворотке крови человека при диагностике ряда заболеваний и в биологических препаратах. Способ характеризуется тем, что сорбируют в лунках микропанели иммунохимически чистый иммуноглобулин G, затем в лунки микропанелей одновременно вносят анализируемую пробу, содержащую компонент С3 комплемента человека с неизвестной активностью, и раствор, содержащий сыворотку морской свинки, проводят инкубацию, после чего выливают содержимое лунок, а в лунки вносят конъюгат фермента с антителами против компонента С3 человека и субстрат этого фермента, расчет активности С3 проводят по количеству образовавшегося продукта ферментативной реакции. Преимущество изобретения заключается в том, что сокращается время определения, повышается чувствительность. 2 ил.
Реферат
Изобретение относится к медицинской иммунологии, а именно к способам определения функциональной активности компонентов комплемента в сыворотке крови человека при диагностике ряда заболеваний и в биологических препаратах.
Наиболее перспективным из современных методов определения белков сыворотки крови является метод иммуноферментного анализа благодаря своей чувствительности, избирательности и возможности автоматизации аналитического процесса. Кроме того, наиболее информативным является оценка функциональной активности этих белков, которая и характеризует развитие патологического процесса.
Что касается определения функциональной активности компонента С3 комплемента, то на сегодняшний день имеется иммуноферментный метод определения, описанный в патенте РФ №2195664 [1]. Согласно этому описанию способ осуществляется следующим образом: проводят сорбцию в лунках микропанели иммуноглобулина G, затем в лунки вносят сыворотку морской свинки и буферный раствор, содержащий ионы Са2+ и Ni2+, и проводят инкубацию для формирования на поверхности лунок стабильной С3-конвертазы классического пути комплемента, после чего, вылив содержимое, в лунки вносят растворы, в которых определяют активность компонента С3 и проводят инкубацию, во время которой происходит ковалентное связывание С3 с С3-конвертазой с превращением последней в С5-конвертазу. Количество ковалентно связавшегося в результате активации компонента С3 определяют по продукту ферментативной реакции с помощью антител к С3-фракции иммуноглобулинов G, ковалентно связанных с ферментом. Способ основан на способности функционально активного компонента С3 образовывать С5-конвертазу классического пути при взаимодействии с С3 конвертазой.
К недостаткам этого метода определения функциональной активности С3 можно отнести необходимость в ходе анализа предварительного создания на поверхности лунок микропанели сорбированной С3-конвертазы, что требует дополнительных затрат времени и средств. Кроме того, за время перехода к следующей стадии - активации С3 и сорбции последнего на С3-конвертазе, т.е. образования С5-конвертазы, происходит частичный естественный распад С3-конвертазы, что отражается на чувствительности метода определения.
Задачей заявленного изобретения является удешевление и упрощение способа, а также повышение его чувствительности.
Поставленная задача достигается путем разработки способа определения функциональной активности С3 компонента комплемента человека, который характеризуется тем, что сорбируют в лунках микропанели иммунохимически чистый иммуноглобулин G, затем в лунки микропанелей одновременно вносят анализируемую пробу, содержащую компонент С3 комплемента человека с неизвестной активностью, и раствор, содержащий сыворотку морской свинки, проводят инкубацию, после чего выливают содержимое лунок, а в лунки вносят конъюгат фермента с антителами против компонента С3 человека и субстрат этого фермента, расчет активности С3 проводят по количеству образовавшегося продукта ферментативной реакции.
Техническим результатом предложенного связывания С3 на С3-конвертазе одновременно с ее формированием является сокращение времени определения, повышение чувствительности и расширение диапазона активности определяемого компонента С3.
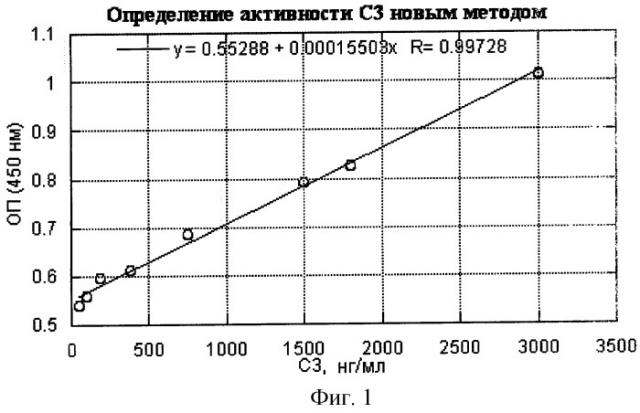
Пример 1. Определение активности С3 по классическому пути методом ИФА. Полистироловые планшеты сенсибилизировали иммунохимически чистым IgG3 в концентрациях белка 10-100 мкг/мл в 0.05 М натрий-карбонатном буфере, рН 9.5, внесением по 100 мкл раствора в каждую лунку плоскодонной полистироловой 96-луночной микропанели и инкубировали в течение 18 ч при 4°С. После трехкратной отмывки всех лунок планшета 4.55 мМ веронал-мединаловым буфером, рН 7.4, содержащим 0.15 М NaCl, 5 мМ MgCl2 и 1.5 мМ СаСl2, и последующего высушивания путем вытряхивания остатка жидкости во все лунки вертикального ряда планшета добавляли по 100 мкл того же буфера. В первую лунку ряда вносили 100 мкл стандартной сыворотки в предварительном разведении 1:100 в том же буфере, перемешивали и раститровывали на восемь лунок ряда, последовательно перенося и перемешивая по 100 мкл раствора из каждой предыдущей лунки в каждую последующую. В остальные 88 лунок планшета вносили по 100 мкл образцов сывороток в разведении 1:800 в том же буфере. Затем во все 96 лунок планшета вносили по 10 мкл комплемента морской свинки в рабочем разведении и с целью получения гомогенного раствора в каждой из лунок планшет встряхивали во время инкубации на электрокачалке. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки фосфатным буфером, рН 7.4, содержащим 0.15 М NaCl и 0,05% твин-20, и осушения планшета в каждую лунку вносили по 100 мкл конъюгата пероксидазы с антителами против С3 компонента человека в том же буфере в рабочем разведении. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки тем же буфером и осушения микропанели в каждую лунку вносят по 100 мкл раствора 3,3',5,5'-тетраметилбензидина (ТМБ) в субстратном буфере. После 30 мин инкубации в темноте реакцию останавливали внесением в каждую лунку 50 мкл 4% серной кислоты. Результаты реакции учитывали с помощью спектрофотометра с вертикальным лучом измерением светопоглощения при 450 нм. Функциональную активность препарата С3 рассчитывали по стандартной кривой. Результаты определения активности С3 приведены на фиг.1.
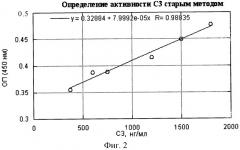
Пример 2. Определение активности С3 по классическому пути методом ИФА с добавлением солей никеля согласно прототипу. Растворяли иммунохимически чистый IgG3 в 0.05 М натрий-карбонатном буфере, рН 9.5, в концентрациях белка 10-100 мкг/мл и вносили по 100 мкл раствора в каждую лунку плоскодонного полистиролового 96-луночного планшета. Закрывали крышкой и оставляли на ночь при 4°С. Два раза отмывали планшет вероналовым буферным раствором, рН 7.4, содержащим 0.15 М NaCl, 0.15 мМ Са2+(VBS-Ca2+), по 150 мкл в каждую лунку, затем планшет осушали путем вытряхивания остатка жидкости. В лунки планшета ряда вносили 75 мкл VBS-Са2+, 15 мкл 0.1М нитрата никеля (II) и 10 мкл сыворотки морской свинки. После инкубации в термостате в течение 30 мин при 37°С, двукратной отмывки VBS, содержащим 5 мМ ЭДТА, (VBS-E) и осушения планшета, в лунки планшета каждого ряда вносили по 100 мкл раствора, содержащего С3 в растворе VBS-E, в виде прогрессивных двукратных разведений. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки фосфатным буфером, рН 7.4, содержащим 0,15 М NaCl и 0,05% твин-20, и осушения планшета в каждую лунку вносили по 100 мкл конъюгата пероксидазы с антителами против компонента СЗ человека в том же буфере в подобранном разведении. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки тем же буфером и осушения микропанели в каждую лунку вносят по 100 мкл раствора ТМБ в субстратном буфере. После 30 мин инкубации в темноте реакцию останавливали внесением в каждую лунку 50 мкл 4% серной кислоты. Результаты реакции учитывали с помощью спектрофотометра с вертикальным лучом измерением светопоглощения при 450 нм. Функциональную активность препарата С3 рассчитывали по стандартной кривой. Результаты определения активности С3 приведены на фиг.2.
Из приведенных на фигурах данных следует, что диапазон определяемых активностей С3 в предлагаемом методе вдвое больше, чем в прототипе, минимальная определяемая активность соответствует 50 нг/мл, но сравнению с 375 нг/мл в прототипе. Кроме того, исключается одна стадия инкубации в присутствии ионов никеля, занимающая 30 мин, и соответственно стадия отмывки планшета. Корреляция линейной калибровки в новом методе также несколько лучше. Таким образом, задача упрощения метода и повышение его чувствительности достигнута.
ЛИТЕРАТУРА
1. Козлов Л.В., Романов С.В., Баталов Т.Н., Лахтин В.М., Гузова В.А., Дьяков В.Л. Способ определения функциональной активности компонента С3 комплемента человека. Патент на изобретение РФ №2195664, 27.12.2002, Бюл. №36.
Способ определения функциональной активности компонента С3 комплемента человека по классическому пути активации, характеризующийся тем, что сорбируют в лунках микропанели иммунохимически чистый иммуноглобулин G, затем в лунки микропанелей одновременно вносят анализируемую пробу, содержащую компонент С3 комплемента человека с неизвестной активностью, и раствор, содержащий сыворотку морской свинки, проводят инкубацию, после чего выливают содержимое лунок, а в лунки вносят конъюгат фермента с антителами против компонента С3 человека и субстрат этого фермента, расчет активности С3 проводят по количеству образовавшегося продукта ферментативной реакции.