Способ исследования функционального состояния головного мозга, устройство для исследования функционального состояния головного мозга и способ измерения подэлектродного сопротивления
Иллюстрации
Показать всеИзобретения относятся к медицине и могут использоваться при контроле за состоянием больных. Способ исследования функционального состояния головного мозга: осуществляют многоканальную запись электроэнцефалограммы (ЭЭГ), электрокардиограммы (ЭКГ), проводят функциональную пробу и компьютерный анализ электрофизиологических сигналов, синхронно с многоканальной записью ЭЭГ и ЭКГ в реальном масштабе времени. Проводят регистрацию сверхмедленной активности мозга, запись реоэлектроэнцефалограммы (РЭГ) в бассейнах сонных и позвоночных артерий и фотоплетизмограммы (ФПГ) пальцев рук и/или ног и измерение подэлектродных сопротивлений электродов для снятия биоэлектрической активности головного мозга. При этом в едином покардиоцикловом временном масштабе осуществляют вычисление и визуализацию физиологических показателей биоэлектрической активности мозга - абсолютные и относительные значения мощности альфа-активности, патологической медленно-волновой активности в диапазоне дельта- и тета-волн, показатель динамики уровня метаболической активности головного мозга по уровню постоянного потенциала, частоту сердечных сокращений по ЭКГ, показатели пульсового кровенаполнения сосудов мозга по реографическим индексам РЭГ, показатель периферического сопротивления мозговых сосудов (ППСС), показатель тонуса периферических сосудов в виде амплитуды пульсации периферической ФПГ, показатель тонуса магистральных сосудов по времени распространения пульсовой волны от зубца Q сигнала ЭКГ до начала систолической волны периферической ФПГ, показатель тонуса посткапиллярно-венулярных сосудов по постоянной составляющей ФПГ, а оценку функционального состояния головного мозга производят по динамике изменений физиологических показателей до, во время и после проведения функциональной пробы. Устройство для исследования функционального состояния головного мозга содержит последовательно соединенные многоканальный аналого-цифровой преобразователь, микроЭВМ с гальванически развязанными портами ввода-вывода и ПЭВМ стандартной конфигурации, блок электродов для съема сигналов биоэлектрической активности головного мозга, подключенный к многоканальному усилителю сигналов биоэлектрической активности головного мозга, блок датчиков электрофизиологических сигналов, соединенный с усилителем электрофизиологических сигналов, блок токовых и потенциальных электродов для осуществления записи реосигналов, многоканальный усилитель реосигналов, генератор токовых реосигналов и синхронный детектор реосигналов, также устройство дополнительно содержит двухчастотный прецизионный генератор тока, задающий вход которого подключен к микроЭВМ, первая группа выходов соединена с рабочими электродами, а вторая - с референтными электродами блока электродов для съема сигналов биоэлектрической активности головного мозга, коммутатор отведений, первая группа входов которого соединена с потенциальными электродами блока токовых и потенциальных электродов для осуществления записи реосигналов, вторая группа входов - с выходами генератора токовых реосигналов. Первая группа выходов - с токовыми электродами блока токовых и потенциальных электродов для осуществления записи реосигналов, вторая группа выходов - с входами синхронного детектора реосигналов, демультиплексор, вход которого соединен с выходом синхронного детектора реосигналов, а выходы - с входами многоканального усилителя реосигналов. Выходы многоканального усилителя сигналов биоэлектрической активности головного мозга, многоканального усилителя реосигналов и усилителя электрофизиологических сигналов соединены с соответствующими входами многоканального аналого-цифрового преобразователя, выходы микроЭВМ соединены с входом управления коммутатора отведений, входом управления демультиплексора, входом управления многоканального аналого-цифрового преобразователя и входами синхронизации генератора токовых реосигналов и синхронного детектора реосигналов. Для измерения подэлектродного сопротивления на каждый рабочий электрод подают сигнал от узкополосного генератора тока с частотой f1, превышающей верхнюю частоту регистрируемых сигналов fверх, а на референтный электрод подают сигнал от узкополосного генератора тока с частотой f2≠f1>fверх, узкополосной фильтрацией выделяют и измеряют на выходе каждого усилителя напряжения с частотами f1 и f2 - Uf1 и uf2. При этом подэлектродное сопротивление каждого рабочего электрода определяют по формуле Zj=Ujf1: (Jf1×Kj), где Zj – подэлектродное сопротивление j-го электрода, Ujf1 - напряжение на выходе j-го усилителя с частотой f1, Jf1 - ток узкополосного генератора тока с частотой f1, Кj - коэффициент усиления j-го усилителя, а подэлектродное сопротивление референтного электрода определяют по формуле ZA=ujf2: (Jf2×Kj), где zA - подэлектродное сопротивление референтного электрода А, сопричастного j-му усилителю, Ujf2 - напряжение на выходе j-го усилителя с частотой f2, Jf2 - ток узкополосного генератора тока с частотой f2. Изобретение позволяет расширить арсенал диагностических средств. 10 ил. 3 н. и 12 з.п. ф-лы.
Реферат
Изобретения относятся к медицине и могут использоваться при контроле за состоянием больных с нарушением мозгового кровообращения и для дифференциальной диагностики эпилепсии и эпилептиформных проявлений.
Пароксизмальные состояния нервной системы относятся к нервньм заболеваниям, которые широко распространены, особенно в развитых странах, и имеют тенденцию к увеличению. Диагностика этих заболеваний производится, как правило, по данным тщательного клинического обследования пациентов, включающего применение электрофизиологических методов, ангиографии, рентгеноскопии, метода ядерного магнитного резонанса, позитронно-эмиссионной томографии и других инструментальных подходов. Для уточнения диагноза нередко используют клинико-биохимический анализ крови и других биологических жидкостей на содержание возбуждающих и тормозных нейромедиаторов и нейропептидов или продуктов их метаболизма: глютамата, ГАМК, серотонина, дофамина, моноаминооксидазы, эндорфина и др. (см., например, патент Российской Федерации №2112243, МПК7 G 01 N 33/53, C 12 Q 1/04, А 61 К 39/00) Однако использование всех этих методов для оценки функционального состояния мозга и организма не позволяет однозначно определить степень вовлеченности определенных обменных и регуляторных систем в патогенез заболевания, что очень важно для определения тактики лечения, требует больших временных и экономических затрат на выполнение исследований, не обладает достаточным уровнем специфичности для каждой нозологической формы, практически не дает возможности выявлять предрасположенность (группу риска), проводить диагностику заболеваний на ранних стадиях.
Известен способ определения биоэлектрической активности мозга, включающий наложение на голову пациента измерительных электродов над мозгом и нулевого электрода на определенном расстоянии от мозга, усиление сигналов с измерительных электродов в два этапа: на первом этапе биопотенциал с каждого измерительного электрода поступает на один вход соответствующего дифференциального усилителя, на второй вход которого подается биопотенциал с нулевого электрода, на втором этапе выходной сигнал каждого дифференциального усилителя сравнивается с усредненным выходным сигналом дифференциальных усилителей соседних измерительных электродов (см. заявку Великобритании № 1501803, МПК3 А61В 5/04, НКИ G1N, A3R, публ. 1979 г.). Этот способ из-за отсутствия возможности измерения подэлектродных сопротивлений не обладает достаточной точностью регистрации сверхмедленной (менее 1 Гц) биоэлектрической активности мозга, по которой оценивается величина церебральных энергозатрат. Поэтому такое исследование функционального состояния мозга мало информативно для дифференциальной диагностики эпилепсии и эпилептиформных проявлений.
В патенте Российской Федерации № 2007116, МПК5 А 61 В 5/04, публ. 1994 г., описан способ регистрации сдвига уровня постоянного электрического потенциала головного мозга, используемый при оценке стабильности функционального состояния, при диагностике неврозов и психических заболеваний. Способ осуществляется следующим образом. На голове испытуемого устанавливают пару регистрирующих электродов над заданным участком мозга. Электроды подсоединяют к усилителю электрических напряжений, с выхода которого считывают в начале и конце сдвига, вызванного внешним воздействием, значения постоянного электрического потенциала и сравнивают их между собой. Для исключения влияния нестабильности межэлектродного кожного потенциала вход усилителя кратковременно шунтируют эталонным сопротивлением и осуществляют сравнение между снижением сопротивления, возникающего при кратковременном шунтировании входа усилителя в начале и конце сдвига. Если снижение усиления одинаково, то полагают, что влияние кожного потенциала не сказывается, и результат регистрируется. Если же снижение усиления в начале и конце сдвига разное, то считается, что результаты искажены нестабильностью кожного потенциала, и регистрация не осуществляется. Недостаток такого способа оценки функционального состояния мозга - ограниченная применимость, отсутствие возможности дифференциальной диагностики мозгового кровообращения, малая информативность и низкая точность из-за нестабильности и различия подэлектродного сопротивления.
Патентом Российской Федерации № 2187958, МПК7 А 61 В 5/04, публ. 2002 г., защищен способ исследования состояния сосудов головного мозга, включающий локальное холодовое воздействие и реоэнцефалографию, отличающийся тем, что локальное холодовое воздействие осуществляют в проекции бассейна сосудов внутренней сонной артерии теплообменником с температурой t° =10±2° С в течение 10 мин, причем реоэнцефалография проводится до, сразу и через 10 и 20 мин после холодового воздействия. Этот способ имеет ограниченное применение и непригоден для дифференциальной диагностики эпилепсии и эпилепиформных проявлений.
Из описания к патенту Российской Федерации № 2189776, МПК7 А 61 В 5/0476, публ. 2002 г., известен способ диагностики и прогнозирования развития эпилепсии у пациентов с доклинической стадией болезни. Регистрируют электроэнцефалограмму в состоянии пациента пассивного бодрствования. Методом кросскорреляционного анализа обрабатывают фрагменты ЭЭГ длительностью не более одной минуты, которые не содержат пароксизмальной активности. Получают коэффициенты кросскорреляций (ККр) альфа-активности между отведениями левой лобной и левой затылочной областей. Полученные значения ККр в пределах от –1,00 до -0,35 свидетельствуют о здоровье пациента, при значениях ККр от -0,34 до 0,00 диагностируют доклиническую стадию эпилепсии, а при значениях ККр от 0,01 до 1,00 - клиническую стадию эпилепсии. Способ позволяет повысить точность диагностики развития эпилепсии. Недостаток - способ имеет ограниченное применение и не позволяет из-за малой информативности осуществлять дифференциальную диагностику нарушений мозгового кровообращения.
Известен способ определения нарушения кровоснабжения головы (см. патент Российской Федерации № 2159075, МПК7 А 61 В 5/05, публ. 2000 г.), в соответствии с которым регистрируют дифференциальные реограммы с области шеи, груди, рук. Измеряют их амплитудно-временные характеристики. Рассчитывают объем притока крови к голове как разность объемов кровотока на участках грудь - шея и грудь - руки. Регистрируют огибающую реограмму на участке грудь - шея и измеряют амплитуды ее венозной систолической и основной волн. Рассчитывают их соотношение. Регистрируют ультразвуковую доплерограмму потока крови через правое атриовентрикулярное отверстие сердца. Измеряют по ней средние скорости потока крови во время раннего наполнения правого желудочка сердца и систолы правого предсердия. Рассчитывают их соотношение. Нарушение кровоснабжения головы определяют по рассчитанным величинам. Недостаток этого способа - он позволяет выявить патологические нарушения только при их клинической выраженности и мало эффективен в донозологической диагностике.
Из описания к патенту Российской Федерации № 2188575, МПК7 А 61 В 5/0476, G 01 N 33/53, публ. 2002 г., известен способ диагностики и прогнозирования развития эпилепсии у пациентов с доклинической стадией болезни, включающий ЭЭГ-мониторинг, обработку полученной ЭЭГ методом фрактального анализа и получение значений фрактальной размерности (ФР), расчет значений теста параксимальной активности (ПАТ) по содержанию в крови пациента аутоантител к квисквалатсвязывающему мембранному белку, расчет индекса эпилепсии (ИЭ) по формуле ИЭ=ПАТ × ФР и диагностирование клинической стадии эпилепсии при значениях ИЭ=132,5±5,32, отсутствие признаков эпилепсии при значениях ИЭ=45,05±3,31 и доклинической стадии эпилепсии при промежуточных значениях ИЭ. Этот способ позволяет выявить доклиническую стадию эпилепсии, но мало информативен для дифференциальной диагностики эпилепсии и эпилептиформных проявлений.
Из патента Российской Федерации № 2103912, МПК6 А 61 В 5/0476, публ. 1998 г., известен способ исследования мозга, согласно которому снимают электроэнцефалограмму до и после предъявления стимула, вычисляют спектр мощности ЭЭГ или коэффициент синхронности электрических процессов в каждой точке расположения электрода по отношению к соседним. Определяют изменение величины полученных значений после стимула и представляют результаты вычислений в виде топографической карты. Дополнительно в точках расположения электродов измеряют температуру, рассчитывают ее разность и вносят в карту. Этот способ позволяет одновременно с измерением и исследованием электрических процессов, измерять и исследовать тепловое поле головы. Недостаток этого способа - отсутствие возможности дифференциальной диагностики нарушений мозгового кровообращения, отсутствие возможности различения эпилепсии и эпилептиформных проявлений.
Известен способ диагностики степени психофизиологической дезадаптации у больных с начальными формами хронической цереброваскулярной патологии (см. патент Российской Федерации № 2154979, МПК7 А 61 В 5/04, 5/0476, публ. 2000 г.). Этот способ осуществляется следующим образом. Больному, находящемуся в состоянии расслабленного бодрствования с закрытыми глазами, производят многоканальную запись ЭЭГ по стандартной методике, располагая 19 или более электродов для отслеживания артефактов. Одновременно осуществляют компьютерный спектральный анализ лишенных артефактов фрагментов ЭЭГ с оценкой мощности спектрограммы в полосах частот альфа-(8... 12 Гц), бета-(12 Гц и выше), тета-(4... 8 Гц) и дельта-(0...4 Гц) активности. При значении абсолютной мощности альфа-активности более 10 мкВ2, или более 80 мкВ2, и/или при значениях мощности альфа-активности более 50% диагностируют значительную степень психофизиологической дезадаптации. Описанный способ позволяет объектизировать у больных с начальными формами сосудистых заболеваний головного мозга значительную психофизиологическую дезадаптацию, являющуюся важным патогенетическим фактором развития патологии. Недостаток такого способа - низкая эффективность при установлении причин нарушения мозгового кровообращения и при дифференциальной диагностике эпилепсии и эпилептиформных проявлений.
Наиболее близким к заявляемому способу исследования функционального состояния головного мозга по большинству совпадающих признаков является способ исследования индивидуальных особенностей регуляции физиологических функций организма человека, защищенный патентом Российской Федерации № 2185088, МПК7 А 61 В 5/00, 5/04, публ. 2002 г. Способ исследования индивидуальных особенностей регуляции физиологических функций включает запись электроэнцефалограммы (ЭЭГ), электрокардиограммы (ЭКГ) пневмограммы, измерение артериального давления (АД) и проведение семи функциональных дыхательных проб. Особенности регуляции физиологических функций определяют по показателям внешнего дыхания и газообмена, РАСО2, РАО2, пневмограммы, характеру и скорости появления изменений ЭКГ, АД, ЭЭГ, латентного периода двигательной реакции, скорости выработки не дыхательных условных рефлексов. Первую пробу, 1-2-минутную не дозированную по интенсивности гипервентиляцию, проводят с учетом ощущений, обусловленных изменениями мозгового кровообращения, головокружения, легкой головной боли, пелены перед глазами, изменениями в деятельности ЦНС, проявляющимися в форме сенсорных или двигательных расстройств, в виде парестезии, онемения, скованности, напряженности, дрожи, а также вегетативными сдвигами в виде ощущения тепла, учащения сердцебиений, потливости, сухости во рту, позволяющими выявить физиологические функции: сердечно-сосудистые, дыхательные, нервной системы, участвующие в развитии гипервентиляционного синдрома. Вторую пробу - жесткую гипервентиляцию осуществляют на протяжении 2,5-3,5 минут, во время которой испытуемому дают команды для поддержания уровня вентиляции, проводят с целью выявления людей, чувствительных к гипервентиляции, регистрируя скорость появления ощущений и их характер. Третью пробу - изокапническую гипервентиляцию, обеспечивающую поддержание у обследуемых стабильного уровня РСО2, проводят для выявления испытуемых с преобладанием нейрогенного фактора в регуляции функций. Четвертая проба - задержка дыхания на уровне спокойного вдоха. Пятая проба - задержка дыхания на уровне обычного выдоха. Шестая проба - задержка дыхания на вдохе после произвольной гипервентиляции. Во всех трех пробах с задержкой дыхания определяют время от начала задержки дыхания до первого побуждения к дыханию (1-я фаза) и до возобновления дыхания (2-я фаза), а также общее время задержки дыхания. По первой фазе оценивают индивидуальную чувствительность испытуемых к совокупности гуморальных СО2 и O2 и нейрогенных факторов, по второй фазе оценивают способность к волевым усилиям. Седьмая проба - гиповентиляция - режим дыхания, при котором обследуемый дышит не менее 10 минут в ритме два дыхания в минуту без ограничения глубины, после предварительной дыхательной тренировки, срок которой индивидуально обусловлен. Перечисленные семь проб позволяют выявить индивидуальную чувствительность обследуемых к гуморальным и нейрогенным факторам, причем первая и вторая пробы с гипервентиляцией - к степени падения РАСО2 и выраженным в разной степени нейрогенным сдвигам, третья проба с гипервентиляцией - только к нейрогенным факторам, четвертая и пятая пробы с задержкой дыхания - к накоплению СO2, снижению РАО2 и нейрогенньм факторам, шестая проба с задержкой дыхания - к снижению РАО2, седьмая - к снижению РАО2, накоплению РАСО2, нейрогенньм факторам, тренируемости дыхания и способности к установлению нового, более эффективного стереотипа дыхания. Достигаемый результат заключается в возможности получения наиболее полной информации о формировании физиологических реакций организма на произвольное управление дыханием и его адаптивных возможностях, целенаправленного влияния на функциональное состояние организма, повышении умственной и физической работоспособности здоровых людей, увеличении эффективности адаптации к изменяемым условиям окружающей среды, тренировки и установления нового эффективного стереотипа дыхания. Недостаток способа прототипа - он применим для исследования индивидуальных особенностей здоровых людей и неэффективен при установлении причин нарушения мозгового кровообращения, при дифференциальной диагностике эпилепсии и эпилептиформных проявлений, при выявлении начальных проявлений цереброваскулярных нарушений и прогнозе их развития.
Задача, решаемая изобретением, - повышение эффективности при установлении причин нарушения мозгового кровообращения и при дифференциальной диагностике эпилепсии и эпилептиформных проявлений, выявлении начальных проявлений цереброваскулярных нарушений и прогнозе их развития.
Решение указанной задачи достигается тем, что в способе исследования функционального состояния головного мозга, включающем многоканальную запись электроэнцефалограммы (ЭЭГ), электрокардиограммы (ЭКГ), проведение функциональной пробы и компьютерный анализ электрофизиологических сигналов, дополнительно, синхронно с многоканальной записью ЭЭГ и ЭКГ в реальном масштабе времени, осуществляют регистрацию сверхмедленной активности мозга, запись реоэлектроэнцефалограммы (РЭГ) в бассейнах сонных и позвоночных артерий и фотоплетизмограммы (ФПГ) пальцев рук и/или ног и измерение подэлектродных сопротивлений электродов для снятия биоэлектрической активности головного мозга, при этом в едином покардиоцикловом временном масштабе, т.е. в привязке к каждому из автоматически распознаваемых кардиоциклов, осуществляют вычисление и визуализацию физиологических показателей биоэлектрической активности мозга - абсолютные и относительные значения мощности альфа-активности, патологической медленно-волновой активности в диапазоне дельта- и тета-волн, показатель динамики уровня метаболической активности головного мозга по постоянной составляющей ЭЭГ, частоту сердечных сокращений по ЭКГ, показатели пульсового кровенаполнения сосудов мозга по реографическим индексам РЭГ, показатель периферического сопротивления мозговых сосудов (ППСС), показатель тонуса периферических сосудов в виде амплитуды пульсации периферической ФПГ, показатель тонуса магистральных сосудов по времени распространения пульсовой волны от зубца Q сигнала ЭКГ до начала систолической волны периферической ФПГ, показатель тонуса посткапиллярно-венулярных сосудов по постоянной составляющей ФПГ, а дифференциальную диагностику эпилепсии и эпилептиформных проявлений производят по динамике изменений физиологических показателей до, во время и после проведения функциональной пробы. Для определения функционального состояния мозга проводят функциональную пробу на гипервентиляцию и, если после начала проведения пробы наблюдается снижение реографического индекса РЭГ более чем на 20%, а затем наблюдаются пароксизмальные проявления на ЭЭГ в виде резкого повышения отношения патологических медленно-волновых волн в дельта- и тета-диапазонах к альфа-активности, то потенциально возможной причиной пароксимальных проявлений на ЭЭГ формулируют сосудистые нарушения головного мозга. Если снижение реографического индекса РЭГ и появление пароксимальных проявлений на ЭЭГ сопровождается смещением уровня постоянного потенциала сверхмедленной активности мозга, то делается вывод о наличии влияния сосудистого фактора на пароксимальные проявления, сопровождающегося метаболическими изменениями. Если снижение реографического индекса РЭГ и появление пароксимальных проявлений на ЭЭГ не сопровождается значимым снижением периферического кровотока по ФПГ, то потенциально возможной причиной сосудистых нарушений головного мозга формулируют недостаточность регуляторных процессов по компенсаторному снижению периферического кровотока и перераспределению общего кровотока в жизненно важные органы. Если снижение реографического индекса РЭГ и появления пароксимальных проявлений на ЭЭГ совпадают, то дополнительно делается вывод о наличии фокуса патологической активноста, определяющего неадекватность регионарного мозгового кровотока. Если до проведения функциональной пробы на гипервентиляцию наблюдались дезорганизация ЭЭГ, снижение пульсового кровенаполнения и повышение тонуса по РЭГ, а в процессе проведения пробы наблюдалась нормализация показателей мозгового кровотока, выражающаяся в повышении пульсового кровенаполнения, снижении показателя периферического сопротивления мозговых сосудов, и нормализация ЭЭГ, выражающаяся в повышении уровня альфа-активнсти с сохранением зональных различий по лобно-затылочным областям, снижении отношения патологических медленно-волновых волн в дельта- и тета-диапазонах к альфа-активности, то формулируют предположение о наличии цереброваскулярных нарушений, связанных с нарушением газового состава крови в исходном фоновом состоянии. Если проводят функциональную пробу на гипервентиляцию и в процессе проведения пробы на сигнале ЭКГ наблюдаются экстрасистолы и им предшествуют пароксизмы на синхронно регистрируемых сигналах ЭЭГ, то делают вывод о цереброгенном характере нарушений сердечного ритма, если отсутствует причинно-временная связь между пароксизмами на ЭЭГ и экстрасистолами на ЭКГ, то делается вывод о кардиогенном характере нарушений сердечного ритма. Проводят длительную пассивную ортостатическую пробу и, если в процессе проведения пробы у пациента фиксируется синокопальное состояние, то при резко выраженной брадикардии или асистолии по ЭКГ до наступления синокопального состояния и снижении показателей мозгового кровотока по РЭГ диагностируют кардиоингибиторную причину синкопального состояния, при предшествующих синокопальному состоянию выраженных признаках депонирования крови в конечностях по ФПГ и снижении показателей мозгового кровотока по РЭГ и отсутствии значимого уменьшения частоты сердечных сокращений по ЭКГ диагностируют вазодепресивную причину синкопального состояния, а при предшествующих синкопальному состоянию пароксизмах на ЭЭГ и отсутствии значимого уменьшения частоты сердечных сокращений по ЭКГ и выраженных признаков депонирования крови в конечностях по ФПГ диагностируют судорожный тип обморока.
Устройство для исследования функционального состояния головного мозга является самостоятельньм объектом изобретения.
Известен электроэнцефалограф, защищенный патентом СССР N 880241, МПК3. А61В 5/04 (заявка ФРГ N 2727583 от 20.06.77 г.), содержащий измерительные электроды, накладываемые на голову пациента, селектор отведений, выполненный в виде изображения головы с размещенными на нем переключателями с индикаторньми лампочками, и сигнальные усилители, входы которых через селектор отведений подключается к измерительным электродам, а выходные сигналы управляют самописцами. В этом электроэнцефалографе обеспечивается наглядность подключения измерительных электродов ко входам усилителей, чем снижается вероятность их ошибочного подсоединения. К недостаткам такого электроэнцефалографа следует отнести отсутствие возможности оперативного анализа электроэнцефалограмм, невозможность выявления нарушений мозгового кровотока.
Известно устройство для оценки патологических изменений в системной деятельности мозга человека, включающее набор датчиков, налагаемых на голову человека и/или подключаемых к глубинным электродам, многоканальный усилитель сигналов датчиков с числом каналов, соответствующим числу датчиков, блок одновременного преобразования сигналов из непрерывной формы в дискретную, блок статистической обработки полученных данных и блок объемного воспроизведения (см. патент США № 4736751, МПК5 А 61 В 5/04, публ. 1988 г.). Такое устройство не обеспечивает выявление причин нарушения мозгового кровообращения и недостаточно эффективно при дифференциальной диагностике эпилепсии и элептиформных проявлений.
Из патента Российской Федерации № 2177716, МПК7 А 61 В 5/0476, публ. 2002 г., известно устройство для оценки патологических изменений в системной деятельности мозга, которое включает набор датчиков, налагаемых на голову человека, и/или подключаемых к глубинным электродам, и/или располагаемых на некотором расстоянии от головы, многоканальный усилитель сигналов датчиков, например электроэнцефалограф, с числом каналов, соответствующим числу датчиков, блок преобразования сигналов, например преобразования из непрерывной формы в дискретную, блок измерения статистической взаимосвязи между процессами, блок измерения размерности пространства отображаемых процессов, соответствующей совокупным статистическим свойствам взаимосвязей между измеряемыми процессами, блок вычисления координат и/или величин радиус-векторов отображаемых процессов, блок визуализации пространственного распределения радиус-векторов отображаемых процессов, например графопостроитель или графический дисплей, запоминающее устройство, блок измерения отличий параметров пространственных распределений радиус-векторов отображаемых процессов, блок визуализации отличий в интегративной деятельности мозга пациента, блок предъявления тестов и блок синхронизации. Устройство позволяет достоверно выявить степень и характер устойчивых патологических отклонений в системной деятельности мозга человека, определять их локализацию и характер нарушений, количественно оценивать степень патологических отклонений, связанных с выполнением тестов или с любыми переменами функционального состояния мозга. Недостаток этого устройства для оценки патологических изменений в системной деятельности мозга - сравнительно низкая эффективность при дифференциальной диагностике эпилепсии и элептиформных проявлений, отсутствие возможности диагностировать причину нарушения мозгового кровообращения.
Устройство для съема, регистрации и анализа электрофизиологических сигналов, защищенное патентом Российской Федерации № 2102004, МПК6 А 61 В 5/04, публ. 1998 г., содержит последовательно соединенные блок электродов, селективный многоканальный усилитель, мультиплексор, аналого-цифровой преобразователь, устройство управления и первичной обработки, блок гальванического разделения, интерфейсный блок и персональную ЭВМ. Цепи питания многоканального усилителя соединены с выходными шинами блока защиты от аварийных токов, первая группа входов которого подключена к электродам, а вторая к выходным шинам источника питания. Это устройство не эффективно при дифференциальной диагностике эпилепсии и элептиформных проявлений из-за отсутствия возможности измерения импеданса головного мозга синхронно со съемом сигналов биоэлектрической активности мозга и контроля подэлектродных сопротивлений.
Наиболее близким к заявляемому устройству для исследования функционального состояния головного мозга является устройство для исследования биологической активности мозга, содержащее блок отводящих электродов, датчик электрокардиосигнала, коммутационную панель, выполненную в виде изображения головы с гнездами для подключения отводящих электродов, многоканальный предварительный усилитель, входы которого соединены с соответствующими гнездами подключения коммутационной панели, а выходы с соответствующими информационными выходами селектора отведений, усилитель электрокардиосигнала, выходы которого соединены с соответствующими гнездами подключения коммутационной панели, блок контроля импеданса электродов, многоканальный селективный усилитель, аналого-цифровой преобразователь, генератор звуковых стимулов, генератор зрительных стимулов и ЭВМ с подключенными к ней накопителем на магнитных дисках, дисплеем и печатающим устройством, дополнительно включены блок измерительных электродов, блок измерения внутричерепного импеданса, блок контроля работоспособности с соединительной колодкой, четырехканальный дифференциальный усилитель, многоканальный аналоговый коммутатор, усилитель с регулируемыми напряжением смещения и коэффициентом усиления, блок памяти, микропроцессор, блоки обмена информацией и сопряжения и четырехканальный аналоговый переключатель (см. патент Российской Федерации № 2076625, МПК6 А 61 В 5/04, публ. 1997 г). Это устройство позволяет в течение одного сеанса обследования снимать и анализировать сигналы электроэнцефалографии, электрографии и реоэлектроэнцефалографии, контролировать параметры усилителей и импеданс электродов, что особенно важно при исследованиях с проведением функциональных проб.
Устройство для исследования биологической активности мозга по патенту Российской Федерации № 2076625 принято в качестве прототипа. Общими признаками заявляемого устройства с прототипом являются следующие:
- назначение - оба устройства предназначены для исследования функционального состояния головного мозга;
- оба устройства включают аналогичные по назначению функциональные узлы - блок электродов для съема сигналов биоэлектрической активности головного мозга (в прототипе это блок отводящих электродов), блок датчиков электрофизиологических сигналов (в прототипе - датчик электрокардиосигналов), блок токовых и потенциальных электродов для осуществления записи реосигналов (в прототипе - блок измерительных электродов), многоканальный усилитель сигналов биоэлектрической активности головного мозга (в прототипе - многоканальный предварительный усилитель), многоканальный усилитель реосигналов (в прототипе - многоканальный селективный усилитель), многоканальный аналого-цифровой преобразователь (в прототипе - многоканальный аналоговый переключатель и аналого-цифровой преобразователь), усилитель электрофизиологических сигналов (в прототипе - усилитель электрокардиосигнала), микроЭВМ (в прототипе - микропроцессор), ПЭВМ стандартной конфигурации (в прототипе - ЭВМ с дисплеем и печатающим устройством), генератор токовых реосигналов и синхронный детектор реосигналов (в прототипе - блок измерения внутричерепного импеданса);
- соединения блоков и узлов - блок электродов для съема сигналов биоэлектрической активности головного мозга и блок датчиков электрофизиологических сигналов соединены соответственно с многоканальным усилителем сигналов биоэлектрической активности головного мозга и усилителем электрофизиологических сигналов (в прототипе они соединены через коммутационную панель), многоканальный аналого-цифровой преобразователь, микроЭВМ и ПЭВМ стандартной конфигурации соединены последовательно (в прототипе через шину данных и устройство сопряжения соответственно).
Недостатки прототипа - отсутствие возможности синхронного съема сигналов электроэнцефалографии и реоэлектроэнцефалографии, что снижает возможность их взаимной корреляции, низкая точность измерения подэлектродного сопротивления, что снижает точность регистрации сверхмедленной биоэлектрической активности головного мозга. Эти недостатки существенно затрудняют дифференциальную диагностику эпилепсии и эпилептиформных проявлений и выявление начальных проявлений нарушений регуляторного характера.
Задача, решаемая изобретением, - повышение эффективности дифференциальной диагностики эпилепсии и эпилептиформных проявлений, выявление начальных проявлений нарушений регуляторного характера.
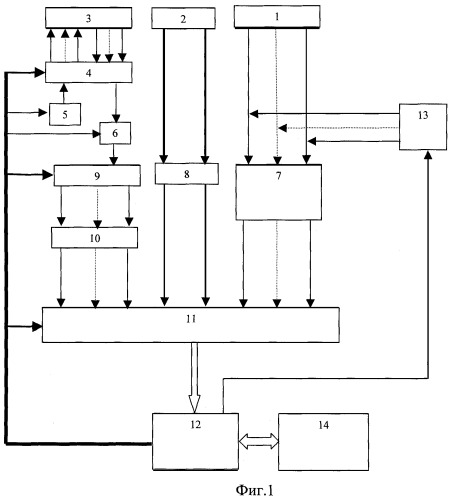
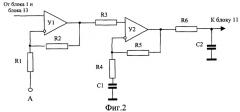
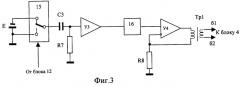
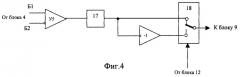
Решение указанной задачи достигается тем, что устройство для исследования функционального состояния головного мозга, содержащее последовательно соединенные многоканальный аналого-цифровой преобразователь, микроЭВМ с гальванически развязанными портами ввода-вывода и ПЭВМ стандартной конфигурации, блок электродов для съема сигналов биоэлектрической активности головного мозга, подключенный к многоканальному усилителю сигналов биоэлектрической активности головного мозга, блок датчиков электрофизиологических сигналов, соединенный с усилителем электрофизиологических сигналов, блок токовых и потенциальных электродов для осуществления записи реосигналов, многоканальный усилитель реосигналов, генератор токовых реосигналов и синхронный детектор реосигналов, дополнительно содержит двухчастотный прецизионный генератор тока, задающий вход которого подключен к микроЭВМ, первая группа выходов соединена с рабочими электродами, а вторая - с референтньми электродами блока электродов для съема сигналов биоэлектрической активности головного мозга, коммутатор отведений, первая группа входов которого соединена с потенциальными электродами блока токовых и потенциальных электродов для осуществления записи реосигналов, вторая группа входов - с выходами генератора токовых реосигналов, первая группа выходов - с токовыми электродами блока токовых и потенциальных электродов для осуществления записи реосигналов, вторая группа выходов - с входами синхронного детектора реосигналов, демультиплексор, вход которого соединен с выходом синхронного детектора реосигналов, а выходы с входами многоканального усилителя реосигналов, выходы многоканального усилителя сигналов биоэлектрической активности головного мозга, многоканального усилителя реосигналов и усилителя электрофизиологических сигналов соединены с соответствующими входами многоканального аналого-цифрового преобразователя, выходы микроЭВМ соединены с входом управления коммутатора отведений, входом управления демультиплексора, входом управления многоканального аналого-цифрового преобразователя и входами синхронизации генератора токовых реосигналов и синхронного детектора реосигналов. Блок датчиков электрофизиологических сигналов содержит электроды для съема электрической активности сердца, электрических сигналов двигательной активности мышц, фотодатчик пульсовой волны и датчик дыхательной волны. Генератор токовых реосигналов содержит источник постоянного напряжения, полюсы которого через управляемый переключатель и узкополосный усилитель напряжения соединен с входом линейного преобразователя напряжение - ток, выход которого является выходом генератора. Синхронный детектор реосигналов содержит последовательно соединенные дифференциальный усилитель, полосовой фильтр и инвертор, а также управляемый переключатель, переключаемые входы соединены с входом и выходом инвертора, входами синхронного детектора являются входы дифференциального усилителя и управляющий вход управляемого переключателя, выходом - выход управляемого переключателя. Двухчастотный прецизионный генератор тока содержит два частотных делителя, входы которых объединены и являются задающим входом генератора, а выходы через конденсаторы емкостью 10... 20 pF соединены: первого с выходами для подключения рабочих электродов, второго - для подключения референтных электродов. Усилительный канал многоканального усилителя сигналов биоэлектрической активности головного мозга содержит последовательно соединенные дифференциальный усилитель, неинвертирующий вход которого соединен с входом для подключения соответствующего рабочего электрода, а инвертирующий - через согласующий каскад с входом для подключения референтного электрода, усилитель с коэффициентом усиления по постоянному току, равном единице, и усилением в рабочей полосе частот, равном номинальному, и фильтр нижних частот.
Способ измерения подэлектродных сопротивлений является самостоятельньм объектом изобретения.
Известен способ измерения электрокожного сопротивления, защищенный авторским свидетельством СССР № 1821195, МПК5 А 61 Н 39/00, А 61 В 5/05, публ. 1993 г., по которому на кожу накладывают измерительные электроды, пропускают между ними знакопостоянные стабилизированные импульсы электрического тока длительностью 200... 380 мксек при плотности тока 7,1... 36,2 мкА, многократно измеряют сопротивление в конце каждого импульса, вычисляют значение поправки к измеряемому сопротивлению как разность между значением сопротивления при первом измерении и значением сопротивления при втором через 42 сек после первого измерения, а значение сопротивления при каждом последующем измерении определяют с учетом этой поправки. Этот способ неприменим для синхронного измерения подэлектродного сопротивления при регистрации биопотенциалов головного мозга и/или электрических сигналов, генерируемых сердцем и/или электрических сигналов мышечных движений.
По способу двухэлектродного измерения электрического сопротивления биообъектов, защищенному авторским свидетельством СССР №1204182, МПК4 А 61 В 5/05, G 01 R 27/02, публ. 1986 г., на исследуемом объекте размещают электроды, через которые пропускают измерительный ток и измеряют межэлектродное сопротивление R1, затем изменяют величину измерительного тока и площадь электродов в k раз при условии неизменности внешних габаритов электродов и измеряют новое значение межэлектродного сопротивления R2, а величину сопротивления ткани биообъекта и подэлектродного сопротивления R3 вычисляют по формулам. Этот способ также неприемлем для синхронного измерения подэлектродных сопротивлений при регистрации биопотенциалов головного мозга и/или электрических сигналов, генерируемых сердцем и/или электрических сигналов мышечных движений.
Технический результат от использования изобретения - обеспечение возможности синхронного измерения подэлектродных сопротивлений при регистрации биопотенциалов головного мозга и/или электрических сигналов, генерируемых сердцем и/или электрических сигналов мышечных движений.
Указанный результат достигается тем, что в способе измерения подэлектродного сопротивления при регистрации биопотенциалов головного мозга и/или электрических сигналов, генерируемых сердцем, и/или электрических сигналов мышечных движений с использованием дифференциальных усилителей этих сигналов, на каждый рабочий электрод подают сигнал от узкополосного генератора тока с частотой f1, превышающей верхнюю частоту регистрируемых сигналов fвepx, а на референтный электрод подают сигнал от узкополосного генератора тока с частотой f