Пептидное соединение, восстанавливающее функцию миокарда
Иллюстрации
Показать всеИзобретение относится к лекарственным средствам для лечения заболеваний сердечно-сосудистой системы и может быть использовано как средство, восстанавливающее функцию миокарда, при лечении различных форм данной патологии. Предлагается новый тетрапептид аланил-глутамил-аспартил-аргинин общей формулы Ala-Glu-Asp-Arg последовательности 1 [SEQ ID NO:1], обладающий биологической активностью, проявляющейся в восстановлении функции миокарда. Предлагается фармакологическое средство, содержащее в качестве активного пептидного агента эффективное количество тетрапептида аланил-глутамил-аспартил-аргинин общей формулы Ala-Glu-Asp-Arg последовательности 1 [SEQ ID NO:1], обладающий биологической активностью, проявляющейся в восстановлении функции миокарда. Использование нового тетрапептида Ala-Glu-Asp-Arg в медикаменте способствует восстановлению функции миокарда. 3 н. и 1 з.п. ф-лы, 9 табл., 1 ил.
Реферат
Изобретение относится к лекарственным средствам для лечения заболеваний сердечно-сосудистой системы и может быть использовано как средство, восстанавливающее функцию миокарда, при лечении различных форм данной патологии.
В настоящее время не теряет актуальности проблема профилактики и лечения сердечно-сосудистых заболеваний в связи с их серьезностью и распространенностью. Отмечена тенденция к увеличению развития патологии сердечно-сосудистой системы, что является причиной нетрудоспособности и смертности во все более раннем возрасте. В связи с этим возрастающую социальную значимость приобретает разработка новых лекарственных средств, применяемых для лечения заболеваний сердечно-сосудистой системы.
Наиболее распространенные формы сердечной патологии связаны с ишемией сердца, возникающей в результате нарушений в сосудистой системе, в тяжелых случаях приводящей к инфаркту миокарда - лидирующей причине смерти в современном обществе. Ишемическая болезнь сердца часто приводит к таким осложнениям как нарушения сократимости, возбудимости, проводимости миокарда. Помимо этого следует выделить отдельную группу заболеваний сердечной мышцы, лечение которых сводится, в основном, к общеукрепляющей терапии и отчасти является симптоматическим. Это миокардиодистрофии, миопатии, кардиомиопатии.
Среди средств, используемых для профилактики ишемии миокарда, используют фармакологические препараты различных групп, в том числе антагонисты кальция: амлодипин, верапамил, фелодипин (Регистр лекарственных средств России. Энциклопедия лекарственных средств. - Москва, 2003. - С.90, С.180, С.865) и бета-адреноблокаторы, такие как пропанолол, пиндолол (Регистр лекарственных средств России. Энциклопедия лекарственных средств. - Москва, 2003. - С.700, С.659). Особенностью действия этих веществ является снижение потребности миокарда в кислороде и отрицательный инотропный эффект. Другим классом широко применяемых препаратов являются нитропрепараты (различные формы нитросорбида и мононитрата, препарат чистой аэрозольной формы нитроглицерина - нитроминт) (Регистр лекарственных средств России. Энциклопедия лекарственных средств. - Москва, 2003. - С.588, С.332, С.587). Помимо этих препаратов можно использовать природные или синтетические сердечные гликозиды (препараты наперстянки, строфанта, ландыша) (Машковский М.Д. Лекарственные средства. - М.: Новая волна, 2004. - С.215). Наряду с сердечными гликозидами деятельность сердца усиливают негликозидные кардиотоники. В качестве кардиотоников назначают симпатомиметические (адренергические) препараты: добутамин, допамин (Регистр лекарственных средств России. Энциклопедия лекарственных средств. - Москва, 2003. - С.296, С.305). В определенной мере кардиотоническими свойствами обладают вещества, оказывающие общее положительное влияние на метаболические процессы организма.
Недостатком этих препаратов является то, что эти препараты не лишены побочных эффектов и противопоказаний. В частности, большинство препаратов оказывает подавляющий эффект на чувствительность миокарда к возбуждению, вызывают аритмии, сердечную недостаточность, гипотонию, брадикардию, а также синдром отмены.
Среди известных лекарственных препаратов, применяемых при лечении ишемии миокарда, необходимо также упомянуть актовегин (Регистр лекарственных средств России. Энциклопедия лекарственных средств. - Москва, 2003. - С.63), как препарат, действующий на метаболизм клетки и улучшающий энергозависимые процессы обмена в ткани, однако его действие не является специфическим.
Известны пептидные препараты, действующие на функцию миокарда. К ним относятся опиоидные пептиды (Усынин А.Ф., Павленко B.C., Хлыстов В.В. Ишемическое повреждение миокарда и влияние на него некоторых фармакологических препаратов у крыс в эксперименте. Актуальные вопросы кардиологии. Вып.2. - Томск: Изд-во Томского ун-та, 1987. - С.116-118) и их синтетический аналог даларгин (Регистр лекарственных средств России. Энциклопедия лекарственных средств. - Москва, 2003. - С.249).
Известно применение даларгина для лечения инфаркта миокарда как способ профилактики фибрилляций желудочков сердца (патент РФ №2032422 “Способ лечения инфаркта миокарда”, МКИ6 А 61 К 38/00, 1995). Кроме того, известно средство, улучшающее функциональное состояние миокарда путем коррекции нарушений метаболизма, основывающееся на сочетанном применении даларгина и солкосерила (патент РФ 2061484 “Способ лечения острого периода инфаркта миокарда”, МКИ6 А 61 К 35/14, А 61 К 38/33, 1996).
Известен также препарат полипептидной природы (патент РФ №1417242 на изобретение "Способ получения вещества, восстанавливающего функцию миокарда", МКИ А 61 К 35/24, 1989), полученный из сердца животных и обладающий аналогичной биологической активностью, который является наиболее близким аналогом, принятым за прототип по отношению к фармакологическому средству (фармацевтической композиции).
Однако применение этого препарата ограничено в связи со сложностью способа получения, малым выходом активных веществ, значительной вариабельностью их физико-химических свойств, а также из-за возможного возникновения у больных побочного действия в виде аллергических реакций.
Следует отметить, что заявляемое пептидное соединение - тетрапептид - структурных аналогов не имеет.
Заявляемое изобретение направлено на получение нового биологически активного соединения пептидной природы, восстанавливающее функцию миокарда.
Технический результат изобретения заключается в создании нового пептидного соединения, а также фармакологического средства (фармацевтической композиции), содержащего это пептидное соединение в качестве активного пептидного агента, использование которого в медикаменте способствует восстановлению функции миокарда.
Возможность объективного проявления технического результата при использовании изобретения подтверждена достоверными данными, приведенными в примерах, содержащих сведения экспериментального характера, полученные по методикам, принятым в данной области.
Настоящее изобретение относится к новому тетрапептиду аланил-глутамил-аспартил-аргинин общей формулы Ala-Glu-Asp-Arg последовательности 1 [SEQ ID NO:1].
Тетрапептид получают классическим методом пептидного синтеза в растворе (Якубке Х. - Д., Ешкайт X. Аминокислоты, пептиды, белки: Пер. с нем. - М.: Мир, 1985. - 456 с.).
Настоящее изобретение относится к тетрапептиду аланил-глутамил-аспартил-аргинин общей формулы Ala-Glu-Asp-Arg последовательности 1 [SEQ ID NO:1], обладающему биологической активностью, проявляющейся в восстановлении функции миокарда.
Действие тетрапептида Ala-Glu-Asp-Arg, направленное на восстановление функции миокарда, выявлено при его изучении в экспериментальной патологии, в частности при использовании следующих моделей:
- влияние тетрапептида на течение экспериментального инфаркта миокарда при перевязке коронарной артерии у крыс;
- влияние тетрапептида на состояние изолированного сердца при перфузии и ишемии;
- влияние тетрапептида на течение адреналиновой дистрофии миокарда у крыс;
- выявлении протекторного действия тетрапептида при экспериментальных токсикохимических миокардиопатиях;
- влияние тетрапептида на течение и исход хлоркальциевой аритмии у крыс;
- влияние тетрапептида на рост эксплантатов органотипической культуры сердца половозрелых крыс;
- влияние тетрапептида на биоэнергетику кардиомиоцитов.
Как известно, перечисленные патологии характеризуются формированием зон некроза кардиомиоцитов, несбалансированным протеканием кислородзависимых реакций в миокарде: процессов биологического окисления с ростом энергодефицита, повышенный расход макроэргических соединений, накоплением недоокисленных соединений, продуктов перекисного окисления липидов. Нарушаются транспорт и обмен кальция, его распределение между клеточными пулами и межклеточным пространством. Отмеченные изменения приводят к нарушению сократительной функции миокарда, аритмии и вызывают развитие патологии сердечно-сосудистой системы.
В результате экспериментального изучения установлено, что тетрапептид Ala-Glu-Asp-Arg не обладает токсичностью.
Настоящее изобретение также относится к фармакологическому средству (фармацевтической композиции), восстанавливающему функцию миокарда, содержащему в качестве активного пептидного агента эффективное количество тетрапептида аланил-глутамил-аспартил-аргинин общей формулы Ala-Glu-Asp-Arg последовательности 1[SEQ ID NO:1].
Понятие “фармакологическое средство”, используемое в данной заявке, подразумевает использование такой лекарственной формы, содержащей эффективное количество тетрапептида общей формулы Ala-Glu-Asp-Arg, которая может найти профилактическое и/или лечебное применение в медицине в качестве средства, восстанавливающего функцию миокарда.
Понятие "эффективное количество", используемое в данной заявке, подразумевает использование такого количества активного пептидного агента, которое в соответствии с его количественными показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме.
Для получения фармацевтических композиций, отвечающих изобретению, предлагаемый тетрапептид как активный ингредиент смешивается с фармацевтически приемлемым носителем согласно принятым в фармацевтике способам компаундирования.
Носитель может иметь различные формы, которые зависят от лекарственной формы препарата, желаемой для введения в организм, например, парентерального или перорального.
При изготовлении композиций в предпочтительной дозированной форме для перорального применения могут использоваться известные фармацевтические компоненты.
Для парентерального введения носитель обычно включает стерильный 0,9% раствор хлорида натрия или стерильную воду, хотя могут быть включены другие ингредиенты, способствующие стабильности препарата.
Сущность изобретения поясняется таблицами, приведенными в конце описания.
В Таблице 1 показано влияние тетрапептида Ala-Glu-Asp-Arg на биохимические показатели в миокарде крыс при экспериментальном инфаркте (вариант лечения).
В Таблице 2 показано влияние тетрапептида Ala-Glu-Asp-Arg на состояние изолированного сердца морских свинок (вариант лечения).
В Таблице 3 показано влияние тетрапептида Ala-Glu-Asp-Arg на показатели сократительной способности изолированного сердца крыс после ишемии.
В Таблице 4 показано влияние тетрапептида Ala-Glu-Asp-Arg на показатели перекисного окисления липидов в миокарде крыс при адреналиновой дистрофии через сутки после ее создания.
В Таблице 5 показано влияние тетрапептида Ala-Glu-Asp-Arg на активность дегидрогеназ и содержание гликогена в миокарде крыс через 4 часа после адреналиновой дистрофии.
В Таблице 6 показано влияние тетрапептида Ala-Glu-Asp-Arg на цитоморфологические показатели в миокарде при отравлении крыс тетраметилурамдисульфидом.
В Таблице 7 показано влияние тетрапептида Ala-Glu-Asp-Arg на показатели течения и исхода хлоркальцевой анемии у крыс.
В Таблице 8 показано влияние тетрапептида Ala-Glu-Asp-Arg на рост органотипических эксплантатов ткани миокарда.
В Таблице 9 показано влияние тетрапептида Ala-Glu-Asp-Arg на морфологические и биохимические показатели периферической крови морских свинок.
Настоящее изобретение иллюстрируется примером синтеза тетрапептида формулы Ala-Glu-Asp-Arg (пример 1), примерами, подтверждающими биологическую активность тетрапептида (примеры 2, 3, 4, 5, 6, 7, 8), примером испытания тетрапептида на токсичность (пример 9), демонстрирующими его фармакологические свойства и подтверждающими терапевтическую активность фармацевтической композиции.
Пример 1. Синтез тетрапептида Ala-Glu-Asp-Arg.
1. Название соединения: L-аланил-L-глутамил-L-аспартил-L-аргинин
2. Структурная формула: H-Ala-Glu-Asp-Arg-OH
3. Брутто-формула без противоиона: C18H31N7O9
4. Молекулярный вес без противоиона: 489,48
5. Противоион: ацетат
6. Внешний вид: белый аморфный порошок без запаха
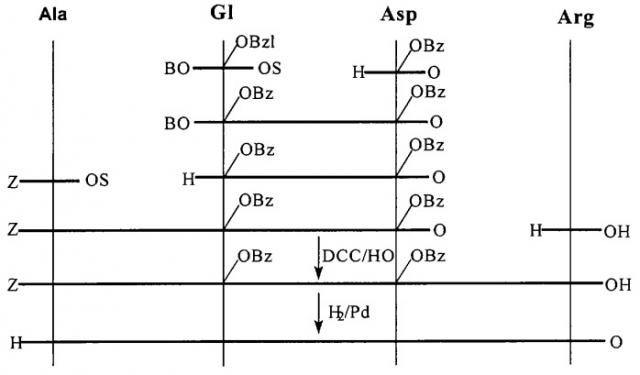
7. Способ синтеза: пептид получен классическим методом синтеза в растворе по схеме
Z - бензилоксикарбонильная группа;
ВОС - трет.бутилоксикарбонильная группа;
OSu - N-оксисукцинимидный эфир;
OBzl - бензиловый эфир;
DCC -N,N'-дициклогексилкарбодиимид;
НОВТ - N-оксибензотриазол.
В качестве растворителя используют N,N'-диметилформамид, при введении аспарагиновой кислоты используют защиту α-СООН группы солеобразованием с триэтиламином. Деблокирование ВОС-защитной группы проводят раствором трифторуксусной кислоты (TFA), Z-защитной группы - каталитическим гидрогенолизом. Выделение и очистку препарата осуществляют методом препаративной ВЭЖХ на колонке с обращенной фазой. 8. Характеристики готового препарата:
- аминокислотный анализ: Glu 1,08; Asp 1,08; Ala 1,00; Arg 1,07;
- содержание основного вещества 98,01% (по ВЭЖХ, 220 нм);
- ТСХ - индивидуален, Rf=0,59 (ацетонитрил-уксусная к-та-вода 5:1:3);
- содержание влаги: 8%;
- рН 0,001% раствора: 4,58;
- удельное оптическое вращение: [α]D 22: -24° (c=1, H2O).
Пример синтеза:
1) BOC-Glu(OBzl)-Asp(OBzl)-OH (I), N-трет.бутилоксикарбонил-(γ-бензил)-глутамил-(β-бензил)-аспартат.
N-оксисукцинимидный эфир N-трет.бутилоксикарбонил-(γ-бензил)глутаминовой кислоты BOC-Glu(OBzl)-OSu 4,34 г (0,01 моль) растворяют в 20 мл диметилформамида, добавляют триэтиламин 1,72 мл (0,0125 моль) и β-бензиласпартат 2,80 г (0,0125 моль). Перемешивают при комнатной температуре в течение 24 час.
Продукт высаживают 0,5 н раствором серной кислоты (150 мл), экстрагируют в этилацетат (3×30 мл), промывают 0,5 н раствором серной кислоты (2×20 мл) водой, 5% раствором бикарбоната натрия (1×20 мл), водой, 0,5 н раствором серной кислоты (2×20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40°С, остаток сушат в вакууме над P2O5. Получают масло 5,68 г (≈100%).
Rf=0,42 (бензол-ацетон 2:1, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление УФ и хлор/бензидин).
2) TFA-H-Glu(OBzl)-Asp(OBzl)-OH (II), трифторацетат (γ-бензил)-глутамил-(β-бензил)-аспартат.
N-трет.бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартат (I) 5,68 г (≈0,01 моль) растворяют в 20 мл смеси дихлорметан-трифторуксусная кислота (3:1). Через 2 часа растворитель упаривают в вакууме при 40°С, упаривание повторяют с новой порцией дихлорметана (2×10 мл), остаток сушат в вакууме над NaOH. Получают масло 5,80 г (≈100%). Rf=0,63 (н-бутанол-пиридин-уксусная кислота-вода, 15:10:3:12).
3) Z-Ala-Glu(OBz1)-Asp(OBz1)-OH (III), N-карбобензоксиаланил-(γ-бензил)глутамил-(β-бензил)аспартат.
Трифторацетат(γ-бензил)глутамил-(β-бензил)аспартат (II) 5,65 г (0,01 моль) растворяют в 10 мл диметилформамида, добавляют триэтиламин 2,80 мл (0,02 моль) и N-оксисукцинимидный эфир N-карбобензоксиаланина 4,14 г (0,013 моль). Смесь перемешивают в течение 24 часов при комнатной температуре.
Продукт высаживают 0,5 н раствором серной кислоты (150 мл), экстрагируют в этилацетат (3×30 мл), промывают 0,5 н раствором серной кислоты (2×20 мл), водой, 5% раствором бикарбоната натрия (1×20 мл), водой, 0,5 н раствором серной кислоты (2×20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40°С, остаток закристаллизовывают в системе этилацетат/гексан. Продукт отфильтровывают и сушат в вакууме над Р2O5. Выход 4,10 г (66%). Т. пл.=154°С.
Rf=0,48 (бензол-ацетон, 1:1), Rf=0,72 (н-бутанол-пиридин-уксусная кислота-вода, 15:10:3:12).
4) Z-Ala-Glu(OBzl)-Asp(OBzl)-Arg-OH (IV), N-карбобензоксиаланил-(γ-бензил)-глутамил-(β-бензил)аспартиларгинин.
Растворяют N-карбобензоксиаланил-(γ-бензил)глутамил-(β-бензил)аспартат (III) 5,0 г (8 ммоль) и N-оксибензотриазол 1,35 г (10 ммоль) в 20 мл диметилформамида, охлаждают смесь до 0°С и добавляют охлажденный раствор N,N’-дициклогексилкарбодиимида 2,0 г (10 ммоль) в 5 мл, перемешивают в течение 20 мин. Затем добавляют охлажденную суспензию HClH-Arg-OH, гидрохлорида аргинина 5,00 г (24 ммоль) в 15 мл диметилформамида, перемешивают в течение 2 часов реакционную смесь при 0°С и оставляют на ночь перемешиваться при комнатной температуре. Осадок дициклогексилмочевины и избыток аргинина отфильтровывают. В фильтрат выливают 0,5 л 2 н H2SO4 до образования желтого осадка, оставляют на ночь в холодильнике. Осадок растворяют в 100 мл н-бутанола, насыщенного 2% уксусной кислотой, и несколько раз промывают 2% уксусной кислотой. Органический слой промывают водой до нейтрального значения рН и упаривают в вакууме. Остаток закристаллизовывают в диэтиловом эфире, отфильтровывают и сушат над P2O5. Выход 2,5 г (45%).
Rf=0,88 (н-бутанол-уксусная к-та-вода 4:1:1).
5) H-Ala-Glu-Asp-Arg-OH (V), аланил-глутамил-аспартил-аргинин.
N-карбобензоксиаланил-(γ-бензил)глутамил-(β-бензил)аспартиларгинин (III) 2,50 г гидрируют в системе метанол-вода (5:1) над катализатором Pd/C. Контроль за полнотой деблокирования в ТСХ системах бензол-ацетон (2:1) и ацетонитрил-уксусная кислота-вода (5:1:3). По окончании реакции катализатор отфильтровывают, фильтрат упаривают в вакууме и остаток закристаллизовывают в системе вода/метанол. Продукт сушат в вакууме над КОН. Выход 1,00 г (70%).
Rf=0,59 (ацетонитрил-уксусная к-та-вода, 5:1:3). Для очистки 250 мг препарата растворяют в 4 мл 0,01% трифторуксусной кислоты и подвергают высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50×250 мм Diasorb-130-C16T, 7 mkm. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module.
Условия хроматографирования - A: 0,1% TFA; В: MeCN/0,l% TFA; градиент В 0→10% за 100 мин. Объем пробы 5 мл, детекция при 215 нм, сканирование 190-600 нм, скорость потока 10 мл/мин.
Отбирают фракцию 49,0-54,0 мин. Растворитель упаривают в вакууме при температуре не выше 40°С и повторяют очистку методом ВЭЖХ в тех же условиях. Отбирают фракцию 32-48 мин. Растворитель упаривают, упаривание многократно (5 раз) повторяют с 10 мл 10% раствора уксусной кислоты. Окончательно остаток растворяют в 20 мл деионизованной воды и лиофилизуют. Получают 110 мг очищенного препарата в виде аморфного белого порошка без запаха.
6) Анализ готового препарата.
- Содержание основного вещества определяют методом ВЭЖХ на колонке Supelco LC-18-DB 4,6×250 mm, gard. LC-18-DB. A: 0,1% TFA; В: MeCN/0,1%TFA; grad. В 0→10% за 30 мин. Скорость потока 1 мл/мин. Детекция при 220 нм, сканирование 190-600 нм, проба 20 μl. Содержание основного вещества 98,01%;
- Аминокислотный анализ проводят на анализаторе ААА "Т-339" Prague. Гидролиз в 6 н НСl при 125°С 24 час. Glu 1,08; Asp 1,08; Ala 1,00; Arg 1,07;
- ТСХ: индивидуален, Rf=0,59 (ацетонитрил-уксусная к-та-вода, 5:1:3 пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление хлор/бензидин);
- Содержание влаги: 8% (определяют гравиметрически по потере массы при сушке 20 мг при 100°С). рН 0,001% раствора: 4,58 (потенциометрически);
- Удельное оптическое вращение: [α]D 22:-24° (c=1, H2O), "Polamat A", Carl Zeiss Jena.
Пример 2. Влияние тетрапептида на течение экспериментального инфаркта миокарда при перевязке коронарной артерии у крыс.
Эксперимент проведен на 40 белых беспородных крысах массой 180-200 г. Животные были рандомизированно разделены на две группы по 20 животных в каждой. Инфаркт миокарда (ИМ) воспроизводили перевязкой левой коронарной артерии. Тетрапептид А1а-Glu-Asp-Arg вводили животным внутрибрюшинно в дозе 0,05 мкг/животное в стерильном 0,9% растворе NaCl трехкратно - через 1, 3, 5 часов после коронароокклюзии. Крыс декапитировали через 6 и 24 часа после операции. Контролем служили оперированные животные, получавшие внутрибрюшинно 0,9% раствор NaCl. Размеры зоны ИМ определяли гравиметрически. Фрагменты миокарда фиксировали для световой, электронной микроскопии, часть материала замораживали в жидком азоте для биохимических исследований.
Результаты эксперимента приведены в Таблице 1. Введение тетрапептида Ala-Glu-Asp-Arg приводило к значительному снижению летальности у крыс в течение первых суток после инфаркта (45% среди контрольных животных и 15% в группе крыс после применения тетрапептида). Гистологически это проявлялось в достоверном уменьшении зон некроза у животных после применения тетрапептида уже в первые часы развития заболевания. При анализе динамики изменения биохимических показателей видно, что пептидный препарат достоверно снижает почти в 1,5 раза содержание в крови глюкозы, вызванное острой ишемией миокарда. Это происходит, главным образом, за счет сохранения нормальной активности маркерных ферментов - лактатдегидрогеназы (ЛДГ) и креатинфосфокиназы (КФК). Протекторное действие тетрапептида в данной модели проявляется также в сохранении содержания гликогена в ткани миокарда, которое без применения препарата снижается в 3 раза.
Ультраструктурные изменения состояния кардиомиоцитов были изучены с помощью электронной микроскопии. При изучении 180 электронограмм было обнаружено, что особенно отчетливо протекторное действие тетрапептида выявляется по сохранности структур митохондрий через 24 часа от начала ИМ. Под действием препарата коэффициент энергетической эффективности митохондрий (выраженное в процентах отношение произведения среднего суммарного количества крист на сумму площадей митохондрий в одной электронограмме при патологии к тем же показателям нормального сердца) достоверно возрастает по отношению к контрольным животным (93,2±2,3 и 41,5±2,4 соответственно р<0,05).
Таким образом, тетрапептид значительно ослабляет ишемическое повреждение околоинфарктного миокарда и стимулирует в нем репаративные процессы, что приводит к сохранению жизнеспособности кардиомиоцитов и нормализации их ультраструктуры, в то время как у контрольных животных происходит нарастание тяжести ишемического повреждения, заканчивающееся их гибелью.
Пример 3. Влияние тетрапептида на состояние изолированного сердца при перфузии и ишемии.
Эксперимент проведен при перфузии изолированных сердец 60 морских свинок самцов, по Лагендорфу. Животные были рандомизированно разделены на группы по 6 животных в каждой. Тотальную ишемию сердца создавали путем полного пережатия подающего перфузионный раствор шланга на 30 мин. Затем начинали реперфузию при тех же условиях, что и до ишемии (контрольная группа). В группе подопытных животных проводили перфузию в присутствии тетрапептида Ala-Glu-Asp-Arg в концентрациях 0,002-0,05 мкг/мл. Вели запись механических сокращений, в процессе опыта несколько раз производили забор биоптатов из верхушки сердца массой около 10 мг, в дальнейшем определяли в них содержание малонового диальдегида (МДА). Сердца в конце опыта и часть сердец до ишемии замораживали в жидком азоте для определения содержания АТФ, АДФ и АМФ.
В другом эксперименте исследовали влияние тетрапептида на восстановление сократительной способности изолированного сердца крысы после периода ишемии. Исследование проводили на 3 группах по 8 животных в каждой в более напряженном режиме работы сердечной мышцы при навязанном ритме сокращений и повышении температуры перфузионного раствора до 37°С.
Результаты эксперимента приведены в Таблицах 2 и 3. Анализ полученных данных показывает, что действие тетрапептида на нормальное и ишемизированное сердце различно. Применение тетрапептида не влияет на состояние нормального сердца, в то время как при ишемии наличие препарата в перфузате в малых дозах от 0,002 до 0,005 мкг/мл благоприятно сказывается на работе сердца в состоянии ишемии. Отмечено увеличение силы и амплитуды сердечных сокращений, достоверно повысилось содержание макроэргических фосфатов при содержании МДА, достоверно не отличающемся от нормы. Добавление тетрапептида в перфузионный раствор в концентрации 0,005 мкг/мл приводило к значительному улучшению сократительной функции - возрастала амплитуда сокращений (до 75±12% от исходной при уровне у животных контрольной группы 43±7%). Скорости сокращения и расслабления были достоверно выше у животных подопытной группы, коронарный проток достоверно увеличился до 10,8±1,6 мл/мин по сравнению с животными контрольной группы (8,5±0,4 мл/мин, р<0,05).
В другой серии опытов на 12 сердцах крыс провели исследование протекторного влияния тетрапептида при его добавлении в перфузат в концентрации 10 нг/мл до создания ишемии. Затем проводили “жесткую” стимуляцию (частота 5 Гц) сердца и оценивали сократительную активность. При изучении протекторного действия тетрапептида при его введении до создания ишемии было показано, что тетрапептид в дозе 0,005 мкг/мл сдерживал рост контрактуры в период ишемии и способствовал ее снижению по мере реперфузии, в то время как в контрольных сердцах после стимуляции не происходило восстановления нормальной сократительной активности при реперфузии, что приводило к полной остановке сокращений уже через 5 минут реперфузии. Введение тетрапептида в очень малой дозе 0,005 мкг/мл предохраняло сердце, находящееся на грани остановки, от фибрилляции и снижения сократительной активности, восстанавливая ее.
Пример 4. Влияние тетрапептида на течение адреналиновой дистрофии миокарда у крыс.
Эксперимент проведен на 30 белых беспородных крысах массой 180-200 г. Животные были рандомизированно разделены на три группы по 10 животных в каждой. Адреналиновую дистрофию создавали введением свежеприготовленного раствора адреналина (“Серва”, США) внутрибрюшинно в дозе 2 мг/кг. Животным контрольной группы вводили 0,9% раствор NaCl. Затем животным подопытной группы через 1 и 5 часов вводили тетрапептид Ala-Glu-Asp-Arg в дозе 0,05 мкг/животное в стерильном 0,9% растворе NaCl. Через 4 часа от начала эксперимента у животных были взяты биоптаты сердечной мышцы массой около 10 мг для определения активности сердечных дегидрогеназ и содержания гликогена в миокарде. Через 1 сутки животных забивали одномоментной декапитацией. Кусочки левого желудочка замораживали в жидком азоте. В криостатных срезах гистохимически определяли активность сукцинатдегидрогеназы (СДГ), НАДН-дегидрогеназы (НАДН-ДГ), лактагдегидрогеназы и содержание гликогена.
Результаты исследования представлены в таблицах 4 и 5.
Проведенные исследования показали, что введение тетрапептида одновременно с сильной адренергической стимуляцией миокарда заметно снижает интенсивность процесса ПОЛ, который является одним из повреждающих миокард факторов в данной модели. Через 1 сутки после создания дистрофии миокарда количество диеновых конъюгатов в миокарде у животных подопытной группы достоверно снизилось до нормальных показателей по сравнению с животными контрольной группы (110±17 и 176±24 нмоль/г ткани соответственно, р<0,05).
Гистохимическое исследование активности дегидрогеназ и содержания гликогена в ткани миокарда в первые часы после введения адреналина (Таблица 5) показало, что тетрапептид достоверно снижает активность лактагдегидрогеназы, что способствует уменьшению ацидоза и лучшей сохранности сердечной мышцы в условиях кислородного голодания. Это подтверждается сохранением количества гликогена в сердце крыс, получавших тетрапептид, по сравнению с контрольными животными (0,168±0,021 и 0,112±0,0,17 отн. ед. оптич. плотности соответственно).
Таким образом, применение тетрапептида Ala-Glu-Asp-Arg оказывает протекторный эффект в отношении действия адреналина на ферментные системы организма, что позволяет снизить избыточную интенсивность процессов липидной пероксидации и уменьшить развитие некробиотической мелкоочаговой адреналиновой дистрофии миокарда.
Пример 5. Протекторное действие тетрапептида при экспериментальной токсикохимической миокардиопатии при отравлении тетраметилтиурамдисульфидом.
Эксперимент проведен на 40 белых беспородных крысах массой 220-230 г. Животные были рандомизированно разделены на четыре группы. Затравливание животных промышленным ядом тетраметилурамдисульфидом (ТМТД) проводили введением в течение 20 дней 5% масляного раствора ТМТД в дозе 25 мг/кг внутрижелудочно. Тетрапептид вводили в течение последних 10 дней эксперимента внутримышечно в дозе 0,05 мкг/животное в стерильном 0,9% растворе NaCl. По истечении указанных сроков контрольных и подопытных животных забивали одномоментной декапитацией. Кусочки миокарда фиксировали в 12% растворе формалина. Парафиновые срезы окрашивали гематоксилином-эозином, а также по Ван-Гизону, Браше, Суданом III, IV. Контролем служили интактные животные.
Результаты исследования представлены в Таблице 6.
Морфологическое исследование показало корригирующее действие тетрапептида при затравке животных промышленным ядом ТМТД. Результаты гистологического и морфометрического изучения выявили, что при введении тетрапептида интактным животным несколько увеличивались наполнение миокарда и объем ядер кардиомиоцитов (на 11% и 14% соответственно). На фоне поражающего действия ТМТД исследуемый препарат достоверно способствовал восстановлению ядерно-цитоплазматического соотношения (от 0,16±0,02 при затравке до 0,28±0.03), снижал объем стромы (от 0,218±0,01 см3/см3 у затравленных животных до 0,180±0,02 см3/см3), увеличивал объем паренхимы до нормальных значений.
Таким образом, проведенное исследование показало, что под действием тетрапептида происходят восстановление структуры миокарда и нормализация основных объемных соотношений в сердечной мышце затравленных животных. Это свидетельствует о положительном влиянии препарата на ускоренное восстановление функции сердца при отравлении промышленным ядом.
Пример 6. Влияние тетрапептида на течение и исход хлоркальциевой аритмии у крыс.
Эксперимент проведен на 60 белых беспородных крысах массой 180-200 г. Животные были рандомизированно разделены на 6 групп по 10 животных в каждой. Крыс наркотизировали уретаном и вводили по 220 мг/кг 10% раствора CaCl2. Тетрапептид Ala-Glu-Asp-Arg вводили животным внутрибрюшинно однократно в дозах 0,05-1,0 мкг/кг в стерильном 0,9% растворе NaCl.
Результаты исследования, представленные в Таблице 7, показали, что наиболее эффективной является доза 0,2 мкг/кг. При введении тетрапептида снижается летальность животных, достоверно уменьшается частота развития фибрилляции желудочков, увеличиваются частота восстановления синусового ритма после первого введения CaCl2 и переносимая доза аритмогена. Препарат в дозировках 0,2 мкг/кг и 0,5 мкг/кг способствовал нормализации частоты сердечных сокращений (ЧСС): при этом у крыс с брадикардией ЧСС увеличилась на 12,3-48,6%, а у крыс с исходной тахикардией тетрапептид уменьшал ЧСС до нормальных показателей.
Таким образом, введение тетрапептида Ala-Glu-Asp-Arg способствует нормализации сердечной деятельности при аритмии.
Пример 7. Влияние тетрапептида на рост эксплантатов органотипической культуры сердца половозрелых крыс.
Эксплантаты тканей сердца (левого и правого желудочков) половозрелых крыс линии Вистар культивировали в чашках Петри с коллагеновым покрытием дна. Питательная среда состояла из 35% среды Игла, 35% раствора Хенкса, 25% фетальной телячьей сыворотки и 5% куриного эмбрионального экстракта с добавлением глюкозы, инсулина, гентамицина и глютамина. Исследуемый тетрапептид Ala-Glu-Asp-Arg добавляли в культуральную среду в фиксированной концентрации от 0,01 до 20,0 нг/мл питательной среды. После инкубирования в течение 3 сут при температуре 37°С оценивали увеличение площади эксплантатов под фазово-контрастным микроскопом. Биологическое действие препарата выражали в изменении индекса площади (ИП) эксплантатов, выросших в среде с пептидом, по сравнению с контрольными.
Результаты эксперимента приведены в Таблице 8, из которой следует, что тетрапептид Ala-Glu-Asp-Arg стимулирует рост эксплантатов органотипической культуры сердца в широком диапазоне концентраций. В интенсивной зоне роста под влиянием тетрапептида были выявлены выделяющиеся миокардиоциты с характерными для незрелых клеток большими круглыми ядрами, а также эндотелиальные клетки и фибробласты. С помощью иммуногистохимического метода выявления пролиферативного ядерного антигена (PCNA) с последующим компьютерным анализом микроскопических изображений установлено, что ведущую роль в механизме действия тетрапептида Ala-Glu-Asp-Arg играет усиление пролиферативного потенциала клеток.
Таким образом, применение тетрапептида Ala-Glu-Asp-Arg способствует ускоренному обновлению клеточной популяции кардиомиоцитов с нормальными свойствами и, таким образом, стимулирует функцию ткани миокарда.
Пример 8. Влияние тетрапептида на биоэнергетику кардиомиоцитов.
Кардиомиоциты выделяли из сердечной мышцы взрослых крыс по методу Vahouny. Потребление кислорода изолированными кардиомиоцитами регистрировали полярографически при температуре 30°С. Оксигенацию части суспензии кардиомиоцитов осуществляли насыщением ее карбогеном в течение 1-3 часов при комнатной температуре. Другую часть суспензии не оксигенировали (условия умеренной гипоксии). Сукцинат добавляли в концентрации 1×10-4 М и по степени стимуляции потребления кислорода оценивали повреждение биоэнергетики клетки в условиях гипоксии. Тетрапептид добавляли в среду в концентрации 10 нг/мл.
Результаты исследования показали, что при введении тетрапептида в среду происходила нормализация процесса окисления сукцината. Так, в условиях гипоксии коэффициент стимуляции дыхания (отношение скорости дыхания в присутствии сукцината к исходной скорости дыхания) был равен 7,35±0,26, а при добавлении тетрапептида он снизился до 1,97±0,26. При этом потребление кислорода не менялось, если тетрапептид добавляли к суспензии оксигенированных клеток. Было показано, что при добавлении в среду тетрапептида возрастает окисление НАД·Н2 кардиомиоцитами. Таким образом, тетрапептид, избирательно ингибируя окисление янтарной кислоты и способствуя окислению НАД·Н2, нормализует биоэнергетику кардиомиоцитов в условиях кислородной недостаточности.
Дополнительные исследования, проведенные на срезах миокарда различных животных, продемонстрировали ингибирующее действие тетрапептида на активность сукцинатдегидрогеназы, что и является, по-видимому, механизмом защитного действия тетрапептида на процессы дыхания в клетках миокарда при гипоксии.
Пример 9. Изучение общетоксического действия тетрапептида
Общетоксическое действие тетрапептида Ala-Glu-Asp-Arg исследовали в соответствии с требованиями “Руководства по экспериментальному (доклиническому) изучению новых фармакологических веществ” (2000): острой токсичности при однократном введении препарата, а также подострой и хронической токсичности при длительном введении тетрапептида.
Исследование по изучению острой токсичности проведено на 66 белых беспородных мышах-самцах массой 20-23 г. Животные были рандомизированно разделены на 6 равных групп. Препарат вводили животным однократно внутримышечно в объеме 0,25 мл в дозах 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг в стерильном 0,9% растворе NaCl. Животным контрольной группы в том же объеме вводили 0,9% раствор NaCl.
Исследования по изучению подострой токсичности проведено на 60 белых беспородных крысах-самцах массой 160-240 г. Ежедневно однократно животным подопытных групп вводили препарат внутримышечно в течение 90 дней в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл 0,9% раствора NaCl. Животным контрольной группы вводили в том же объеме 0,9% раствор NaCl. До введения препарата, на 30, 60 и 90 сутки после начала введения препарата у животных исследовали морфологический состав и свойства периферической крови. При завершении эксперимента исследовали биохимические и коагулологические показатели крови.
Исследования по изучению хронической токсичности проводили в течении 6 месяцев, исходя из длительности рекомендуемого клинического назначения препарата, на 96 морских свинках-самцах массой 300-340 г. Животные опытных групп получали ежедневно однократно внутримышечно тетрапептид в течение 6 месяцев в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл 0,9% раствора NaCl. В контрольной группе животных вводили по аналогичной схеме 0,9% раствор NaCl в том же объеме. У животных в периферической крови общепринятыми методами определяли: количество эритроцитов, гемоглобина, ретикулоцитов, тромбоцитов, лейкоцитов, лейкоцитарную формулу, скорость оседания эритроцитов (СОЭ), резистентность эритроцитов. Наряду с этим определяли содержание в сыво