Способ скриннингового выявления лиц группы риска развития патологии нервной системы и мониторинга за состоянием больных, страдающих нервно-психическими заболеваниями
Иллюстрации
Показать всеИзобретение относится к области медицины и касается способа скриннингового выявления лиц группы риска развития патологии нервной системы и мониторинга за состоянием больных, страдающих нервно-психическими заболеваниями. Способ включает забор крови, получение сыворотки, проведение иммуноферментного анализа для определения содержания антиидиотипических антител к антигенам нервной ткани и скрининг пациентов по уровню определяемых антител, в котором дополнительно определяют иммунореактивность идиотипических антител к ней ромедиатором нервной системы ГАМК, глутамину, дофамину, серотонину и к антигенам нервной ткани: белкам S100, GFAP, MBP и NGF и к рецепторам нейромедиаторов и по степени выраженности отклонений от нормы и соотношения идиотипических и антиидиотипических антител определяют уровень риска нарушений развития нервной системы. Преимущество изобретения заключается в возможности прогнозирования указанных нарушений до выраженных клинических изменений.
Реферат
Изобретение относится к области медицины и может найти применение при скриннинге нервно-психических заболеваний.
Известно, что вызванные разными внешними или внутренними причинами сбои в механизмах иммунорегуляции, в том числе врожденные, могут сопровождаться нарушениями формирования и функционального созревания нервной системы ребенка или развитием нарушений в деятельности нервной системы взрослого человека (В.В.Абрамов, Взаимодействие нервной и иммунной систем. Новосибирск, Наука, 1988; А.Б.Полетаев и др., Нейроиммунология, 2003, 1,1, 11-20).
Иммунная система здорового человека постоянно продуцирует естественные регуляторные аутоантитела (е-аАТ) к любым антигенным компонентам собственного организма, в том числе, е-аАТ к компонентам нервных клеток или нейротропные е-аАТ (Полетаев А.Б. и др., Регуляторная метасистема, М.: Медицина, 2002). Синтез е-аАТ в здоровом организме поддерживается в определенных границах, необходимых для выполнения последними определенных регуляторных функций, а их избыточная, равно как и недостаточная продукция могут вести к развитию патологических состояний, в том числе, затрагивающих формирование и/или деятельность нервной системы.
Известен способ определения степени риска развития нервно-психических заболеваний путем определения с помощью иммуноферментного анализа иммунореактивности сывороточных антител к Р(ab)2-фрагментом антиидиотипических антител, специфически связывающих антитела к антигенам нервной ткани и при получении данных об отклонении иммунореактивности тестируемых сывороток от уровня нормальных значений и по степени выраженности отклонений определяют степень риска развития нервно-психических заболеваний, исходя из данных "Таблицы прогноза", полученной по результатам клинических наблюдений (патент РФ №2147128, зарегистрирован 27.03.2000 "Способ скриннинга нервно-психических заболеваний" авторы: Полетаев А.Б., Морозов С.Г., Клюшник Т.П., Будыкина Т.С., Выбищевич Н.К., Гнеденко Б.Б.). В качестве антигенов нервной ткани используют Р(аb)2-фрагментом антиидиотипических антител, специфически связывающих антитела с направленностью к антигенам нервной ткани S100, GFAP, MP65, NGF. Недостатком известного способа является его сравнительно невысокая точность. Во-первых, он позволяет оценивать содержание е-аАТ лишь к четырем белковым компонентам нервных клеток (белки S100, GFAP, МР-65 и NGF). Соответствующие изменениям частот, но не всегда, являются характерным признаком нервно-психических заболеваний.
Во-вторых, он позволяет регистрировать патологические изменения в сывороточном содержании лишь е-аАТ первого порядка (идиотипических). Этого недостаточно для суждения о давности патологического процесса и стадии его развития.
Задачей изобретения является повышение точности способа.
Поставленная задача решается тем, что дополнительно определяют иммунореактивность сывороточных антител к F(ab)-фрагментам нейромедиаторов нервной системы ГАМК, глутамату, дофамину, серотонину и их антиген-связывающим фрагментам или молекулам идиотипических антител к указанным нейромедиаторам и при отклонении иммунореактивности тестируемых сывороток от уровня нормальных значений до степени выраженности отклонений определяют уровень риска нарушений развития нервной системы у детей, риска возникновения патологических изменений в деятельности нервной системы у взрослых лиц, а по соотношениям парных идиотипических/антиидиотипических антител судят о давности и динамике развития патологического процесса.
Способ по изобретению позволяет:
1. Регистрировать патологические изменения в сывороточном содержании е-аАТ, взаимодействующих как с белками нервных клеток (белки S100, GFAP, МВР), так и с главным белком миелиновой оболочки нервных волокон (белок NGF), а также е-аАТ, взаимодействующих с основными нейромедиаторами нервной системы (ГАМК, глутамин, дофамин, серотонин), и е-аАТ, взаимодействующих с мембранными рецепторами перечисленных нейромедиаторов.
2. Регистрировать патологические изменения в сывороточном содержании перечисленных выше е-аАТ первого порядка (идиотипов), равно как и е-аАТ второго порядка (специфических анти-антител; антиидиотипических антител).
Все это существенно расширяет спектр детектируемых форм патологии нервной системы и позволяет надежно судить о динамике и стадии развития патологического процесса в нервной ткани и давности заболевания.
Практически способ осуществляют следующим образом.
В результате сорбции на стандартные 96-луночные полистироловые планшеты для ИФА а) антиген-связывающих фрагментов или цельных молекул антиидиотипических антител-иммунохимических аналогов эпитопов белков S100, GFAP, МВР и NGF; б) антиген-связывающих фрагментов или цельных молекул идиотипических антител; в) конъюгатов молекул нейромедиаторов - ГАМК, глутамата, серотонина, дофамина, используемых для оценки содержания соответствующих антимедиаторных антител первого порядка; г) антиген-связывающих фрагментов или цельных молекул идиотипических антител к указанным нейромедиаторам, используемых для оценки содержания соответствующих антител второго порядка, одновременно являющихся антителами к рецепторам соответствующих нейромедиаторов.
I. Нанесения на них тестируемых проб сывороток и эталонной референс-сыворотки, полученной от здоровых лиц.
II. Выявлении образующихся антиген-антительных комплексов с помощью конъюгатов вторичных (антивидовых) иммуноглобулинов, меченных пероксидазой хрена или иным ферментом.
III. IV. Проявления реакции в лунках планшета с помощью субстрата-хромогена.
IV. Сравнения интенсивности реакции в лунках, содержащих тестируемые сыворотки с лунками, содержащими референс-сыворотку.
Для проведения анализа ЭЛИ-Н-Тест требуется около 0,03 мл сыворотки крови обследуемого (например, полученной из подушечки пальца).
ПОЛУЧЕНИЕ ОСНОВНЫХ КОМПОНЕНТОВ, ИСПОЛЬЗУЕМЫХ В ТЕСТ-СИСТЕМЕ ЭЛИ-Н-ТЕСТ
1. Получение антиген-связывающих фрагментов или цельных молекул-идиотипических антител к белкам S100, GFAP, MBP и NGF. Для получения данных компонентов тест-системы проводили иммунизацию кроликов белками S100, GFAP, MBP и NGF; из иммунной сыворотки с помощью иммуноаффинной хроматографии на колонках с иммобилизованными белками S100, GFAP, MBP и NGF выделяли соответствующие идиотипические антитела (антитела первого порядка) и в результате протеолитической обработки получали их F(ab)- или Р(ab)2-фрагменты. Полученный материал (в виде антигенсвязывающих фрагментов или цельных молекул идиотипических антител (AT1)) использовался в работе.
2. Получение антиген-связывающих фрагментов или цельных молекул антиидиотипических антител (АТ2) - иммунохимических аналогов эпитопов белков S100, GFAP, МВР и NGF. Для получения данных компонентов тест-системы проводили иммунизацию кроликов F(ab)2-фрагментами поликлональных антител к соответствующим белкам; из иммунной сыворотки с помощью иммуноаффинной хроматографии на колоннах с иммобилизованными поликлональными антителами к белкам S100, GFAP, MBP и NGF выделяли соответствующие антиидиотипические антитела и в результате протеолитической обработки получали их F(ab)- или F(ab)2-фрагменты. Полученный материал (в виде антигенсвязывающих фрагментов или цельных молекул антиидиотипических антител) использовался в работе.
3. Получение конъюгатов молекул нейромедиаторов - ГАМК, глутамата, серотонина, дофамина, используемых для оценки содержания соответствующих антимедиаторных антител первого порядка. Для получения данных компонентов тест-системы проводили ковалентную сшивку соответствующих нейромедиаторов с желатином, альбумином или иным макромолекулярным носителем. Полученный материал использовался в работе.
4. Получение антиген-связывающих фрагментов или цельных молекул-идиотипических антител к нейромедиаторам ГАМК, глутамату, серотонину и дофамину. Для получения данных компонентов тест-системы проводили иммунизацию кроликов конъюгатами молекул нейромедиаторов - ГАМК, глутамата, серотонина, дофамина; из иммунной сыворотки с помощью иммуноаффинной хроматографии на колонках с иммобилизованными нейромедиаторами выделяли соответствующие идиотипические антитела (антитела первого порядка) и в результате протеолитической обработки получали их F(ab)- или F(ab)2-фрагменты. Полученный материал (в виде антиген-связывающих фрагментов или цельных молекул идиотипических антител) использовался в работе.
МЕТОДИКА ПРОВЕДЕНИЯ НЕПРЯМОГО ИФА
1. Для сорбции на стандартные 96-луночные плоскодонные планшеты для иммуноферментного анализа готовят растворы каждого из компонентов тест-системы на карбонатном буфере рН 9-10. Приготовленные растворы вносят в отдельные лунки планшета. Планшеты инкубируют ночь при +2...+4°С.
2. Удаляют (стряхнуть) из лунок растворы компонентов и (без дополнительной отмывки) заливают в них блокирующий буфер (например, 0.5% раствор желатина на 0,15 М NaCl).
3. После инкубации отмывают планшеты отмывочным буфером (например, 0.15 М NaCl с 0.05% твин-20).
4. Внесение тестируемых сывороток:
а) в отдельных флаконах или ванночках или ИФА готовят разведения сывороток (например, 1:200) на отмывочном буфере.
б) вносят разведенные сыворотки в лунки.
в) планшеты инкубируют ночь при +4°С.
5. Отмывают планшеты отмывочным буфером.
6. Проявление реакции:
а) исходный раствор конъюгата пероксидазы хрена (или иного фермента) с антителами к иммуноглобулинам IgG человека разводят в необходимое число раз (в зависимости от его активности) отмывочным буфером; б) раствор конъюгата вносят во все лунки планшета; в) планшеты инкубируют 60-90 мин при 37°С, либо 12-16 час при +2...+4°С. Конъюгат удаляют, а планшеты отмывают отмывочным буфером; г) сразу после этого в лунки вносят раствор субстрата-хромогена (например, 0.01-0.05% о-фенилендиамина с 0.001-0.01% перекиси водорода на 0.01-0.05 М цитрат-фосфатном буфере в случае применения пероксидазных конъюгатов). Инкубируют планшеты в темноте 15-20 мин при комнатной температуре.
7. По достижении оптимального уровня окрашивания (обычно через 10-20 мин инкубации в темноте) реакцию останавливают добавлением 0.2-0.4 М кислоты.
8. Регистрация результатов реакции: интенсивность окрашивания оценивают с помощью иммуноферментного анализатора (ИФА-ридера) любой модели.
9. Обработка полученных данных:
По полученным значениям оптической плотности лунок рассчитывают относительную интенсивность реакции тестировавшихся сывороток с каждым из компонентов тест-системы ИЛИ-Н-Тест по отношению к реакции контрольной сыворотки с тем же антигеном за минусом 100 единиц и выражают в условных единицах. Для расчета используют формулу
Обозначения:
R(ar1) - величина оптической плотности анализируемой сыворотки крови в лунках с антигеном - 1;
R(ar2) - величина оптической плотности анализируемой сыворотки крови в лунках с антигеном-2;...
R(arn) - величина оптической плотности анализируемой сыворотки крови в лунках с антигеном-n;
R(к1...кn) - величина оптической плотности контрольной сыворотки крови в лунках с антигенами 1...n.
10. Интерпретация полученных данных:
а) в случае, если интенсивность реакции исследуемой сыворотки взрослых с любым из компонентов тест-системы не выходит за пределы от -25% до +15% по отношению к реакции сыворотки-эталона, данную сыворотку относят к 1-й классификационной группе или группе нормы (вероятность возникновения психо-невропатологии минимальна). Для новорожденных и детей до пубертата параметры нормы не выходят за пределы от -40% до 0;
б) в случае, если интенсивность реакции исследуемой сыворотки с любым из компонентов выходит за пределы группы 1, но не превышает отклонений от -40% до +40% по отношению к реакции сыворотки-эталона, данную сыворотку относят ко 2-й классификационной группе или группе умеренных отклонений (малый/умеренный риск развития психоневропатологии). Для новорожденных и детей до пубертата параметры нормы не выходят за пределы от 60% до +10;
в) в случае, если интенсивность реакции исследуемой сыворотки с любым из компонентов выходит за пределы 1-й и 2-й групп, данную сыворотку относят к 3-й классификационной группе или группе выраженных отклонений (признаки наличия нервно-психического заболевания или высокий риск его развития);
г) вероятность благоприятного/неблагоприятного прогноза развития (нормального формирования) нервной системы у новорожденных и детей раннего возраста, так и в плане нормальной деятельности нервной системы прямо зависит от уровней нормы/отклонений от нормы, определяемых е-аАТ в сыворотке крови обследуемых, а частота аномалий в формировании и функционировании нервной системы прямо коррелирует с уровнем отклонений. Чем более выражены отклонения, тем выше риск возникновения аномалий функционально-морфологического развития нервной системы;
д) риск развития патологических изменений в нервной системе у взрослых лиц прямо коррелирует с уровнями отклонений от нормы, определяемых е-аАТ в сыворотке крови обследуемых. Чем более выражены отклонения, тем выше риск развития заболеваний центральной или периферической нервной системы;
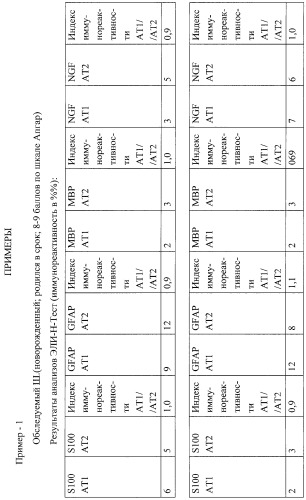
3+-е) нормальные соотношения между идиотипическими и антиидиотипическими антителами (Индексы АТ1/АТ2) у любой из пар близки к 1,0 (должны укладываться в диапазон 0,8...1,2). Преимущественно повышенный уровень антител первого порядка (идиотипов) указывает на небольшую длительность (не более 1 мес) патологического процесса. Преимущественно повышенный уровень антител второго порядка (антиидиотипов) свидетельствует о давности (хронизации) патологического процесса (более 6 мес). По динамике изменений в соотношениях парных идиотипических и антиидиотипических е-аАТ можно судить как о нарастании негативных тенденций, так и о нормализации функций нервной системы, например на фоне эффективного лечения.
Необходимо отметить, что выполнение анализов производится в условиях in vitro без какого-либо вреда для обследуемого.
Способ выявления лиц группы риска развития патологии нервной системы, включающий получение сыворотки, проведение иммуноферментного анализа для выявления содержания антиидиотипических антител (антител второго порядка) к антигенам нервной ткани с последующим рассчётом показателей иммунореактивности и скрининг пациентов по уровню иммунореактивности, отличающийся тем, что определяют иммунореактивность как антиидиотипических (АТ2) так и идиотипических антител (AT1) к антигенам нервной ткани: белкам: S100, GFAP, МВР и NGF, а также к нейромедиаторам: ГАМК, глутамату, серотонину, дофамину и к рецепторам нейромедиаторов и по степени отклонения иммунореактивности от нормы в соотношениях идиотипических и антиидиотипических антител судят о риске развития патологии нервной системы.